锗及其化合物被广泛应用于半导体、催化剂等领域。以铅锌矿含锗烟尘为原料可制备GeO2,其工艺流程图如下。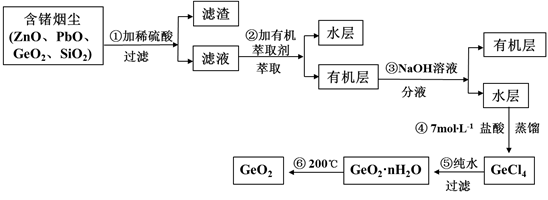
已知:GeO2是两性氧化物;GeCl4易水解,沸点86.6℃
(1)第①步滤渣主要成分有 (填化学式),实验室萃取操作用到的玻璃仪器有 。
(2)第③步萃取时,锗的萃取率与V水相/V有机相(水相和有机相的体积比)的关系如下图所示,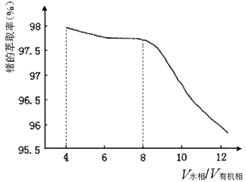
从生产成本角度考虑,较适宜的V水相/V有机相的值为 。
(3)第④步加入盐酸作用 (答两点即可)。
(4)第⑤步反应的化学方程式 。
(5)检验GeO2·nH2O是否洗涤干净的操作是 。
(6)GeO2产品中通常混有少量SiO2。取样品5.4g,测得其中氧原子的物质的量为0.105mol,则该样品中GeO2的物质的量为_____ mol。
以下装置图中,A是氯气的发生装置,B、C是净化气体的装置,D中装铁丝网;反应后E的底部有棕黄色固体聚集;F是吸收多余气体的装置。
(1)实验前检查整套装置气密性的方法是:
(2)A装置中分液漏斗中装什么药品,烧瓶中装什么药品。
(3)B中所盛装的是,作用是;
C中所盛装的是,作用是。
(4)写出A、D、F三个装置中发生反应的化学方程式
(5)化学实验中检验是否有Cl2产生常用湿润的淀粉-KI试纸。如有Cl2产生,可观察到的现象是,写出反应方程式。
选择下列实验方法分离物质,将分离方法的序号填在横线上。
| A.萃取分液 | B.升华 | C.结晶 | D.分液 E.蒸馏 F.过滤 |
(1)分离饱和食盐水与沙子的混合物______
(2)从硝酸钾和氯化钠的混合液中获得硝酸钾______
(3)分离水和 汽油的混合物______
汽油的混合物______
(4)分离酒精(沸点为78.1℃)和甲苯(沸点为110.6℃)两种互溶液体______
(5)从碘水中提取碘单质
某实验小组用下列装置进行乙醇催化氧化的实验。

 (1)实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学方程式
(1)实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学方程式 、 。
、 。 (2)甲和乙两个水浴作用不相同。
(2)甲和乙两个水浴作用不相同。 甲的作用是 ;乙的作用是。
甲的作用是 ;乙的作用是。 (3)反应进行一段时间后,试管a中能收集到不同的物质,它们是。集气瓶中收集到的气体的主要成分是。
(3)反应进行一段时间后,试管a中能收集到不同的物质,它们是。集气瓶中收集到的气体的主要成分是。 (4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有。
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有。 要除去该物质,可在混合液中加入(填写字母)。
要除去该物质,可在混合液中加入(填写字母)。 a.氯化钠溶液 b.苯 c.碳酸氢钠溶液 d.四氯化碳
a.氯化钠溶液 b.苯 c.碳酸氢钠溶液 d.四氯化碳
然后,再通过 (填试验操作名称)即可除去。
(16分,每空2分)用质量分 数为98%,密度为1.84 g•cm-3的浓硫酸配制100mL物质的量浓度为1mol/L的稀硫酸。
数为98%,密度为1.84 g•cm-3的浓硫酸配制100mL物质的量浓度为1mol/L的稀硫酸。
(1)需要使用的主要仪器有量筒、烧杯、玻璃棒、、。
(2)其操作步骤可分解为以下几步:
A.用量筒量取mL浓硫酸,缓缓注入装有约50mL蒸馏水的烧杯里,并用玻璃 棒搅拌
棒搅拌
B.用约30mL蒸馏水分三次洗涤烧杯和玻璃棒,将每次的洗液 都倒入容量瓶里
都倒入容量瓶里
C.将稀释后的硫酸小心地用玻璃棒引流容量瓶里
D.检查100mL容量瓶,是否漏水
E.将蒸馏水直接加入容量瓶,至液面接近刻度线
F.盖紧瓶塞,反复颠倒振荡,摇匀溶液
G.用胶头滴管向容量瓶里逐滴加入蒸馏水,到液面最低点恰好与刻线相切
请据此填写:
①完成上述步骤中的空白处。
②正确的操作顺序是(用字母填写):
()→()→()→()→()→()→()。
③进行A步操作时,选用量筒的规格是。(选填字母)
A.10mL B.50mL C.100mL D.1000mL
④如果对装有浓硫酸的量筒仰视读数,配制的稀硫酸浓度将(选填“偏高”、“偏低”、“无影响”)。
⑤A步骤操作完成时,必须后,才能进行后面的操作。
某次化学兴趣小组活动上,三组学生分别用图示甲、乙两装置,探究“NaHCO3和Na2CO3与稀盐酸的反应”,按表中的试剂用量,在相同条件下,将两个气球中的固体粉末同时倒入试管中(装置的气密性已检查)请回答:
(1)各组反应开始时,______装置中的气球体积先变大,该装置中反应的离子方程式是。
(2)当试管中不再有气体生成时,三组实验出现不同现象。请参照第①组,分析原因的方式填写下表的空格