〔化学—选修3:物质结构与性质〕(15分)已知A、B、C、D、E五种元素的原子序数依次递增,A、B、C、D位于短周期。A位于周期表的s区,其原子中电子层数和未成对电子数相同;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子最外层电子数是次外层电子数的3倍。E有“生物金属”之称,E4+和氩原子的核外电子排布相同。
请回答下列问题:
(1)B、C、D三种元素的电负性由小到大的顺序为 ,E的基态原子的电子排布式为 。
(2)由B、D形成的BD32-离子中,其VSEPR模型名称是 ,离子的中心原子采用 杂化。
(3)已知由A、C、D三种元素按照4:2:3的原子个数比可形成某离子化合物,常温下测得该离子化合物的水溶液pH=5,则该溶液中水电离出的氢离子浓度为 。
(4)D、E和钡三种元素构成的某化合物的晶胞结构如图所示,该化合物的化学式为 。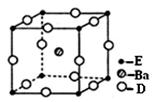
纳米级的EO2是一种广泛使用的催化剂,实验室往往通过ECl4在大量水中加热水解制得EO2·xH2O,该反应的化学方程式为 。
某些化学反应可以表示为: A + B → C + D + H2O请回答下列问题:
(1)若A为红色的金属单质,B为第二周期某种元素的最高价氧化物的水化物,D在常温下可以转化为具有相同化合价的另一种氧化物E,则D和E分别为;
(2)若D分子的空间构型为三角锥形,C在实验室中常用作干燥剂,则A的晶体类型为、电子式为;
(3)若C、D均为气体且都能使澄清石灰水变浑浊,写出该反应的化学方程式;
(4)若A、C、D均含有氯元素,且A的化合价介于C与D之间,写出该反应的离子方程式:;
A~I分别表示中学化学中常见的一种物质,它们之间相互关系如下图所示(部分反应物、生成物没有列出),且已知G为主族元素的固态氧化物,A、B、C、D、E、F六种物质中均含同一种元素。
请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含的同一种元素在周期表中的位置为 ;
(2)写出反应⑥的化学方程式 ;
(3)写出反应④的离子方程式 ;
(4)写出反应③阳极的电极反应式 ;
(5)反应①中每生成3molA,转移电子的物质的量为 。
减少SO2的排放、回收利用SO2成为世界性的研究课题。我国研究人员研制的利用低品位软锰矿浆(主要成分是MnO2)吸收废渣高温焙烧产生的SO2,制备硫酸锰的生产流程如下:
浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+、Ca2+、Pb2+等其他金属离子。
有关金属离子的半径以及形成氢氧化物沉淀时的pH见下表,阳离子吸附剂吸附金属离子的效果见下图。
| 离子 |
离子半径(pm) |
开始沉淀时的pH |
完全沉淀时的pH |
| Fe2+ |
74 |
7.6 |
9.7 |
| Fe3+ |
64 |
2.7 |
3.7 |
| Al3+ |
50 |
3.8 |
4.7 |
| Mn2+ |
80 |
8.3 |
9.8 |
| Pb2+ |
121 |
8.0 |
8.8 |
| Ca2+ |
99 |
- |
- |
已知PbO2的氧化性大于MnO2。请回答下列问题:
⑴ 写出浸出过程中主要反应的化学方程式,氧化过程中主要反应的离子方程式。
⑵ 在氧化后的液体中加入石灰浆,用于调节pH,pH应调节至。
⑶ 阳离子吸附剂用于除去杂质金属离子。决定阳离子吸附剂吸附效果的因素是(填写序号)。
a.溶液的pHb.金属离子的电荷c.金属离子的半径d.吸附时间
⑷ 操作a包括等过程。
空气质量高低直接影响着人类的生产和生活,它越来越受到人们的关注。被污染的空气中杂质的成分有多种,其中计入《空气质量日报》空气污染指数的项目有SO2、CO、NO2、O3和可吸入颗粒物等。
请回答下列问题:
⑴ S、N、O的第一电离能由大到小的顺序为。
⑵ 血红蛋白中含有Fe2+,CO易与血红蛋白结合成稳定的配合物而使人中毒。
① 写出亚铁离子的基态电子排布式。
② CO有多种等电子体,其中常见的两种为。
⑶ SO2是一种大气污染物,为减轻SO2污染,火力发电厂生产中常在
燃煤中加入CaO以“固硫”。 CaO晶胞如右图所示,其中Ca2+的配位
数为,CaO晶体和NaCl晶体中离子排列方式相同,其晶格能分
别为:CaO-3401kJ/mol、NaCl-786kJ/mol。CaO晶体的熔点NaCl
晶体的熔点(填“高于”、“等于”或“低于”)。
⑷ 随着人们生活质量的提高,不仅室外的环境安全为人们所重视,室内的环境安全和食品安全也越来
越为人们所关注。甲醛是室内主要空气污染物之一(其沸点是-19.5 ℃),甲醇是“假酒”中的主要
有害物质(其沸点是64.65 ℃),甲醇的沸点明显高于甲醛的主要原因是:。
BAD是一种紫外线吸收剂,其合成方法如下:
已知:
Ⅰ、B分子中所有H原子的化学环境相同;
Ⅱ、BAD的结构为: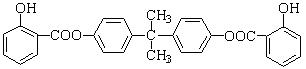 。
。
请回答下列问题:
⑴ A的名称为。
⑵ F的结构简式为。F的一些同分异构体能使氯化铁溶液变色,能发生银镜反应,且苯环上的一硝基取代产物有两种。符合上述条件的同分异构体有种。
⑶ 反应②的化学方程式为;反应③在一定条件下能直接进行,其反应类型为。
⑷ G是一种氨基酸,且羧基和氨基处于苯环的对位。写出G缩聚产物可能的结构简式(只要求写一种)。