【化学-有机化学基础】(13分)芳香族化合物水杨酸、冬青油、阿司匹林都是常用西药。它们的结构简式如下表:
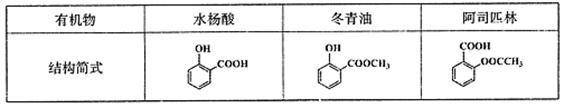
(1)阿司匹林分子中能发生水解反应的官能团名称是 。
(2)关于水杨酸的说法正确的是 (填序号)。
a.属于芳香族化合物
b.0.1mol水杨酸完全燃烧消耗氧气的体积是15.68L
c.能发生取代反应,但不能发生加成反应
d.可用氯化铁溶液鉴别水杨酸和阿司匹林
(3)水杨酸在一定条件下可以聚合成高分子化合物聚水杨酸,反应的化学方程式为: 。
(4)符合下列条件的冬青油的同分异构体有_______种。
①苯环上有3个取代基,但不存在甲基;
②能发生银镜反应;
③1mol该有机物最多消耗2mol氢氧化钠。
其中苯环上的一卤代物有两种的有机物结构简式为____________________。
(5)效果更佳的长效缓释阿司匹林(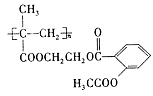 )在人体内可缓慢释放出阿司匹林分子,反应的化学方程式为 ,反应类型为 。
)在人体内可缓慢释放出阿司匹林分子,反应的化学方程式为 ,反应类型为 。
今有aX、bY、cZ三种元素。已知:①各原子序数a、b、c均小于20,且a+b+c=25; ②元素Y的原子价电子构型为ns2npn+2; ③X和Y在不同条件下可形成X2Y和X2Y2两种化合物,Y和Z在不同条件下可形成ZY和ZY2两种化合物; ④Z的硫化物的相对分子质量与Z氯化物的相对分子质量之比为38︰77。回答下列问题:
(1)X: (写元素名称);Z的价电子排布图为: 。
(2)X2Y2的电子式 ,属于 化合物(填“离子”或“共价”)。
(3)Z的硫化物的VSEPR模型为 ,分子空间构型为 ;Z的氯化物的VSEPR模型和分子空间构型分别是 、 ,其中Z原子分别以 杂化轨道成键,根据原子轨道成键方式分,Z的硫化物分子中含有的键的种类及数目是 、 。
下表为长式周期表的一部分,其中的编号代表对应的元素。
| ① |
|||||||||||||||||
| ② |
③ |
||||||||||||||||
| ④ |
⑤ |
⑥ |
⑦ |
||||||||||||||
| ⑧ |
⑨ |
⑩ |
请回答下列问题:
(1)按电子排布,可把周期表中的元素划分成5个区,请在上图中划出区域并注明。
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状分子名称为 ;③和⑦形成的一种常见溶剂的化学式为 ,其立体构型为__________,键角为______。
(3)某元素原子的价电子排布式为nsnnpn+1,该元素原子的最外电子层上孤电子对数为 ;该元素与元素①形成的最简单分子X属于 分子(填“极性”或“非极性”)。
(4)元素④的第一电离能 元素⑤(选填“>”、“=”、“<”)的第一电离能;元素⑥的电负性 元素⑦(选填“>”、“=”、“<”)的电负性。
(5)元素⑥和①形成的化合物的结构式为 ; 元素⑨的基态原子核外电子排布式是 。
(6)某些不同族元素的性质也有一定的相似性,如上表中元素②与元素⑤的氢氧化物有相似的性质。请写出元素②的氢氧化物与NaOH溶液反应的化学方程式
将27.4g Na2CO3和NaHCO3的混合物平均分成等量的两份,一份溶于水后加入足量某浓度的盐酸恰好完全反应,收集到CO2气体V L ,消耗盐酸100 mL。另一份直接加热至恒重,生成CO2气体1.12 L(所有气体体积均在标准状况下测定)。试计算:
(1)原混合固体中Na2CO3和NaHCO3的物质的量之比:n(Na2CO3):n(NaHCO3)=____________;
(2)盐酸的物质的量浓度c(HCl)=______________mol·L-1。
现有部分元素的原子结构特点如下表:
| X |
其单质之一是空气中主要成分,最常见的助燃剂 |
| Y |
其某种核素不含中子 |
| Z |
失去一个电子后,形成Ne原子电子层结构 |
| W |
最外层电子数是次外层电子数的2倍 |
(1)写出各元素的元素符号:X_______,Y________,
(2)画出下列微粒的结构示意图Z+________,W原子__________。
(3)写出两种由上述任意三种元素组成的水溶液呈碱性的物质_____________、___________。(填化学式)
有以下几种物质:①食盐颗粒②硫酸铜晶体③KNO3溶液④熔融的氢氧化钾。
回答以下问题(填序号):
(1)物质中构成的微粒只能在固定位置上振动的是_________________;
(2)以上物质中能导电且属于电解质的是___________________;