【改编】Ⅰ.(8分)利用下图装置作电解50mL 0.5 mol·L-1的CuCl2溶液实验。
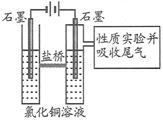
实验记录:
A.阳极上有黄绿色气体产生,该气体使湿润的淀粉碘化钾试纸先变蓝后褪色(提示:Cl2氧化性大于IO3-);
B.电解一段时间以后,阴极表面除有铜吸附外,还出现了少量气泡和浅蓝色固体。
(1)分析实验记录A中试纸颜色变化,用离子方程式解释:① ;
② 。
(2)分析实验记录B中浅蓝色固体可能是 (写化学式),试分析生成该物质的原因 。
Ⅱ.(10分)A、B、C、D、E、F六种元素的原子序数依次递增,A+核外无电子,B元素的一种单质是自然界中最硬的物质,C、D、E的简单离子具有相同的核外电子排布,舍勒是D元素单质的发现者之一,戴维最早制得了E元素的单质,F元素的单质历史上曾作为流通货币,A、C、D、F四种元素形成的化合物W可用于制镜工业。
(1)D、E两元素通常可形成两种离子化合物,其中一种化合物X可用做供氧剂,X与A2D反应会产生大量气体,该气体能使带火星的木条复燃。请写出X与A2D反应的化学方程式 。
(2)A、B、D、E四种元素形成的某化合物,摩尔质量为68 g·mol-1,请用离子方程式解释其水溶液呈碱性的原因 。
(3)B、C的氧化物是汽车尾气中的主要有害物质,通过钯碳催化剂,两者能反应生成无毒物质,请写出该反应的化学方程式 。
(4)W的水溶液久置会析出一种沉淀物Z,Z由C、F两元素形成且两元素原子个数比为1:3,Z极易爆炸分解生成两种单质。请写出Z分解的化学方程式 。请从化学反应原理的角度解释Z能发生分解反应的原因 。
(1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是 。(填字母)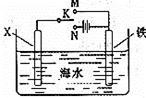
A.C(s)+H2O(g)=CO(g)+H2(g) △H>0
B.NaOH(aq)+HC1(aq)=NaC1(aq)+H2O(1) △H<0
C.2CO(g)+O2(g)=2CO2(1) △H<0
(2)以KOH溶液为电解质溶液,依据所选反应设计一个原电池,其负极的电极反应式为 。
(3)利用右图装置,可以模拟铁的电化学防护。若X为碳棒,为减缓铁的腐蚀,开关K应该置于 处,此时溶液中的阴离子向极(填X或铁)移动。
[化学—选修有机化学基础]
A、B、C、D、E、F、G都是链状有机物,它们的转化关系如图所示,D的相对分子质量与E相差42,请回答下列问题;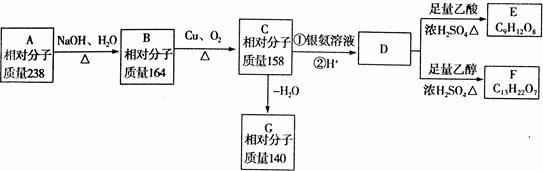
(1)D中含有的官能团是_________;D的分子式为________。
(2)D的核磁共振氢谱图上有3个峰,且峰面积之比为1:3,请写出D的结构简式__________。
(3)写出B生成C的化学方程式___________.
(4)A只含一种官能团,则A的结构简式为___________。
(5)芳香族化合物H与G互为同分异构体,1molH与足量氢氧化钠溶液反应消耗2molNaOH,且H苯环上的一氯代物只有两种,写出符合条件的H的结构简式:______。
[化学—选修物质结构和性质]
下表为部分短周期元素的性质或原子结构,已知A—D的原子序数依次增大。
| 元素编号 |
元素性质或原子结构 |
| A |
A原子所处的周期数、族序数、原子序数均相等 |
| B |
核外电子有6种不同运动状态 |
| C |
最简单氢化物的水溶液呈碱性 |
| D |
基态原子的S轨道电子数等于P轨道电子数 |
请结合表中信息完成下列各小题(答题时用所对应的元素符号)
A:(1)写出C原子的电子排布图____________
(2)A、B、C、D的第一电离能由大到小的顺序为______________
(3)用电离方程式表示C的最简单氢化物的水溶液呈碱性的原因_______________
B:按照共价键理论,分子中每个原子的最外电子层电子数均已饱和。已知ABCD分子可能有三种不同结构,它们的结构可以从其他物质的结构中获得启发。
(4)ABC的结构式是___________。向其中插入一个D原子,若形成配位键(用→表示)则ABCD的结构式为______________分子中C的原子的杂化类型是______________;若无配位键则ABCD的结构式为___________分子中D原子的杂化类型为______________。
(5)BD2的电子式是____________将D原子换成等电子的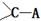 所得ABCD的结构式为________,分子中C原子的杂化类型是______________。
所得ABCD的结构式为________,分子中C原子的杂化类型是______________。
(6)在ABCD的三种可能结构中B原子的杂化类型__________(填“相同”或“不相同”)
有关物质存在如图所示的转化关系(部分产物已省略)。通常C为气体单质,G为紫黑色固体单质。实验室中常用固体E在B的催化下加热制取气体单质H。
请回答下列问题: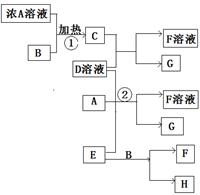
(1)反应①的化学方程式为____________________
(2)反应②的离子方程式为____________________
(3)写出另外一种实验室制取H的化学方程式_______________________
(4)D溶液与Pb(NO3)2溶液混合可形成沉淀,此沉淀的KSP=7.0×10-9。将等体积的D溶液与Pb(NO3)2溶液混合。若D的浓度为1×10-2mol/L,则生成沉淀所需Pb(NO3)2溶液的最小浓度为_______
钛(Ti)被称为继铁、铝之后的第三金属。如下图所示,将钛厂、氯碱厂和甲醇厂组成产业链可以大大提高资源利用率,减小环境污染。请填写下列空白: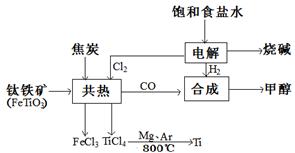
(1)电解饱和食盐水时,该反应的离子方程式是____________________。
(2)已知:①Mg(s)+Cl2(g)=MgCl2(s);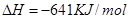
②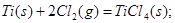
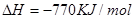
则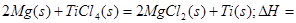 ____________
____________
反应: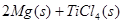
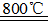
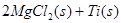 在Ar气氛中进行的理由是________
在Ar气氛中进行的理由是________
(3)写出钛铁矿与焦炭、Cl2共热制得四氯化钛的化学方程式______________________
(4)以甲醇、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。已知该燃料电池的总反应式为:2CH3OH+3O2+4OH-=2CO32-+6H2O,该燃料电池发生反应时正极区溶液的PH_____(填“增大”、“减小”或“不变”)该电池中负极上的电极反应是__________.
(5)在上述产业链中合成96t甲醇理论上消耗H2_________t(不考虑生产过程中物质的任何损失)