以天然气为原料合成尿素的主要步骤如图所示(图中某些转化步骤及生成物未列出):
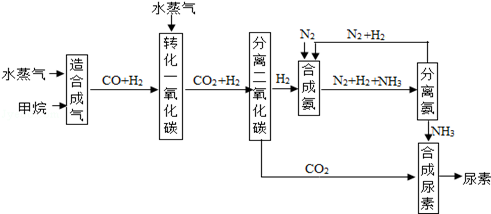
(1)尿素与熟石灰混合研磨 (填“有”或“无”)刺激性气味.
(2)甲烷和水蒸气在高温及催化剂的条件下反应,生成CO和H2,该反应的化学方程式为 .
(3)分离出氨后,可循环利用的两种物质是 、 .
(2013襄阳)小强同学用三支试管,分别取适量的稀盐酸、澄清石灰水、碳酸钠溶液,进行相关实验探究。
步骤1:向三支试管中分别滴加酚酞后,Na2CO3溶液中显红色,说明Na2CO3溶液显_____性;
步骤2:小强把三支试管中的溶液同时倒入一只烧杯中,发现有气泡产生,最终有白色沉淀生成且溶液显红色;
步骤3:把烧杯中的混合物进行过滤,得到滤液,滤液中一定不含有________。
A.稀盐酸 B.澄清石灰水 C.碳酸钠溶液)
[实验猜想]步骤3所得滤液中溶质可能为:
①NaCl Na2CO3;②NaCl CaCl2和NaOH;③NaCl Na2CO3和NaOH;④……
[实验验证](提示:CaCl2溶液显中性)
| 实验操作 |
实验现象 |
实验结论 |
| 取少量滤液于试管中,加入足量CaCl2溶液 |
|
猜想③成立 |
[反思评价]有同学提出将CaCl2溶液改为稀盐酸,若观察到有气泡产生且红色消失,则证明猜想③成立。小刚同学认为不正确,其理由是:___________________________。
某兴趣小组对物质的性质进行相关探究、
【提出问题】氯化氢(HCl)气体显酸性吗?
【进行实验】该兴趣小组的同学根据二氧化碳与水反应的实验探究方法,用三朵由紫甘蓝的汁液染成蓝紫色的纸质干燥小花进行如图1的三个实验:
实验现象:Ⅰ和Ⅱ中小花不变色;Ⅲ中小花变红色.
【查阅资料】图2是同学们查阅的氯化氢气体溶于水的示意图.
【实验结论】氯化氢气体不显酸性.
【交流反思】
(1)从微观角度分析氯化氢气体不显酸性的原因是__________________.
(2)小明向实验Ⅲ中变红的小花上喷足量的稀氢氧化钠溶液,发现小花最后变成黄绿色,写出相关反应的化学方程式_____________________.
(3)紫甘蓝的汁液在酸性溶液中显__________色.
(4)下列实验可以用来说明氯化氢气体不显酸性的是___________.
| A.测试盐酸的导电性,盐酸能导电 |
| B.干燥的碳酸钠粉末放入氯化氢气体中,不反应 |
| C.氢气与氯气反应,生成氯化氢气体 |
| D.干燥的碳酸钠粉末放入盐酸中,能反应 |
某化学课堂上同学们正在进行酸、碱、盐知识的探究,以下是教学片断,请你参与其中并认真填写空格.
【学生实验】将二氧化碳分别通入澄清石灰水和氢氧化钠溶液中,观察到前者变浑浊,后者无明显现象.
【学生板演】澄清石灰水变浑浊的原理 (用化学方程式表示)
【提出问题】二氧化碳通入氢氧化钠溶液中无明显现象,两者是否发生了化学反应?
【猜想假设】猜想①:两者发生了化学反应;猜想②:两者没有发生化学反应
【实验探究】
(1)小华设计了如图所示的A、B两个实验.
实验现象:A中软塑料瓶変瘪,B中
(2)小红认为小华的实验是可行的,其共同原理是二氧化碳和氢氧化钠溶液反应,使容器内压强降低.小明同学却对此提出质疑,他认为小华的实验不严谨,其理由是 ,要得到科学严谨的结论,仍利用该装置,补做的对比实验是 .
(3)小宁设计的是通过检验生成物来验证猜想,请帮她填写实验报告.
| 实验步骤 |
实验现象 |
实验结论 |
| 向B实验后的溶液中加入 |
验证了二氧化碳和氢氧化钠溶液反应 |
【实验结论】二氧化碳和氢氧化钠溶液发生了反应.
【反思拓展】通过此探究实验,我们发现,对于没有明显现象的化学反应,可以从两个不同的角度证明反应的发生,这两个角度是 ; .
(2013辽宁沈阳)化学小组同学探究“酸的化学性质”,请你参与并完成下列部分实验内容。
| 实验过程 |
实验现象 |
实验结论 |
(1) |
①号试管:固体溶解,产生气泡,放热; ②号试管: 。 |
a、金属活动性: 镁 铜(填“>”或“<”) b、涉及到的化学方程式 。 |
(2) |
③号试管:绿色粉末逐渐溶解,产生气泡,溶液显蓝色。 ④号试管:绿色粉末逐渐溶解,产生气泡,溶液显绿色。 |
Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2↑ Cu2(OH)2CO3+4HCl=2CuCl2+3H2O+CO2↑ |
【发现问题】碱式碳酸铜与稀硫酸反应形成的CuSO4溶液显蓝色,而与盐酸反应形成的CuCl2溶液显绿色。
【提出问题】同样都含有Cu2+,为什么③号试管中的CuSO4溶液显蓝色,而④号试管中的CuCl2溶液显绿色。
【猜想与假设】猜想一:若溶液中Cu2+显蓝色,则SO42+对Cu2+显色无影响,而Cl﹣对Cu2+显色有影响;
猜想二:若溶液中Cu2+显绿色,则 ;
猜想三:…
【实验验证】同学们用下列两种不同方案初步验证猜想一,请你补全实验所需试剂:
方案一:取少量③号试管中的溶液于另一支试管中,向其中加入 ,观察到预期实验现象,猜想一正确。
方案二:取少量④号试管中的CuCl2溶液于另一支试管中,向其中加入 ,观察到预期实验现象,猜想一正确。
【评价与反思】同学们在实验探究的过程中,体会到了溶液颜色成因复杂,相关知识还有待进一步学习。
初中化学课上,同学们利用下列实验探究碱的化学性质:
1)A实验中观察到的现象为 ,原因是(用化学方程式表示) 。
2)B实验中反应的化学方程式为 。
3)C实验中观察到的现象是 。
4)实验结束后,同学们将废液倒入同一只废液缸中,最后发现废液浑浊并显红色。
【提出问题】废液中含有什么物质?
【假设猜想】通过分析上述实验,同学们猜想:废液中除酚酞、碳酸钙及水以外一定含有 。
老师问:废液中还可能有什么物质?引发同学们热烈讨论,下面是大家的发言:
| 学生甲 |
可能有Ca(OH)2、NaOH |
学生丙 |
可能有Ca(OH)2、CaCl2 |
| 学生乙 |
可能有NaOH、Na2CO3 |
学生丁 |
可能有Na2CO3 |
| 学生戊 |
可能有NaOH |
…… |
………… |
【实验验证】同学们对可能含有的物质进行确定,取一定量的废液过滤,向滤液中逐滴加入氯化钡溶液,得到白色沉淀,红色褪去。
【结论】上述滤液中,还含有 ,没有 。