【2014年黑龙江省绥化市】牙膏摩擦剂的类型很多,如CaCO3,SiO2或它们的混合物.某兴趣小组对牙膏摩擦剂的成分进行了如下探究.
【提出问题1】某品牌牙膏中是否含有CaCO3?
【查阅资料】二氧化硅不与稀盐酸反应.
【实验方案】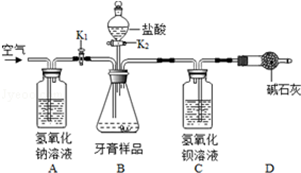
①取少量牙膏于试管中,加入适量的稀盐酸,出现气泡,将气体通入澄清石灰水,石灰水变浑浊,证明摩擦剂中含有_________ (填离子符号)
②取实验①中的溶液,加入碳酸钾溶液,生成白色沉淀,请写出该反应的化学方程式______ .
【提出问题2】该牙膏中CaCO3的质量分数是多少?
【实验装置】
【实验步骤】
(1)按如图连接好装置后,发现一处明显的错误,改正为_________ ;
(2)重新连接好装置,并_________ ;
(3)在B装置中加入牙膏样品8.00g;
(4)_________ K1,_________ K2(填“打开”或“关闭”),向牙膏样品中滴入10%的盐酸,至B中无气泡产生时,停止滴加盐酸;
(5)_________ ,至C中不再产生沉淀;
(6)将C装置中的固液混合物过滤、洗涤、烘干后称量其质量.实验数据如图(已知此品牌牙膏中的其他成分不和盐酸反应,装置内试剂均足量.)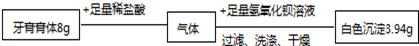
【实验分析及数据处理】
(1)若没有A装置,则测定结果将_________ (填“偏大”、“偏小”或“不变”)。
(2)D装置的作用是_________ .
(3)据上面数据,计算该牙膏样品中碳酸钙的质量分数是_________ .
如图是初中化学的一些基本实验,请回答相关问题:

(1)A实验是用烧杯罩住点燃的蜡烛,说明燃烧必须具备的条件之一是 ;
(2)B装置是电解水的实验,实验得出水由 组成;
(3)C实验是蒸发食盐水的实验,蒸发时用玻璃棒不断搅拌的目的是 ;
(4)根据D实验中得出的二氧化碳的有关性质,可知二氧化碳可用于 。
化学兴趣小组的同学在探究碱溶液的化学性质时,进行了如图所示的实验。

(1)实验A中,推入NaOH溶液后,可观察到的现象是 。
(2)实验B中发生反应的化学方程式为 。
实验结束后,小组同学对B试管中上层清液的溶质成分产生疑问,作出猜想:
猜想一:只含有NaOH;猜想二:含有NaOH、Na 2CO 3;猜想三:含有NaOH、Ca(OH) 2同学们取少量B试管中的清液分别置于甲、乙两支试管中,进行探究:
|
实验操作 |
实验现象 |
结论 |
|
在试管甲中滴加碳酸钠溶液 |
不产生白色沉淀 |
猜想三错误 |
|
在试管乙中滴加足量稀盐酸 |
|
猜想二正确 |
(3)A、B、C、D四个实验中能体现碱化学通性的是 (填字母)。小组同学经过讨论认为A、B、C、D四个实验并没有探究出碱所有的化学通性,从这四个实验中选择一个,继续加入相关试剂,能得出碱的其它化学通性,实验的方案是 (写出操作和现象)。
实验是化学研究的基础,结合下列实验装置及图示回答问题。

(1)图中a的仪器名称是 。
(2)"绿色化学"要求利用化学原理从源头上消除污染,实验室制取氧气的方法中最能体现绿色化追求的途径是 (填编号),该反应的化学方程式是 。
(3)若用二氧化锰和双氧水混合加热制备氧气,应选择的发生装置和收集装置的组合是 (填字母编号)。
(4)做铁丝在氧气中燃烧的实验改进如图3所示,其优点是实验简便、保证安全和 。
化学是一门以实验为基础的自然科学,化学实验和科学探究离不开装置。
|
制取气体的常用装置 |
|
|
|
|
收集气体的常用装置 |
|
|
|
|
干燥气体的常用装置 |
|
|
此格空白 |
(1)制取气体时,首先要对发生装置进行气密性的检查,确保装置不漏气。检查装置C气密性的方法是:首先将导管的末端浸在水中,然后用双手紧握试管,一会儿发现导管末端 ,松开双手后,导管末端液面上升,形成一段稳定的水柱,说明装置的气密性良好。
(2)收集气体的方法主要决定于气体的性质。装置F所示的收集方法是 ,被收集气体的密度 空气的密度(填"大于"、"等于"或"小于");如果用D装置收集某种气体,发现 时,证明气体已集满。
(3)实验室用大理石和稀盐酸反应制取并收集一瓶干燥的二氧化碳气体,所选装置正确的连接顺序是 → → (填装置编号)。
(4)从安全、环保、节能、简便等方面考虑,实验室制取氧气的最佳方法就是利用过氧化氢在二氧化锰做催化剂的条件下分解,其主要操作步骤有:①检查装置的气密性;②组装仪器;③向漏斗中注入过氧化氢溶液;④向锥形瓶中放入二氧化锰;⑤收集气体。正确的操作顺序是 (填序号)。
a.①②③④⑤
b.①④②③⑤
c.②①④③⑤
d.②③④①⑤
(5)写出用高锰酸钾加热制取氧气的化学方程式 。
根据图1,图2回答问题:

(1)实验室用氯酸钾和二氧化锰制取氧气。应选择的发生装置是 (填字母),若用C装置收集氧气时,带火星的木条放在瓶口始终没有复燃,其原因可能是 (写出一种即可),实验完毕后,若要从剩余固体中回收二氧化锰,需用的玻璃仪器有烧杯和 。
(2)已知由一氧化碳发生装置制得的气体中,混有二氧化碳和水蒸气,现用图2中的装置净化该气体,并用净化后的一氧化碳还原氧化铁,再检验气体产物。

①B装置中应盛放的试剂是 。
②如果D、E装置顺序对调,将会导致 。