(10分)已知某粗盐样品中含有泥沙和Na2SO4、MgCl2、CaCl2等杂质。实验室提纯氯化钠的流程如下: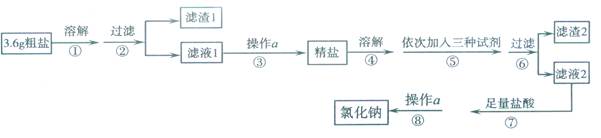
(1)第①步操作时蒸馏水的最佳使用量约为 (已知20℃时NaCl的溶解度为36g)。
增加蒸馏水的用量虽然能加快粗盐的溶解,但会引起的不良后果是 。实验时若加入的氯化钠没有达到饱和,得精盐产率 (填不变、偏大、偏小)
(2)第②步操作时,两次用到玻璃棒,其作用分别是 、 。
(3)第⑤步操作加入试剂的顺序是
| A.过量的氢氧化钠、过量的氯化钡、过量的碳酸钠 |
| B.过量的氯化钡、过量的氢氧化钠、过量的碳酸钠 |
| C.过量的碳酸钠、过量的氯化钡、过量的氢氧化钠 |
| D.过量的氯化钡、过量的碳酸钠、过量的氢氧化钠 |
(4)第③⑧步操作a的名称是 ,此步操作中,如果不使用玻璃棒,常常会使产率 (填不变、偏大、偏小)。
(5)在第⑦步操作中,向滤液中滴加足量盐酸的目的是(用化学反应方程式表示)
从H2、O2、CO2、SO2、C、N2五种物质中,按照下列要求,选择适当的物质,将其化学式填入空格中。
①有刺激性气味的气体;②能使带火星的木条复燃的气体;
③能使澄清石灰水变浑浊的无色无味气体;④焊接金属时作保护气的气体;
⑤标准状况下,密度最小的气体;⑥能够作为固体燃料的是
酒精是生产、生活中的一种重要物质,其学名叫乙醇,它的化学式为C2H5OH,请根据此化学式回答以下问题:
(1)乙醇由种元素组成
(2)乙醇的相对分子质量为
(3)碳、氢、氧元素质量比为
碳元素组成的单质有多种。请回答下列问题:
(1)北宋画家张择端用墨绘制的《清明上河图》能够保存至今,是因为。
(2)碳单质包括金刚石、石墨和C60等,它们的化学性质相似,如它们都有可燃性,试写出C60在空气中充分燃烧的化学方程式
(3)石墨在一定条件下可转变为金刚石,该变化属于(填物理或化学)变化
根据下列图示实验,写出对应的化学方程式。
(1)
(2)
(3)
用化学用语填空或写出符号表示的意义:
(1)亚铁离子;2个氢分子;3个碳酸根离子
(2)+2价的钙元素;2H2O
(3)三个氧原子构成的臭氧分子的化学式。