对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施之一。
(1)硫酸工厂的酸性废水中砷(As)元素(主要以H3AsO3形式存在)含量极高,为控制砷的排放,某工厂采用化学沉降法处理含砷废水。请回答以下问题:
①已知砷是氮的同族元素,比氮原子多2个电子层,砷在元素周期表的位置为 ____,AsH3的稳定性比NH3的稳定性 (填“强”或“弱”)。
②工业上采用硫化法(通常用硫化钠)去除废水中的砷,生成物为难溶性的三硫化二砷,该反应的离子方程式为 。
(2)电镀厂的废水中含有的CN-有剧毒,需要处理加以排放。
①已知HCN为一元弱酸,则NaCN溶液的pH 7(填“>”、“=”或“<”)。
②处理含CN -废水的方法之一是在微生物的作用下,CN -被氧气氧化成HCO3—,同时生成NH3,该反应的离子方程式为 。
(3)电渗析法处理厨房垃圾发酵液,同时得到乳酸的原理如图所示(图中“HA”表示乳酸分子,A—表示乳酸根离子)。
①阳极的电极反应式为 。
②简述浓缩室中得到浓乳酸的原理___________________________。
③电解过程中,采取一定的措施可控制阴极室的pH约为6~8,此时加入浓缩室的OH—可忽略不计。400mL10g/L的乳酸溶液通电一段时间后,浓度上升为145g/L(溶液体积变化忽略不计),阴极上产生的H2在标准状况下的体积约为____L(乳酸的摩尔质量为90g/mol)。
甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上采用如下反应合成甲醇:
CO(g)+2H2(g) CH3OH(g),现模拟并分析该反应:
CH3OH(g),现模拟并分析该反应:
(1)能够说明该反应已达到平衡的是_________:
a.恒温、恒容时,容器内的压强不再变化
b.恒温、恒容时,容器内混合气体的密度不再变化
c.一定条件下,CO、H2和CH3OH的浓度保持不变
d.一定条件下,单位时间内消耗2molH2的同时生成1 mol CH3OH
(2)右图是该反应在不同温度下CO转化率随时间的变化曲线:
①该反应的△H____0(填“>”、“<”或“=”)。
②T1和T2温度下的平衡常数:K1____K2(填“>”、“<”或“=”)。
(3)2009年,长春应用化学研究所在甲醇燃料电池技术上获得新突破,原理如图1所示。
①甲醇完全燃烧的化学方程式_______________________。
②请写出从C口通入O2发生的电极反应式___________________。
(4)用上述电池做电源,用图2装置电解饱和食盐水(C1、C2均为石墨电极)。
①该反应的离子方程式________________________。
②电解开始后在电极__________________的周围(填“C1”或“C2”)先出现红色。
某同学拟用粗氧化铜(含少量FeO及不溶于酸的杂质)制取无水氯化铜,流程如图:
(1)步骤①中氧化铜与盐酸反应的离子万程式:___________________。
(2)步骤②中加入H2O2的目的____________________________________,
沉淀II的化学式为_______________________。
(3)已知:
| 氢氧化物开始沉淀时的pH |
氢氧化物沉淀完全时的pH |
|
| Fe3+ |
1.9 |
3.2 |
| Cu2+ |
4.7 |
6.7 |
| Fe2+ |
7 |
9 |
步骤③中调节pH的最佳范围为____,调节溶液pH的试剂X可以是______________:
a.NaOH b.CuO c.Cu(OH)2 d.
(4)步骤④的操作是___________,过滤、洗涤、干燥。
为得到无水CuCl2,步骤⑤需在干燥的HCl气流中加热 ,原因是__________________________________________________________。
,原因是__________________________________________________________。
咖啡酸(如图)存在于野胡萝卜、光叶水苏、荞麦等物中。咖啡酸有止血作用,特别对内脏的止血效果较好。
(1)咖啡酸的化学式_____________。咖啡酸中含氧官能团的名称________________。
(2)咖啡酸发生加聚反应所得产物的结构简式______________。
(3)下列关于咖啡酸的说法正确的是_____:
| A.1mol咖啡酸最多只能与1molBr2反应 |
| B.咖啡酸和乙醇能发生酯化反应 |
| C.咖啡酸遇氯化铁溶液能发生显色反应 |
| D.只用KMnO4溶液即可检验咖啡酸分子中含有碳碳双键 |
(4)咖啡酸与足量NaOH溶液反应的化学方程式:__________________。
(5)A是咖啡酸的同分异构体,其苯环上只有1个取代基,1molA能与2molNaHCO3反应,A的结构简式_________________________。
砷(As)在地壳中含量不大,但砷的化合物却是丰富多彩。
(1)基态砷原子的电子排布式为;砷与溴的第一电离能较大的是。
(2)AsH3是无色稍有大蒜味气体。AsH3的沸点高于PH3,其主要原因是。
(3)Na3AsO4可作杀虫剂。AsO43-的空间构型为,与其互为等电子体的一种分子为。
(4)某砷的氧化物俗称“砒霜”,其分子结构如图所示。该化合物的分子式为,As原子采取杂化。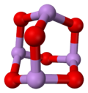
(5)GaAs等是人工合成的新型半导体材料,其晶体结构与金刚石相似。GaAs晶体中,每个As与
个Ga相连,As与Ga之间存在的化学键有(填字母)。
| A.离子键 | B.σ键 | C.π键 | D.氢键 |
E.配位键 F.金属键
G.极性键
(18分)钛(Ti)被称为继铁、铝之后的第三金属,江西省攀枝花和西昌地区的钒钛磁铁矿储量十分丰富。如下图所示,将钛厂、氯碱厂和甲醇厂组成产业链可以大大提高资源利用率,减少环境污染。请填写下列空白: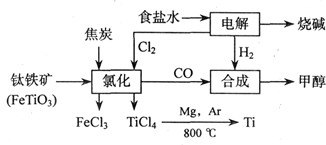
⑴电解食盐水时,总反应的离子方程式_____________________________________。
⑵写出钛铁矿经氯化法得到四氯化钛的化学方程式:___________________。
⑶已知:①Mg(s) +Cl2(g)=MgCl2(s);ΔH=-641 kJ·mol-1
②Ti(s)+2Cl2(g)=TiCl4(s);ΔH=-770 kJ·mol-1
则2Mg(s)+TiCl4(g)=2MgCl2(s)+Ti(s);ΔH____________________
反应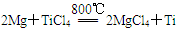 在Ar气氛中进行的理由是____________________。
在Ar气氛中进行的理由是____________________。
⑷在上述产业链中,合成192 t甲醇理论上需额外补充H2__________t(不考虑生产过程中物质的任何损失)。
⑸以甲醇、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。该电池中负极上的电极反应式是____________________________________________。
(6)已知2A2(g)+B2(g)  2C3(g);△H="-a" kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2mol A2和1mol B2,在500℃时充分反应达平衡后C3的浓度为w mol/L,放出热量b kJ。
2C3(g);△H="-a" kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2mol A2和1mol B2,在500℃时充分反应达平衡后C3的浓度为w mol/L,放出热量b kJ。
①比较a____________b(填>、=、<)
②此反应的平衡常数表达式为________________________;若将反应温度升高到700℃,反应的平衡常数将_____________(增大、减小或不变)
③能说明该反应已经达到平衡状态的是______。
| A.v(C3)=2v(B2) | B.容器内压强保持不变 |
| C.v逆(A2)=2v正(B2) | D.容器内的密度保持不变 |