课外化学兴趣小组的同学利用某化工厂的废碱液(主要成分为Na2CO3、还含有少量NaCl)和石灰乳(氢氧化钙的悬浊液)为原料制备烧碱,并对所得的烧碱粗产品的成分进行分析和测定。
【查阅资料】①碱石灰是CaO与NaOH的固体混合物,可吸收二氧化碳和水;
②CO2+Ba(OH)2 ═ BaCO3↓+H2O。
【粗产品制备】
(1)将废碱液加热蒸发浓缩,形成较浓的溶液,冷却后与石灰乳混合,发生反应的化学方程式为 。
(2)将反应后的混合物过滤,得到的滤液进行蒸发结晶,制得NaOH粗产品。
【粗产品成分分析】
(1)取适量粗产品溶于水得澄清溶液,加入Ba(NO3)2溶液出现白色沉淀,由此该粗产品中一定不含有 ,理由是
(2)该小组同学通过对粗产品成分的实验分析,确定该粗产品中含有三种物质。
【含量测定】Na2CO3含量的测定:
该兴趣小组的同学设计了下图所示的实验装置。取20.0g粗产品,进行实验。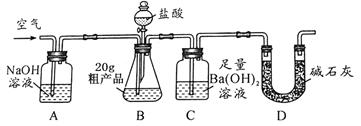
(1)实验过程中需持续缓缓通入空气,其目的是 。
(2)下列各项措施中,不影响测定准确度的是______(填标号)。
a.在加入盐酸之前,应排净装置内的CO2气体
b.滴加盐酸不宜过快
c.在A-B之间增添盛有浓硫酸的洗气装置
d.取消上图中D装置
(3)实验中准确称取20.0g粗产品,进行测定,测得BaCO3质量为1.97g。则粗产品中碳酸钠的质量分数为 。
(4)有人认为不必测定C中生成的BaCO3质量,只要测定装置C在吸收CO2前后的质量差,一样可以确定碳酸钙的质量分数.实验证明按此方法测定的结果明显偏高,原因是 。
甲、乙两同学帮助老师整理实验室时,发现有一瓶试剂标签残缺,只剩下“Na”和“10%”字样(如图)。已知它是无色液体,是初中化学常用的试剂。甲、两同学决定对其成分进行探究:
【提出问题】这瓶试剂可能是什么溶液呢?
【交流讨论】甲根据受损标签的情况判断,这瓶试剂不可能是。
A.酸 B.碱 C.盐
【查阅资料】Ⅰ.初中化学常见的含钠化合物有NaCl、NaOH、Na2CO3、NaHCO3。
Ⅱ.测定室温(20℃)时,四种物质的溶解度的数据如下:
| 物质 |
NaCl |
NaOH |
Na2CO3 |
NaHCO3 |
| 溶解度g |
36 |
109 |
215 |
9.6 |
【得出结论】乙根据试剂瓶标注的溶质质量分数10%和上表中的溶解度的数据判断,这瓶试剂不可能是。
【设计实验并继续探究】
(1)甲取该溶液少量于试管中,加入紫色石蕊,溶液变蓝,这瓶试剂不可能是。
(2)乙为了确定该溶液是哪种溶液,又进行了如下实验:
| 操作步骤 |
实验现象 |
结论及化学方程式 |
| 取样于试管中,滴加 |
产生大量的气泡 |
该溶液是,反应的化学方程式 |
【拓展与应用】
甲确定该溶液,选择了与乙不同的试剂,甲选择的试剂是(要求类别不同)。
【反思与评价】老师指出该结论不严密,其理由是。
在学习盐的性质时,某组同学将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液.同学们对该实验进行了一系列的研究.
探究一 M溶液中的溶质是什么?
(1)【提出猜想】该组同学认为M溶液的溶质有两种可能:①是,②是CaCl2.
【收集资料】CaCl2水溶液呈中性.
(2)【设计实验】同学们设计了如下方案并进行实验:
| 实验操作 |
实验现象 |
实验结论 |
| 取少量M溶液于试管中,向其中滴加 |
猜想①正确,碳酸钠与其反应的化学方程式为 |
探究二 过滤后澄清滤液中会有哪些溶质?
【提出猜想】猜想一:NaOH和Na2CO3;猜想二:_____;猜想三:NaOH
(3)【实验验证】同学们针对“猜想一”进行了如下实验:
| 实验步骤 |
实验现象 |
实验结论 |
| 取样于试管中,滴入几滴稀盐酸 |
没有气体产生 |
“猜想一”不成立 |
他们的实验结论是否正确?,理由是.
(4)【继续探究】设计实验方案确定滤液中溶质的组成.
| 实验操作 |
实验现象 |
实验结论 |
| 分别取少量滤液于A、B两支试管中,A中加入CaCI2溶液,B中加入溶液 |
若A中产生白色沉淀,B中没有沉淀 |
“猜想一”成立 |
| “猜想二”成立 |
||
| “猜想三”成立 |
研究氢气、一氧化碳和二氧化碳具有重要意义.
(1)在汽车“催化转化器”内发生反应的化学方程式是:2NO+2CO N2+2CO2.某化学探究小组的同学为探究温度、催化剂的比表面积对化学反应速率的影响,设计了下列三组实验.
N2+2CO2.某化学探究小组的同学为探究温度、催化剂的比表面积对化学反应速率的影响,设计了下列三组实验.
| 实验编号 |
T/℃ |
NO初始浓度/g•L﹣1 |
CO初始浓度/g•L﹣1 |
催化剂的比表面积/m2•g﹣1 |
| Ⅰ |
280 |
0.036 |
0.162 |
82 |
| Ⅱ |
280 |
0.036 |
0.162 |
124 |
| Ⅲ |
350 |
0.036 |
0.162 |
124 |
(1)分析上表中实验数据,回答下列问题:探究温度对化学反应速率影响的实验是(填写实验编号);研究催化剂的表面积对化学反应速率影响的实验是(填写实验编号).
(2)在300℃、70MPa下,使用催化剂可由氢气和二氧化碳合成乙醇,同时生成水,写出反应的化学方程式.
(3)燃料燃烧时产生的热量不同.已知在某温度下各种燃料燃烧时产生的热量见下表:
| 燃料 |
质量/g |
产物 |
产生的热量/KJ |
| 氢气 |
2 |
水蒸气 |
241.8 |
| 甲烷 |
16 |
二氧化碳气体和水蒸气 |
890.3 |
| 乙醇 |
46 |
二氧化碳气体和水蒸气 |
1367 |
分析表中数据,燃烧单位质量的上述燃料产生的热量由多到少的顺序是(用化学式表示).
小光同学学习化学后知道,镁在氧气中燃烧会生成白色的氧化镁固体。但他在空气中点燃镁条时,却发现在生成的白色固体中还夹杂着少量的淡黄色固体。
【提出问题】为什么会生成淡黄色固体?
【查阅资料】小光查阅资料,记录了下列几种物质的颜色:
| 物质 |
MgO |
MgCl2 |
Mg3N2 |
Mg(NO3)2 |
MgCO3 |
Mg(OH)2 |
| 颜色 |
白色 |
白色 |
淡黄色 |
白色 |
白色 |
白色 |
其他同学认为不必查阅氯化镁的是_________________________;
【提出猜想】分析资料:小光认为淡黄色固体可能是由镁与空气中的____反应生成的;
【实验探究】小光设计实验证实了自己的猜想,他的方案可能是__________________;
【实验结论】根据小光的实验结果,写出镁条在空气中燃烧时发生的两个反应的化学方程_______________________、________________________;
【反思与评价】通过上述实验,你对燃烧的认识______________________________。
某研究性学习小组在实验中发现:不仅碱溶液可以使酚酞试液变红,Na2CO3溶液也能使酚酞试液变红。碱溶液可以使酚酞试液变红,是因为碱在水中解离出了OH-,那么Na2CO3溶液中究竟是哪种粒子可以使酚酞试液变红呢?他们设计了如图三个实验,请你和他们一起探究并完成下列问题: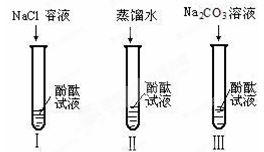
(1)实验Ⅰ是为了
(2)实验Ⅱ加入蒸馏水的目的是探究水分子是否能使酚酞试液变红,小组内有同学认为实验Ⅱ没必要做,你认为他们的理由是;
(3)实验Ⅲ滴入Na2CO3溶液,振荡,酚酞试液变红,向变红后的溶液中再逐滴滴入过量的CaCl2溶液,红色逐渐消失,同时还观察到生成,反应的化学方程式______________________________。由实验Ⅰ、Ⅱ、Ⅲ得出结论:CO32-可以使酚酞试液变红;
(4)小组同学在与老师交流上述结论时,老师说:“其实Na2CO3溶液能使酚酞试液变红也是由于溶液中存在OH-”。你认为Na2CO3溶液中存在OH-的原因是________________________。