现欲探究一固体混合物A的成分,已知其中可能含有NH4Cl、Cu(OH)2、BaSO4、CaO、NH4 NO3五种物质中的两种或多种。按下图所示进行实验,出现的现象如图中所述(设过程中所有发生的反应均恰好完全反应)

试根据实验过程和发生的现象判断:
(1)常温下,气体B的水溶液显_________(填“酸性”“中性”“碱性”之一)。
(2)滤渣D的化学式是_________________。
(3)固体混合物A中,一定存在的物质是(写化学式)___________________________。
(4)滤液C中,一定大量存在的金属离子是(写离子符号)________________________。
(5)写出过程③中可能发生的一个化学方程式: 。
(6)固体混合物A中还不能确定存在的物质是(写化学式) ,得出此结论的理由是 。
实验室有四瓶失去标签的溶液,现标为
、
、
、
,分别是碳酸钠溶液、氯化钡溶液、硫酸钠溶液和稀盐酸中的一种.
[提出问题]如何区分出四种溶液?
[进行实验]甲同学实验如图所示:由此甲同学认为
一定不是.
[表达与交流]甲同学向实验后的溶液中滴加酚酞溶液,酚酞溶液由无色变为红色,则甲同学的结论:
是氯化钡溶液.乙同学不同意甲同学的结论,乙同学的理由是.于是乙同学另取少量
于试管中,向其中滴加一种试剂是溶液,观察到的明显现象是.由此证明了甲同学的结论是错误的.同时确定了
.乙同学继续实验如图所示:
[收集证据]观察到
中产生气泡,
中产生白色沉淀.
[解释与结论]写出
中发生反应的化学方程式.
乙同学最终通过实验区分出了四种溶液.
[反思与评价]请指出甲同学区分上述四种溶液时,在实验方法上的一点不足之处.
学完酸碱盐知识后,小美对妈妈焙制糕点用的小苏打很感兴趣,她把小苏打带到实验室与小刚一起进行探究.
(1)小美取少量小苏打溶于水,滴加酚酞试液后,溶液变红,说明小苏打的水溶液显性;
(2)小刚在烧杯内放入少量小苏打,向其中滴加稀盐酸,立即有产生,说明小苏打能与酸反应.在医疗上可以用小苏打治疗;
(3)小美想:糕点非常松软,是不是小苏打受热分解产生了
气体呢?于是她如图装置对小苏打进行加热,一段时间后,导管口的确有气泡冒出,澄清石灰水变浑浊,同时试管口有水珠生成.当导管口不再有气泡产生时,试管内仍有白色固体,她猜测剩余固体可能是:①
;②
;③
.小刚认为猜想一定不正确,理由是.小刚从试管内取少量白色固体溶于水,滴加酚酞,溶液变红,他判断该固体为NaOH,小美认为他的实验设计不合理,因为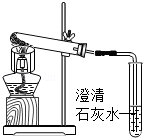
(4)小美和小刚继续探究固体成分,设计了如下实验:
| 操作步骤 |
实验现象 |
结论 |
| 取少量白色固体于试管中,加水溶解,向其中滴加溶液 |
产生白色沉淀 |
试管内剩余的固体为
|
通过实验证明小苏打受热会分解,反应的化学方程式为:.通过本次探究学习,小美对小苏打的性质有了全面的认识,她给妈妈提出保存小苏打的建议有:(答出一点即可).
在中学所学的化学反应中,有很多反应没有明显现象.某探究小组想通过实验来证明某些无现象的反应确实发生了,他们做了以下探究过程.
Ⅰ,对
溶液与盐酸反应的探究
甲同学按如图所示的装置验证
与盐酸发生反应,结果甲同学没有看到预期的实验现象,原因是,如果要想证明盐酸与
发生反应,则实验应改为现象.
Ⅱ,对
与
溶液反应的探究
【查阅资料】通常状况下,1体积水能溶解1体积二氧化碳.
【设计实验】甲同学设计了三个实验进行验证,请你帮他完成下列实验报告.
| 实验操作 |
实验现象 |
实验结论及解释 |
|
| ① |
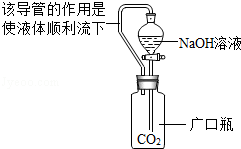 |
氢氧化钠溶液可以与
反应. 反应的化学方程式为: |
|
| ② |
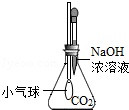 |
氢氧化钠溶液可以与
反应. |
|
| ③ |
 洗气瓶中的溶液均为氢氧化钠溶液或澄清石灰水(均为200mL) |
,
均无明显变化 |
氢氧化钠溶液可以
反应. 中盛放的溶液是. |
【反思交流】
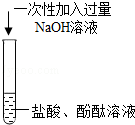
(1)实验①由于甲同学选用的仪器不当,导致未能观察到明显现象,乙同学将甲同学的广口瓶替换成看到了现象,证明
可以与
溶液反应.丙同学认为乙同学的改进实验仍然存在缺陷,应增加一个对比实验,证明
确实可以与
溶液发生反应,该对比实验所用的试剂是.
(2)请判断③中
(填">"、"<"或"="),理由是.
【实验结论】通过实验探究,证明了氢氧化钠溶液可以与二氧化碳反应.
以下是中学常见的实验装置图(图1)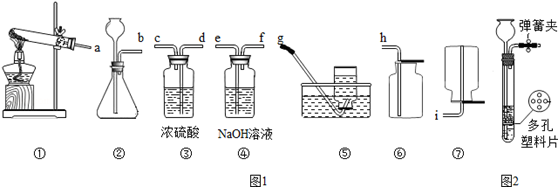
(1)实验室用锌粒和稀硫酸反应制取氢气,要制备并收集干燥的氢气,请将所选装置接口按从左到右顺序连接为.
(2)实验室制取氧气有多种方法.
a,用
制氧气应选用作为发生装置(填装置序号).检验该装置气密性的方法是.
b.如用
溶液制氧气,除
溶液外还需要加入的试剂是(填名称).如图2是实验室制备气体的一种装置图.该装置的特点是:打开弹簧夹,块状固体和液体接触,反应发生;关闭弹簧夹后,产生的气体将液面压回,使固体和液体分开,反应停止.用
溶液制氧气时,(填"可以"或"不可以")采用此装置.
c.实验室还用
来制备氧气,该反应的化学方程式为.将
与
的混合物ag加热一段时间,得到bg固体,将得到的固体溶于水,过滤、洗涤、干燥后,又得到cg固体,则
分解率为.(用含a,b.c的式子表示)(提示:
的分解率是指已分解
质量与原加入
质量之比.)
为了探究酸碱性对唾液淀粉酶催化作用的影响,小明利用蒸馏水、1%淀粉溶液、稀释的唾液、稀盐酸、氢氧化钠溶液、碘液等材料进行实验.请你完成相应的实验设计和问题分析.
【实验设计】
| 实验操作 |
设计要求 |
| 步骤一:取3支洁净的试管标为 、 、 ,在各试管中分别加入1%淀粉溶液2毫升;向 试管加入l毫升稀盐酸和l毫升唾液;向 试管加入1毫升氢氧化钠溶液和1毫升唾液;向 试管加入 | 设置对照实验 |
| 步骤二: | 控制实验条件 |
| 步骤三:10分钟后,往3支试管中分别滴入1滴碘液,观察颜色变化. |
获取实验证据 |
【问题与分析】
正确操作后,小明观察到
试管呈蓝色,而
试管没有出现预期的蓝色.他想:为什么
试管不呈蓝色?他推测可能是氢氧化钠溶液变质或者
试管中液体碱性太弱.在老师的帮助下,他证实了氢氧化钠溶液没有变质,且
试管中液体碱性强度足以抑制酶的催化作用.请你对
试管没有出现蓝色作出一种合理的猜测:.