工业上生产硫酸时,利用催化氧化反应将SO2转化为SO3是一个关键步骤。压强及温度对SO2转化率的影响如下表(原料气各成分的体积分数为:SO2 7% O2 11% N2 82%);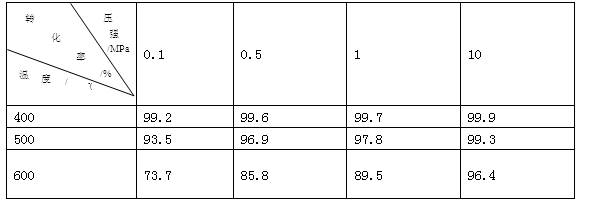
(1)已知SO2的氧化是放热反应,如何利用表中数据推断此结论? ;
(2)在大400~500℃时,SO2的催化氧化采用常压而不是高压,主要原因是: ;
(3)选择适宜的催化剂,是否可以提高SO2的转化率? (填“是”或“否”),是否可以增大该反应所放出的热量? (填“是”或“否”);
(4)为提高SO3吸收率,实际生产中用 吸收SO3;
(5)已知:2SO2(g)+O2(g)=2SO3(g);△H=-196.9kJ·mol-1,计算每生产1万吨98%硫酸所需要的SO3质量和由SO2生产这些SO3所放出的热量。
已知物质M由 属于同一周期的X.Y两种短周期元素组成,X原子的最外层电子数是最内层电子数的一半,Y元素最高正价与它的负价代数和为6.M与其他物质的转化关系如下(部分产物已略去):
属于同一周期的X.Y两种短周期元素组成,X原子的最外层电子数是最内层电子数的一半,Y元素最高正价与它的负价代数和为6.M与其他物质的转化关系如下(部分产物已略去):
(1)已知元素Z与Y是最外层电子数相同的短周期元素,那么Z与Y分别与氢形成的氢化物中沸点较高的是(填化学式);
(2)若A是一种常见的酸性氧化物,且可用于制造玻璃,则E溶液与F溶液反应的离子方程式是:;
(3)若A是与X、Y同周期元素的一种常见金属单质,且A与B溶液能够反应,则其化学方程式是:;
(4)若A是一种常见的化肥,相对分子质量为79,且E与F生成G时有白烟产生,则A的化学式;
(5)若A是一种溶液,只可能含有H+.NH4+、 Mg2+、Fe3+、Al3+、CO32—、SO42-中的某些离子,当向该溶液中加入B溶液时发现生成沉淀的物质的量随B溶液的体积变化如图所示,由此可知,该溶液中肯定含有的离子符号(微粒次序按摩尔质量从小到大)及物质的量浓度之比为
Mg2+、Fe3+、Al3+、CO32—、SO42-中的某些离子,当向该溶液中加入B溶液时发现生成沉淀的物质的量随B溶液的体积变化如图所示,由此可知,该溶液中肯定含有的离子符号(微粒次序按摩尔质量从小到大)及物质的量浓度之比为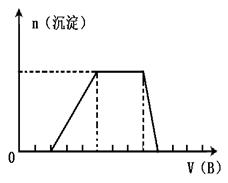 .
.
硬质玻璃管是化学实验中经常使用的一种仪器,分析下列实验(固定装置略)并回答:进行微量实验:如图所示,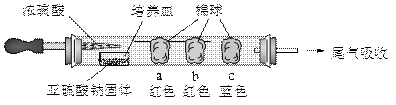
将浓硫酸滴入装有Na2SO3固体的培养皿一段时间后,a.b.c三个棉球变化如下表.
请完成下列表格:
| 棉球 |
棉球上滴加试剂 |
实验现象 |
解释或结论 |
| a |
_______________ |
棉球变白,微热后又恢复红色 |
解释:__________________ 结论:该气体具有漂白性. |
| b |
含酚酞的NaOH溶液 |
棉球变为白色 |
离子方程式: _________________________ |
| c |
淀粉和I2 的混合溶液 |
棉球变为白色 |
结论:该气体具有________. |
(1)纳米材料二氧化钛(TiO2)可做优良的催化剂.
据报道:“生态马路”是在铺设时加入一定量的TiO2,TiO2受太阳光照射后,产生的电子被空气或水中的氧获得,生成H2O2,其过程大致如下: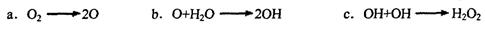
①b中破坏的是__________ (填“极性共价键”或“非极性共价键”).
②H2O2能清除路面空气中的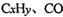 等,其主要是利用了H2O2的作用是_____________________________________________ (填“氧化性”或“还原性”).
等,其主要是利用了H2O2的作用是_____________________________________________ (填“氧化性”或“还原性”).
(2)某固体混合物中含有Na+、K+、Mg2+和Cl-、Br-五种微粒.
I.欲将钠、钾、镁三元素大致分离开来,并将氯、溴两元素大致分离开来,有以下方法和操作步骤可供选择(其中有的步骤可选两次).
①溶于水制成稀溶液;②溶于水制成浓溶液;③通入足量CO2;④加入足量 氯水;
氯水;
⑤通入足量氨气;⑥过滤;⑦用四氯化碳萃取.
选取最合理的方法和步骤:(按顺序先后填写编号).
II.分离后剩余的水溶液中所含的主要物质是.
III.在上述分离过程中分离出一种化合物晶体.欲得到干燥的该化合物固体,有两种方法可供选择:①.加热蒸发掉水分;②.将过滤得到的固体物质自然风干.正确的方法应选择______________________________________________.
实验室制氢氧化铁胶体将滴入 中,继续加热至液体呈红褐色时,用一束可见光照射可观察到现象,这一现象叫丁达尔现象,向胶体中逐滴滴入稀硫酸至过量可观察到现象,产生此现象的原因是。
智利硝石矿层中含有碘酸钠,可用亚硫酸氢钠与其反应来制备单质碘,其化学方程式为:
_____NaIO3+_______NaHSO3——_______NaHSO4+_____ Na2SO4+___I2+____H2O
(1)配平上述反应方程式并用双线桥标出电子转移的方向和数目
(2)反应中 元素被氧化,是氧化剂
(3)反应中,所得氧化产物和还原产物的质量之比为 。