CO是一种无色、无味且不溶于水的有毒气体,其制法有:
(1)实验室可用甲酸和浓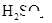 共热制取CO.
共热制取CO.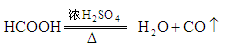
a.甲酸和浓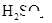 应怎样混合?浓
应怎样混合?浓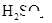 起什么作用
起什么作用
b.请据实验原理选择所需主要玻璃仪器(导管除外)
c.怎样收集CO气体
(2)实验室还可用草酸晶体与浓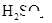 共热制取CO.H2C2O4
共热制取CO.H2C2O4 CO2↑+CO↑+H2O
CO2↑+CO↑+H2O
请问:怎样才能得到不含 的CO气体? _________.
的CO气体? _________.
(3)工业上用焦炭和水在高温下发生反应制取CO,其化学方程式为:________________.在此条件下,C和 的还原性谁强? _________.
的还原性谁强? _________.
下表是某食品包装袋上的说明:
| 品名 |
浓缩菠萝汁 |
| 配料 |
水、浓缩菠萝汁、蔗糖、柠檬酸、黄原胶、甜蜜素、维生素C、菠萝香精、柠檬黄、日落黄、山梨酸钾等 |
| 果汁含量 |
≥80% |
| 生产日期 |
标于包装袋封口上 |
从表中的配料中分别选出一种物质填在相应的横线上。其中属于着色剂的有__________,属于调味剂的有__________,属于防腐剂的有__________,属于营养强化剂的有__________。
氯普鲁卡因盐酸盐是一种局部麻醉剂,麻醉作用较快、较强,毒性较低,其合成路线如下: 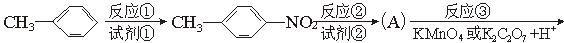
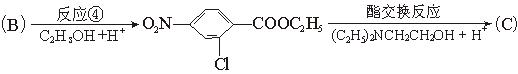
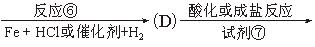
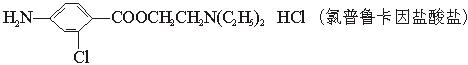
请把相应反应名称填入下表中,供选择的反应名称如下:
氯化、还原、硝化、磺化、氯代、酸化、碱化、成盐、酯化、酯交换、水解
| 反应编号 |
① |
② |
③ |
④ |
⑥ |
| 反应名称 |
大家都知道 6月1日 是国际儿童节,但或许绝大多数人并不了解这天同时也是“世界牛奶日”。20世纪50年代,法国的促进牛奶消费协会提出了庆祝“牛奶日”的设想,并做出了每年5月第三周的周二为“国际牛奶日”的决定,2000年经联合国粮农组织(FAO)的提议,兼顾到某些国家已经确定的日期,并征得了世界700多位乳业界人士的意见,把每年的 6月1日 确定为“世界牛奶日”。人体中的钙元素主要存在于骨骼和牙齿中,以羟基磷酸钙晶体〔Ca 10 (PO 4 ) 6 (OH) 2 〕形式存在。牛奶含钙丰富又易吸收,且牛奶中钙和磷比例合适,是健骨的理想食品。下图是某乳业公司纯牛奶包装标签的部分文字。请仔细阅读后回答下列问题:
| 纯牛奶 配料:鲜牛奶 保质期:8个月 净含量:250 mL/盒 营养成分(每100 mL) 钙≥ 0.11 g 脂肪≥ 3.3 g 蛋白质≥ 2.9 g |
(1)羟基磷酸钙中钙元素的质量分数为__________(保留到 0. 1 g )
(2)包装标签上脂肪≥ 3. 3 g ,是指100 mL牛奶中含脂肪至少 3. 3 g 。那么一盒牛奶中含钙至少__________ g。(保留到 0. 01 g )
味精是烹制菜肴时常用的调味品,其主要成分是谷氨酸钠(化学式为C 5 H 8 NO 4 Na)。谷氨酸钠有鲜味,易溶于水。某品牌味精包装上标注:“谷氨酸钠含量≥80%,NaCl含量<20%”。
某学校化学科研小组对此味精中NaCl的含量进行测定。
Ⅰ.查阅资料:谷氨酸钠的存在不影响NaCl含量的测定。
Ⅱ.设计实验方案:
(1)实验原理:通过味精与硝酸银反应生成氯化银的质量计算该味精中NaCl的质量分数。
(2)实验试剂:水、AgNO 3 溶液等
(3)实验过程: 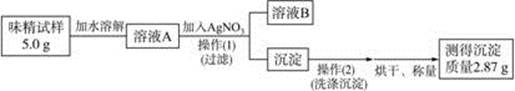
①操作(Ⅰ)所需要的玻璃仪器有____________________。
②通过计算判断该味精中NaCl的质量分数是__________,判断该味精中NaCl __________(填“符合”或“不符合”)其包装上标注的标准。
③若溶液A的体积为50 mL,则其中NaCl的物质的量浓度为____________________。
(12分)已知: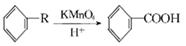 ,从A出发发生图示中的一系列反应,其中B和C按1:2反应生成Z。F和E按1:2反应生成W,W和Z互为同分异构体。
,从A出发发生图示中的一系列反应,其中B和C按1:2反应生成Z。F和E按1:2反应生成W,W和Z互为同分异构体。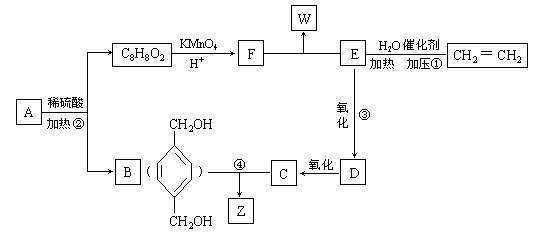
回答下列问题:
(1)写出反应类型:①_____________________,②______________________________。
(2)写出下列反应的化学方程式:
③_____________________________________________________;
④_____________________________________________________。
(3)与B互为同分异构体,属于酚类且苯环上只有两个互为对位取代基的化合物有4种,其结构简式为_______________,_________________,_______________,______________。
(4)A的结构简式可能为_______________________________________(只写一种即可)。