为了维护南海权益,我国去年宣布成立了三沙市。这是维护国家主权的象征,同时也是因为海洋资源十分丰富,有广泛的利用价值。其中通过海水晾晒即可得粗盐,粗盐除NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质。以下是制备精盐的实验方案,各步操作流程如下:

(1)根据以上信息,请写出海水中所含的主要阴离子的符号 。
(2)在上述流程中第③步加过量NaOH的目的是除去海水中的 (填离子符号,下同),第④步加过量Na2CO3的目的是除去海水中的 。第⑥步其实显示的是加适量盐酸,其目的是除去多余的 。
(3)请写出第②步所发生反应的化学方程式 。
(4)在第③步操作中,选择的除杂试剂不能用KOH代替NaOH,理由是 。
氯化钾样品中含有少碳酸钾、硫酸钾和不溶于水的杂质。为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,再将过滤液按下图所示步骤进行操作。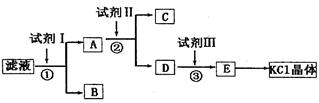
回答下列问题:
(1)起始时滤液的pH_____7(填“大于”“小于”或“等于”),其原因是__________________(用离子方程式表示)。
(2)试剂I的化学式为______,①中发生反应的离子方程式为_____________________。
(3)试剂II的化学式为_____,②中加入试剂II的目的是_________________________。
(4)试剂III的名称是_____,③中发生反应的离子方程式为________________________。
某化学兴趣小组用如下图1所示装置进行探究实验,以验证产物中有乙烯生成且乙烯具有不饱和性。当温度迅速上升后,可观察到试管中溴水褪色,烧瓶中浓H2SO4与乙醇的混合液体变为棕黑色。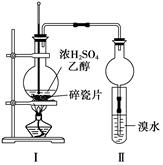
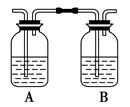
图1图2
(1)写出该实验中生成乙烯的化学方程式。
(2)甲同学认为:考虑到该混合液体反应的复杂性,溴水褪色的现象不能证明反应中有乙烯生成且乙烯具有不饱和性,其理由正确的是。
a.乙烯与溴水易发生取代反应
b.使溴水褪色的反应,未必是加成反应
c.使溴水褪色的物质,未必是乙烯
(3)乙同学经过细致观察后试管中另一现象后并借用pH试纸测定,证明反应中有乙烯生成,请简述
。
(4)丙同学对上述实验装置进行了改进,在Ⅰ和Ⅱ之间增加上图2装置以除去乙醇蒸气和SO2,则A中的试剂是,B中的试剂为。
(5)处理上述实验后烧瓶中废液的正确方法是。
a.冷却后倒入下水道中 b.冷却后倒入空废液缸中 c.冷却后加水稀释,倒入废液缸中,加废碱中和
(15分) (1)某兴趣小组欲准确配制一定物质的量浓度的NaOH溶液:快速准确称取8.0 g 纯净的NaOH固体,配制成100 mL溶液,该NaOH溶液的物质的量浓度为。所需的仪器除托盘天平、钥匙、小烧杯、玻璃棒外还缺少。
(2)有机物X由C、H、O三种元素组成的,为确定其结构进行如下实验:
a.6.0 g X在一定条件下完全分解,生成3.36 L(标准状况下)一氧化碳和1.8 g水;
b.中和2.4 g 有机物X需消耗上述NaOH溶液20.00 mL;
c.0.1 mol有机物X完全转化为酯,需要乙醇9.2 g,0.1 mol X能与足量钠反应放出3.36 L(标准状况下)氢气。则:
①X的相对分子质量为。
②X的分子式为。
③写出X的结构简式:。
④写X与足量乙醇发生酯化反应的方程式。
(12分)为回收和利用废旧塑料减轻“白色污染”,某兴趣小组进行如下探究:
| 实验课题 |
探究废旧塑料热分解的主要产物为多种烃的混合物 |
| 查阅资料 |
①CuO能将烃氧化成CO2和H2O; ②甲苯可被酸性KMnO4溶液氧化为苯甲酸,苯甲酸能溶于苯。 |
| 实验设计 |
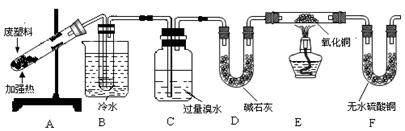  |
| 实验记录 |
按上图连接装置,隔绝空气强热装置A中的试管(忽略装置内空气的影响),一段时间后,可观察到如下现象: ①B装置试管中有液态物质生成; ②C中溴水的颜色变浅; ③E中黑色氧化铜变红; ④F中无水硫酸铜变蓝。 |
试根据上表回答下列问题:
(1)写出一定条件下制备聚丙烯化学方程式。
(2)经分析得知装置B试管中的液态产物是甲苯和苯的混合物。设计实验除去其中含有的甲苯。
(3)实验中装置C的作用是。
(4)若没有装置D,对实验结论产生的影响是。
(5)有同学认为“E中黑色氧化铜变红,F中无水硫酸铜变蓝”是废旧聚丙烯塑料热分解产物中含氢气导致的。请你在F装置后增加一个实验装置,以确认使CuO变红是气态烃,而不是氢气,将增加的装置图(要注明其中盛放的试剂名称)画在虚线框内。
(4分)下列有关实验操作或判断不正确的是 _____________(填序号,多选扣分)。
| A.配制一定物质的量浓度溶液,定容时俯视刻度线会导致所配溶液浓度偏大 |
| B.少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液冲洗 |
| C.配制稀硫酸时,可先在烧杯中加入一定体积的蒸馏水,再边缓慢加入浓硫酸边搅拌 |
| D.100 mL容量瓶可用于配制95 mL 0.1 mol/L NaCl溶液 |
E.在天平左右两盘中各放一张白纸后,即可将NaOH固体放在白纸上称量
F.观察钾元素焰色反应的操作是:先将铂丝放在稀盐酸中洗涤,然后蘸取固体氯化钾,置于酒精灯的火焰上进行灼烧,透过蓝色钴玻璃进行观察。
G.苯、CCl4、酒精可用来萃取溴水中的溴。