【2015新课标Ⅱ卷理综化学】(15 分)二氧化氯(ClO2,黄绿色易溶于水的气体)是高效、低毒的消毒剂,回答下列问題:(1)工业上可用KC1O3与Na2SO3在H2SO4存在下制得ClO2,该反应氧化剂与还原剂物质的量之比为 。
(2)实验室用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料,通过以下过程制备ClO2:

①电解时发生反应的化学方程式为 。
②溶液X中大量存在的阴离子有__________。
③除去ClO2中的NH3可选用的试剂是 (填标号)。
a.水 b.碱石灰 c.浓硫酸 d.饱和食盐水
(3)用下图装置可以测定混合气中ClO2的含量:

Ⅰ.在锥形瓶中加入足量的碘化钾,用50 mL水溶解后,再加入 3 mL稀硫酸:
Ⅱ.在玻璃液封装置中加入水,使液面没过玻璃液封管的管口;
Ⅲ.将一定量的混合气体通入锥形瓶中吸收;
Ⅳ.将玻璃液封装置中的水倒入锥形瓶中:
Ⅴ.用0.1000 mol·L-1硫代硫酸钠标准溶液滴定锥形瓶中的溶液
(I2+2S2O32-=2I-+S4O62-),指示剂显示终点时共用去20.00 mL硫
代硫酸钠溶液。在此过程中:
①锥形瓶内ClO2与碘化钾反应的离子方程式为 。
②玻璃液封装置的作用是 。
③V中加入的指示剂通常为 ,滴定至终点的现象是 。
④测得混合气中ClO2的质量为 g。
(4)用ClO2处理过的饮用水会含有一定最的亚氯酸盐。若要除去超标的亚氯酸盐,下列物质最适宜的是_______(填标号)。
a.明矾 b.碘化钾 c.盐酸 d.硫酸亚铁
为除去粗盐中的Ca2+、Mg2+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量)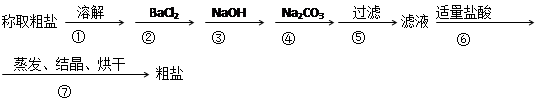
(1)判断BaCl2已过量的方法是
。
(2)第④步中,写出相应的化学方程式(设粗盐溶液中Ca2+的主要存在形式为CaCl2)
。
(3)若先用盐酸调pH再过滤,将对实验结果产生影响,其原因是
。
(4)为检验精盐纯度,需配制250 mL 0.2 mol/L NaCl(精盐)溶液,题图是该同学转移溶液的示意图,图中的错误是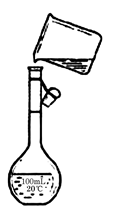
。
(12分)在呼吸面具和潜水艇中可用过氧化钠作为供氧剂。某化学探究学习小组选用适当的化学试剂和实验用品,用下图中实验装置,A是制取CO2的装置,D中装有过氧化钠,进行实验来证明过氧化钠可作供氧剂。
(1)填写表中空格:
| 仪器 |
加入试剂 |
加入该试剂的目的 |
| B |
饱和NaHCO3溶液 |
|
| C |
||
| E |
饱和NaOH溶液 |
(2)若无C装置,可能发生的干扰反应的化学方程式为。
(3)试管F中收集满气体并从水中取出后,下一步实验操作是。
(12分)某化学探究学习小组同学在实验室中配制100mL 3.6 mol·L-1的稀硫酸。
(1)若采用18 mol·L-1的浓硫酸配制溶液,需要浓硫酸的体积为。
(2)下列实验步骤是配制溶液所必需的步骤,请使用各步骤的编号按照实验操作时的顺序进行排序(只填各步骤的编号)。
①溶解并恢复至室温;②定容;③计算;④转移;⑤量取;⑥洗涤并转移;⑦反复倒转摇匀。
(3)实验中除了需要50mL量筒、烧杯、玻璃棒外,还需要的仪器有
。
(4)定容的正确操作是
。
(5)该小组在实验室中发现了一张注射用质量分数为5%的葡萄糖(分子式为C6Hl2O6,相对分子质量为180)溶液的标签,如下图所示。
则该溶液中含水g;该溶液的物质的量浓度为(小数点后保留2位数)。
呋喃甲醇和呋喃甲酸是有机合成中的常用试剂,可用呋喃甲醛制备,其实验原理为: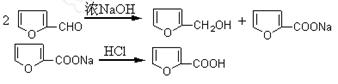
制备方法如下:①在50mL烧杯中放置3.28mL(0.04mol)呋喃甲醛,并用冰水冷却;称取1.6gNaOH溶于少量水中,在搅拌下滴加氢氧化钠水溶液于呋喃甲醛中。②在8~12℃下连续搅拌40min。③向反应混合物加入适量水使其恰好完全溶解,用乙醚萃取分液。④乙醚萃取物用无水硫酸镁干燥后,先在水浴中蒸去乙醚,然后蒸馏,收集169~172℃馏分得1.4g产品。⑤在乙醚提取后的水溶液中慢慢滴加浓盐酸到pH=3,搅拌,冷却,结晶,抽滤。⑥产物用少量冷水洗涤,抽干后,收集粗产物。再提纯后得精产品1.5g。
(1)本实验中,氢氧化钠必须溶于少量的水,否则水量过大主要会影响__________收率。
(2)本实验中要充分连续搅拌40min,其目的是______________________________。
(3)萃取时,用到的主要硅酸盐质的仪器是__________;抽滤的优点是______________________________________________________________________。
(4)呋喃甲酸粗产品提纯的方法是________________________________________。
(5)本实验中呋喃甲酸的产率为________________________________________ 。
盛极一时一种实验室常用的化学试剂,请按要求填空: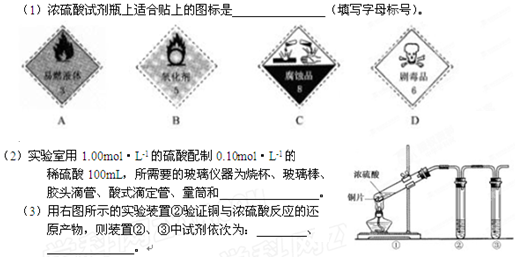
(4)装置①的反应方程式
若装置①中加入铜6.4克和含有0.2摩尔硫酸的浓硫酸产生二氧化硫
A等于6.4克 B 大于6.4克 C 小于6.4克 D不能确定