(1)20世纪30年代,Eyring和Pzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态。NO2和CO反应生成CO2和NO反应是放热反应,NO2和CO的总能量 (填“>”、“<”或“=”)CO2和NO的总能量。
(2)在某体积为2L的密闭容器中充入0.5mol NO2和1mol CO,在一定条件下发生反应:NO2+CO CO2+NO,2 min时,测得容器中NO的物质的量为0.2 mol ,则:
CO2+NO,2 min时,测得容器中NO的物质的量为0.2 mol ,则:
①该段时间内,用CO2表示的平均反应速率为 。
②假设此反应在5 min时达到平衡,则此时容器内气体的总物质的量为 。
③下列事实能够说明上述反应在该条件下已经达到化学平衡状态的是
| A.容器内气体的质量保持不变 |
| B.NO2的物质的量浓度不再改变 |
| C.容器内气体的平均相对分子质量不变 |
| D.NO2的消耗速率与CO2的消耗速率相等 |
E.容器内气体的物质的量保持不变
某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如图所示: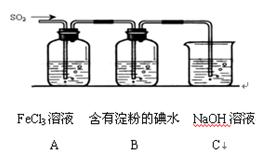
(1)下列实验方案适用于在实验室制取所需SO2的是;
A.Na2SO3溶液与HNO3
B.Na2SO3固体与浓硫酸
C.固体硫在纯氧中燃烧
D.碳与热浓H2SO4
(2)写出SO2气体通入A中的离子反应___________________________________________;
(3)在上述装置中通入过量的SO2,为了验证A中SO2与Fe3+发生了氧化还原反应,
取A中的溶液,分成两份,并设计了如下实验:
方案①:往第一份试液中加入少量酸性KMnO4溶液,紫红色褪去
方案②:往第二份试液加入KSCN溶液,不变红,再加 入新制的氯水,溶液变红
入新制的氯水,溶液变红
上述方案不合理的是 ,原因是;
(4)能表明I-的还原性弱于SO2的现象是。
(5)下图为SO2的制备和收集装置图:(夹持仪器省略)
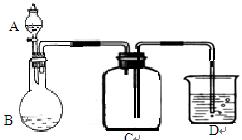
仪器A名称,图中的装置错误的是 (填“A、B、C、D”的一个或多个)
该装置气密性检查的操作是
。
以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3·6H2O)的工艺流程如下: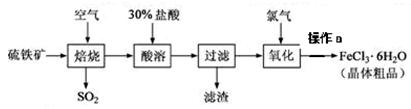
回答下列问题:
(1)在一定条件下,SO2转化为SO3的反应为2SO2+O2 2SO3,该反应的平衡常数表达式为K=;过量的SO2与NaOH溶液反应的化学方程式为。
2SO3,该反应的平衡常数表达式为K=;过量的SO2与NaOH溶液反应的化学方程式为。
(2)用36.5%(密度为1.2g·㎝-3)的盐酸的配制500mL的30%(密度为1.095g·㎝-3的盐酸,所需玻璃仪器是()
| A.玻璃棒 | B.烧杯 | C.托盘天平 | D.500mL量筒 |
E、500mL容量瓶 F、胶头滴管
(3)酸溶及后续过程中均需保持盐酸过量,其目的是、
。
(4)通氯气氧化时,发生的主要反应的离子方程式为;该过程产生的尾气可用碱 溶液吸收,尾气中污染空气的气体为(写化学式)。
溶液吸收,尾气中污染空气的气体为(写化学式)。
(5)操作a为、过滤、洗涤、干燥。
(16分)工业“从海水中提取镁”的流程图如下: 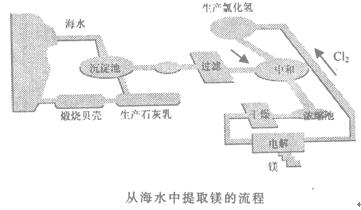
步骤为: ①将海边大量的贝壳煅烧成生石灰,并将生石灰制成石灰乳;
①将海边大量的贝壳煅烧成生石灰,并将生石灰制成石灰乳;
②将石灰乳加入到海水沉淀池中经过滤得到Mg(OH)2沉淀;
③在Mg(OH)2沉淀中加入盐酸得到MgCI2溶液,再经蒸发结晶得到MgCl2·6H2O;
④将MgCl2·6H2O在一定条件下加热得到无水MgCl2;
⑤电解熔融的氯化镁可得到Mg。
⑴步骤①中涉及的化学方程式为 。
⑵步骤③中的蒸发利用风吹日晒完成,但在实验室中蒸发操作时需要的主要仪器有、、酒精灯、三脚架、泥三角、坩埚钳等。
⑶海水中的镁以Mg2+形式存在,设计步骤②③将Mg2+转化为Mg(OH)2又重新转化为Mg2+的目的是。
⑷步骤④中的“一定条件”指的是,目的是。
⑸上述流程中,在降低成本、减少污染方面做了一些工作,请写出其中一点:
⑹有同学认为:可以在步骤②后加热Mg(OH)2得到MgO,再电解熔融的MgO制金属镁,以简化实验步骤,体现实验的简约性原则。你是否同意该同学的观点(填“同意”或“不同意”),理由为。
A、B、C、D、E、F是原子序数依次增大的短周期主族元素,A的最外层电子数是次外层电子数2倍,B是短周期中金属性最强的元素,C是同周期中阳离子半径最小的元素,D元素的最高价氧化物对应水化物与B元素的最高价氧化物对应水化物反应的产物M是制备木材防火剂的原料,E的最外层电子数与内层电子数之比为3﹕ 5。
5。
请回答:
(1)D的元素符号为。
(2)F在元素周期表中的位置。
(3)用电子式表示由元素B和F组成的化合物的形成过程:。(4)B单质与氧气反应的产物与C的 单质同时放入水中,产生两种无色气体,有关的化学方程式为 、 。
单质同时放入水中,产生两种无色气体,有关的化学方程式为 、 。
(5)工业上将干燥的F单质通入熔融的E单质中可制得化合物E2F2,该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,该反应的化学方程式为 。
。
(6)某混合物的稀溶液中,只可能含有B、C、F构成的简单离子或A、E的最高价氧化物对应水化物所电离出来的阴离子。现分别取一定体积的该溶液进行实验。两次每次取200.00mL进行实验。
实验1:取2mL溶液,向其中加入AgNO3溶液有沉淀产生;
实验2:取200mL溶液,向其中加入足量BaCl2溶液后,得干燥沉淀12.54g,沉淀经足量盐酸洗涤、干燥后,剩余4.66g。
请回答:
①根据以上实验,不能判断是否存在的离子有。
② B的简单离子是否存在?;若存在,浓度至少为mol/L(若不存在,则不必回答第二问)。
汽车尾气里含有NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致:
N2(g) + O2(g)  2NO(g)△H > 0
2NO(g)△H > 0
已知该反应在2404℃时,平衡常数K=64×10-4。请回答:
(1)该反应的平衡常数表达式为。
(2)该温度下,向2L密闭 容器中充入N2和O2各1mol,平衡时,N2的转化率是%
容器中充入N2和O2各1mol,平衡时,N2的转化率是%
(保留整数)。
(3)该温度下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10-1mol/L、4.0×10-2mol/L
和3.0×10-3mol/L,此时反应(填“处于化学平衡状态”、“向
正反应方向进行”或“向逆反应方向进行”),理由是
(4)将N2、O2的混合气体充入恒温恒容密闭容器中,下列变化趋势正确的是(填字母序号)。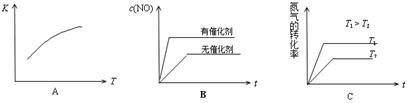
(5)向恒温恒容的密闭容器中充入等物质的量的N2和O2,达到平衡状态后再向其中充入
一定量NO,重新达到化学平衡状态。与原平衡状态相比,此时平衡混合气中NO的
体积分数(填“变大、“变小”或“不变”)。