海洋植物如海带、海藻中含有大量的碘元素,碘元素以碘离子的形式存在.实验室里从海藻中提取碘的流程如图1:
(1)实验室焙烧海带,需要下列仪器中的 (填序号).
a.试管
b.烧杯
c.坩埚
d.泥三角
e.铁三脚架
f.酒精灯
(2)指出提取碘的过程中有关的实验操作名称:① ,③ .
(3)提取碘的过程中,可选择的有机试剂是 .
| A.甲苯、酒精 | B.四氯化碳、苯 |
| C.汽油 、乙酸 | D.汽油、甘油 |
(4)③过程需要使用的主要玻璃仪器为 .
(5)小组用CCl4萃取碘水中的碘,在如图2的分液漏斗中,下层液体呈 色;他们打开分液漏斗活塞,却未见液体流下,原因可能是 .
(6)从含碘的有机溶液中提取碘和回收有机溶剂,还须经过蒸馏,指出下面实验装置图3中的错误之处:
① ;② ;③ .
(7)进行上述蒸馏操作时,使用水浴加热的原因是 .
某研究性学习小组设计实验验证氨气与二氧化硫的性质。请你完成下列研究:
(一)氨气性质探究
(1)实验室制备氨气,下列方法中可选用的是(填编号)
①加热浓氨水;②固体生石灰中滴加浓氨水;③固态氯化铵加热分解;④固态硝酸铵加热分解;
(2)该小组成员设计实验探究氨气还原性及产物,提供实验装置如下:
(3)请你根据提供的装置从左至右连接接口序号()()()()()()
(4)该装置在设计上有一定的缺陷,为确保实验结果的准确性,你对该装置的改进措施是________________;
(5)利用改进后的装置进行实验,观察到CuO全部变为红色物质,无水CuSO4变蓝,同时生成一种无污染的气体。请写出NH3与CuO反应的化学方程式________________;
(6)装置B的作用是:________________;
(二)二氧化硫性质探究
下图是实验室制取SO2并验证SO2的某些性质的装置,试回答: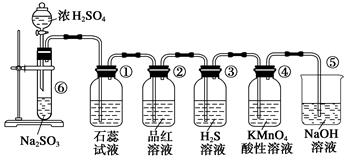
(1)盛放浓硫酸仪器的名称:_________________;
(2)若将浓硫酸改用浓硝酸能否完成此实验探究?答:____________,请写出改用浓硝酸后⑥中的离子反应方程式:_____________________________________
(3)②实验现象为:_________________,证明SO2具有________性;
(4)若③中的试剂改为Na2S溶液,实验现象与原溶液是否相同:______________,含有1mol Na2S的水溶液最多可以吸收SO2的物质的量为:________。
(5)④中发生的离子反应为:_______________________________________。
资料显示:“氨气可在纯氧中安静燃烧……某校化学小组学生设计如下装置(图中铁夹等夹持装置已略去)进行氨气与氧气在不同条件下反应的实验。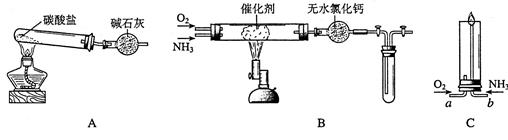
(1)用装置A制取纯净、干燥的氨气,大试管内碳酸盐的化学式是;碱石灰的作用是。
(2)将产生的氨气与过量的氧气通到装置B(催化剂为铂石棉)中,用酒精喷灯加热:
①氨催化氧化的化学方程式是试管内气体变为红棕色,该反应的化学方程式是
②停止反应后,立即关闭B中两个活塞。一段时间后,将试管浸入冰水中。试管内气体颜色变浅,请结合化学方程式说明原因
(3)将过量的氧气与A产生的氨气分别从A、B两管进气口通人到装置C中,并在B管上端点燃氨气,两气体通入的先后顺序是:先通入______(O2 ,NH3 ),后通入__________(O2,NH3)其理由是
某课外活动小组的同学,在实验室做锌与浓硫酸反应的实验时,方方同学认为产生的气体除SO2外,还可能产生氢气。该同学为了验证他的判断是否正确,设计了如图所示的实验装置,其中,装置B中盛有浓硫酸,装置C中放置黑色CuO粉末,装置D中放置的是无水硫酸铜粉末(锌与浓硫酸共热时产生的气体为X,且该装置略去)。试回答: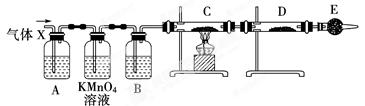
(1) E中加入的试剂是碱石灰,作用是_____________;装置A、B之间的酸性高锰酸钾溶液的作用是_________________;
(2)上述反应中生成二氧化硫的化学方程式为___________________________________;
(3)如果去掉装置B,就不能根据D中的现象判断气体X中有氢气,原因是:_______________________。
(4可以证明气体X中含有氢气的实验现象是:
C中______________________________,D中_______________________。
(14分)某学习小组同学探究FeSO4的化学性质和用途。
(一)利用下图装置探究FeSO4的稳定性和用途。(绿矾成分为FeSO4·7H2O)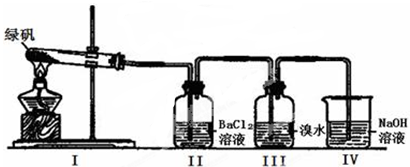
(1)II中有白色沉淀生成,说明FeSO4固体分解生成了_____________。
(2)III中溴水是用来检验是否有SO2气体生成,涉及的化学方程式为_________________,实验中,观察到溴水褪色,据此推测FeSO4分解最有可能被氧化的元素是______________。
(3)Ⅳ中足量NaOH溶液的作用是吸收SO2气体,防止其污染环境,请写出反应的离子方程式___________。
(二)探究FeSO4中Fe2+的还原性
(4)证明FeSO4有较强的还原性,完成下表步骤二及其现象。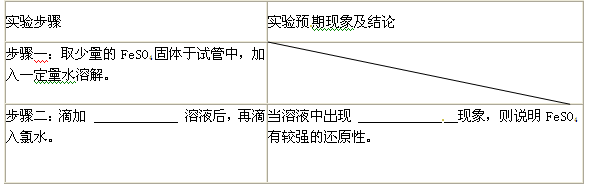
(三)硫酸亚铁用途探究
(5)缺铁性贫血往往口服硫酸亚铁,当用硫酸亚铁制成药片时,外表包有一层特殊的糖衣,其作用是_______________________。
研究性学习小组进行CH4的性质探究实验。
(1)通入高锰酸钾酸性溶液,现象是____。
(2)在无色玻璃集气瓶中与Cl2混合后光照,现象是____。
(3)为了验证CH4是否具有还原性,某小组设计了如下实验: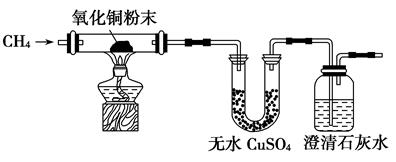
实验过程中还观察到无水CuSO4逐渐变蓝,澄清石灰水出现浑浊现象,则CH4与CuO反应的化学方程式为______。
(4)研究小组将CH4通入溴水时,发现溴水逐渐褪色,你认为原因可能是______。
请设计一个实验方案证明你的结论(用文字表示,不必画实验装置图) ______。