常温下,甲、乙、丙三位同学用实验确定某酸HA是弱电解质的方案分别是:
甲:用pH试纸测定0.1 moI/L HA溶液的pH,即可证明HA是弱电解质。
乙:①分别取pH=l的HA溶液和稀盐酸各10.00 mL,再加水稀释为100 mL:
②各取相同体积的两种稀释液(适量),同时分别加入纯度和形状大小均相同的锌粒(足量),观察现象,即可证明HA是弱电解质。
丙:将适量的HA溶液和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表,分析表中数据可以说明HA是弱电解质。
| 编号 |
NaOH/mol·L-1 |
HA/mol·L-1 |
混合溶液的pH |
| ① |
0.1 |
0.1 |
pH=9 |
| ② |
c |
0.2 |
pH=7 |
| ③ |
0.1 |
0.2 |
pH<7 |
(1)甲的方案中,说明HA是弱电解质的理由是测得溶液的pH_______1(填“>”、“<”或“=”)。甲进行实验时的具体操作方法是_______________。
(2)在乙的方案的第①步中,需要用到的定量仪器是___________。pH均为1的HA溶液和稀盐酸中,水的电离程度的大小关系是____________(填字母)。
a.HA溶液中水的电离程度大
b.稀盐酸中水的电离程度大
c.两种溶液中水的电离程度相同
(3)乙的方案中,说明HA是弱电解质的主要现象是_________(填字母)。
A.装稀盐酸的试管中放出H2的速率快
B.装HA溶液的试管中放出H2的速率快
C.两个试管中产生气体的速率一样快
(4)丙的方案中,编号②中的c_______(填“>”、“<”或“=”)0.l,该混合液中的离子浓度:c(Na+)________(填“>”、“<”或“=”)c(A-)。
(5)丙的方案中,编号③的数据表明,混合溶液中HA的电离程度比NaA的水解程度:________(填“强”、“弱”或“无法确定”)。
锂离子电池的应用很广,其正极材料可再生利用。某锂离子电池正极材料有钴酸锂(LiCoO2)、导电剂乙炔黑和铝箔等。充电时,该锂离子电池负极发生的反应为6C+xLi++xe-==LixC6。现利用以下工艺流程回收正极材料中某些金属资源(部分条件未给出)。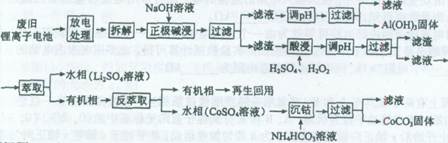
(1)LiCoO2中,Co元素的化合价为______。
(2)写出“正极碱浸”中发生反应的离子方程式____________________。
(3)“酸浸”一般在80℃下进行,写出该步骤中发生的所有氧化还原反应的化学方程式____________;可用盐酸代替H2SO4和H2O2的混合液,但缺点是__________。
(4)写出“沉钴”过程中发生反应的化学方程式__________________________。
(5)充放电过程中,发生LiCoO2与LixCoO2之间的转化,写出放电时电池反应方程式___________________。
(6)上述工艺中,“放电处理”有利于锂在正极的回收,其原因是__________________。在整个回收工艺中,可回收到的金属化合物有_________________(填化学式)。
工业生产纯碱的工艺流程示意图如下:
完成下列填空:
(1)粗盐水加入沉淀剂A、B除杂质(沉淀剂A来源于石灰窑厂),写出A、B的化学式。
A______________B____________。
(2)实验室提纯粗盐的实验操作依次为:
取样、__________、沉淀、__________、__________、冷却结晶、__________、烘干。
(3)工业生产纯碱工艺流程中,碳酸化时产生的现象是__________________。
碳酸化时没有析出碳酸钠晶体,其原因是______________________.
(4)碳酸化后过滤,滤液D最主要的成分是______________(填写化学式),检验这一成分的阴离子的具体方法是:______________________。
(5)氨碱法流程中氨是循环使用的,为此,滤液D加入石灰水产生氨。加石灰水后所发生的反应的离子方程式为:____________________________。
(6)产品纯碱中含有碳酸氢钠。如果用加热分解的方法测定纯碱中碳酸氢钠的质量分数,纯碱中碳酸氢钠的质量分数可表示为:__________(注明你的表达式中所用的有关符号的含义)。
(2013)氧化镁在医药、建筑等行业应用广泛.硫酸镁还原热解制备高纯氧化镁是一种新的探索.以菱镁矿(主要成分为MgCO3,含少量FeCO3)为原料制备高纯氧化镁的实验流程如下:
(1)MgCO3与稀硫酸反应的离子方程式为 .
(2)加入H2O2氧化时,发生反应的化学方程式为 .
(3)滤渣2 的成分是 (填化学式).
(4)煅烧过程存在以下反应:
2MgSO4+C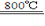 2MgO+2SO2↑+CO2↑
2MgO+2SO2↑+CO2↑
MgSO4+C  MgO+SO2↑+CO↑
MgO+SO2↑+CO↑
MgSO4+3C  MgO+S↑+3CO↑
MgO+S↑+3CO↑
利用如图装置对煅烧产生的气体进行分步吸收或收集.
①D中收集的气体可以是 (填化学式).
②B中盛放的溶液可以是 (填字母).
a.NaOH 溶液 b.Na2CO3溶液c.稀硝酸d.KMnO4溶液
③A中得到的淡黄色固体与热的NaOH溶液反应,产物中元素最高价态为+4,写出该反应的离子方程式: .
利用钛白工业的副产品FeSO4(含TiO2+、Al3+)可以生产电池级高纯超微细草酸亚铁。其工艺流程如下:
(1)检验FeSO4是否已有部分氧化的方法是 。
(2)已知过滤1得到的滤渣的主要成分是Al(OH)3、H2TiO3。请补充化学方程式:
TiOSO4 + =H2SO4 + H2TiO3↓;
铁粉的作用有:①除去溶液中的Fe3+,② 。
(3)沉淀反应的离子方程式是 。
(4)沉淀过程的反应温度为40℃,温度不宜过高的原因除了控制沉淀的粒径外,还有 。FeC2O4生成后,为提高产品纯度,还需调节溶液pH=2,若pH过低,则导致FeC2O4的产率______(填“偏高”、“偏低”或“无影响”)。
(5)过滤2得到的滤液经蒸发浓缩、 、洗涤可得到副产品,该物质可作用于 (写出一种用途)。
乙酰水杨酸俗称阿司匹林,是一种历史悠久的解热镇痛热。合成原理是
(1)水杨酸中含氧官能团的名称是 ,有关水杨酸的说法,正确的是 。
| A.遇FeCl3溶液可能显紫色 |
| B.可发生酯化反应和水解反应 |
| C.能与溴水发生取代反应和加成反应 |
| D.1mol水杨酸最多能与3molH2发生加成反应 |
(2)水杨酸与乙酸酐反应的反应类型是 。
(3)乙酰水杨酸的分子式为 ,1mol乙酰水杨酸最多能与 molNaOH反应。
(4)虚框中为提纯,是为了除去该反应的副产物:水杨酸、乙酰水杨酸水杨酯、乙酰水杨酸酐和聚合物等请写出乙酰水杨酸粗品中加入饱和Na2CO3溶液发生的主要化学反应方程式为:_____ 。
(5)写出一种符合下列条件的乙酰水杨酸的同分异构体的结构简式: 。
Ⅰ.能遇FeCl3溶液显紫色
Ⅱ.苯环上只有一种一溴取代物
Ⅲ.能发生银镜反应
Ⅳ.1mol该化合物能分别与1molNaOH和2mol金属钠反应
(6)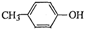 也能与乙酸酐发生类似反应,请写出化学反应方程式,可不写条件:
也能与乙酸酐发生类似反应,请写出化学反应方程式,可不写条件:
。