对于100mL1mol/L盐酸与铁片的反应,采取下列措施:①升高温度;②改用100mL3mol/L盐酸;③改用300mL1mol/L盐酸;④用等量铁粉代替铁片;⑤改用98%的硫酸。其中能使反应速率加快的是
| A.①③④ | B.①②④ | C.①②③④ | D.①②③⑤ |
相同温度下,体积均为0.5L的两个恒容密闭容器中发生可逆反应:X2(g)+3Y2(g)  2XY3(g)△H=-92.6kJ/mol;反应在起始及达到平衡时的有关数据如下表所示:下列叙述不正确的是
2XY3(g)△H=-92.6kJ/mol;反应在起始及达到平衡时的有关数据如下表所示:下列叙述不正确的是
| 容器 编号 |
起始时各物质的物质的量/mol |
达平衡时体系能量的变化 |
||||||
| X2 |
Y2 |
XY3 |
||||||
| ① |
1 |
3 |
0 |
放热46.3kJ |
||||
| ② |
0.4 |
1.2 |
1.2 |
Q
|
一定条件下,建立平衡2NO2 (g) 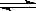 N2O4(g),以下说法正确的是
N2O4(g),以下说法正确的是
| A.恒温恒容,再充入NO2,达到新平衡时,NO2的体积分数增大 |
| B.恒温恒容,再充入N2,达到新平衡时,容器内颜色变浅 |
| C.恒温恒压,再充入N2O4,达到新平衡时,混合气体的平均相对分子质量增大 |
| D.恒温恒压,再充入Ar,达到新平衡时,NO2的转化率降低 |
将 lmolSO2和 l mol O2通入体积不变的密闭容器中,在一定温度和催化剂作用下,反应达到平衡时 SO3为0.3mol,若此时移走 0.5mol O2和 0.5mol SO2则反应达到新的平衡时,SO3的物质的量是
| A.0.3mol | B.0.15mol |
| C.小于 0.15mol | D.大于0.15mol而小于 0.3mol |
已知2-丁烯有顺、反两种异构体,在某条件下两种气体处于平衡,下列说法正确的是: △H=-4.2 kJ/mol
△H=-4.2 kJ/mol
| A.顺-2-丁烯比反-2-丁烯稳定 |
| B.顺-2-丁烯的燃烧热比反-2-丁烯大 |
| C.加压和降温有利于平衡向生成顺-2-丁烯反应方向移动 |
| D.反-2-丁烯和顺-2-丁烯具有相同的熔沸点 |
下列说法正确的是(NA表示阿伏加德罗常数的值)
| A.1 mol聚乙烯含有的原子数目为6NA |
| B.20℃时,1 mol己烷完全燃烧后恢复至原状态,生成气态物质分子数为6NA |
| C.1 mol甲基含10 NA个电子 |
| D.2.8 g乙烯和丙烯的混合气体中所含原子数为0.2NA |