下列关于0.2 mol/L硝酸钾溶液的叙述中,正确的是
| A.1 L该溶液中含硝酸钾202 g |
| B.100 mL该溶液中含硝酸钾0.02 mol |
| C.从1 L该溶液中取出500 mL后,剩余溶液的浓度为0.1 mol/L |
| D.1 L水中溶解0.2 mol硝酸钾,即可配得0.2 mol/L硝酸钾溶液 |
下列化学表达方式不正确的是
| A.中子数为20的氯原子:37Cl |
B.Cl-的结构示意图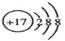 |
C.氢氧根离子的电子式: |
| D.HClO的结构式 H-Cl-O |
重水(D2O)是重要的核工业原料,下列说法错误的是
A.氘(D)原子核外有1个电子
B.1H与D互称同位素
C.H2O与D2O互称同素异形体
D.1H218O与D216O的相对分子质量相同
某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl。下列说法正确的是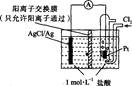
| A.正极反应为AgCl+e-═Ag+Cl- |
| B.放电时,交换膜右侧溶液中有大量白色沉淀生成 |
| C.若用NaCl溶液代替盐酸,则电池总反应随之改变 |
| D.当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.02 mol离子 |
一定条件下,2SO2(g)+O2(g) 2SO3(g)△H<0,有关叙述正确的是
2SO3(g)△H<0,有关叙述正确的是
| A.升高温度,v(正)变大,v(逆)变小 |
| B.恒温恒容,充人O2,02的转化率升高 |
| C.恒温恒压,充人N2,平衡不移动 |
| D.恒温恒容,平衡前后混合气体的密度保持不变 |
为了探索外界条件对反应aX(g)+bY(g) cZ(g)的影响,以X和Y的物质的量比为a:b开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示。以下判断正确的是
cZ(g)的影响,以X和Y的物质的量比为a:b开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示。以下判断正确的是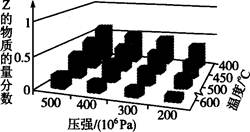
| A.△H>0,a+b>c | B.△H>0,a+b<c |
| C.△H<0,a+b>c | D.△H<0,a+b<c |