【选修3:物质结构与性质】
Ⅰ.Fe3+可以与SCN-、CN-、F-、有机分子等形成很多的配合物。请回答下列问题:
(1)基态Fe3+的价电子排布式可表示为 。
(2)金属配合物Fe(CO)n的中心原子价电子数与配体提供电子总数之和为18,则n= 。
Ⅱ.已知氮化铝的晶胞结构如图所示。请回答下列问题:

(3)NH3空间构型为 ;
(4)若氮化铝可由(CH3)3Al和NH3在一定条件下反应制得,则反应的方程式为 。
(5)若Al与N 原子最近的距离为a cm,则该晶体的密度为 g/cm。(阿伏加德罗常数用NA表示)
研究NO2、SO2、CO等大气污染气体的处理有重要意义。
(1)NO2可用水吸收,相应的化学方程式为______。
利用反应6NO2+8NH3 7N2+12H2O
7N2+12H2O
也可以处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是______L。
(2)已知:2SO2(g)+ O2 (g)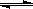 2SO3 (g) △H =-196.6kJ·mol-1
2SO3 (g) △H =-196.6kJ·mol-1
2NO(g)+ O2 (g) 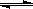 2NO2 (g) △H =-113.0kJ·mol-1
2NO2 (g) △H =-113.0kJ·mol-1
则反应NO2(g)+ SO2 (g) 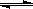 SO3 (g) +NO(g)△H =______kJ·mol-1
SO3 (g) +NO(g)△H =______kJ·mol-1
一定条件下,将体积比为1:2的 NO2和 SO2的混合气体置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是______。
a.体系压强保持不变 b.混合气体颜色保持不变
c.SO3与NO的体积比保持不变 d.每消耗1molSO3的同时生成1molNO2
测得上述反应平衡时的NO2与SO2体积比为1:6,则平衡常数K=______。
(3)CO可用于合成甲醇,反应方程式为CO(g)+ 2H2 (g) 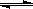 CH3OH (g)。CO在不同温度下的平衡转化率与压强的关系如图所示。该反应△H _____0(填“>”或“<”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是________。
CH3OH (g)。CO在不同温度下的平衡转化率与压强的关系如图所示。该反应△H _____0(填“>”或“<”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是________。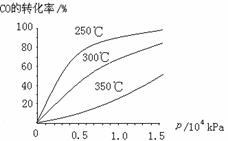
下图是一个乙醇燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少,请回答下列问题: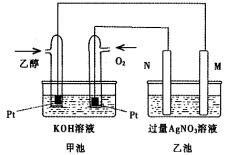
(1)M电极的材料是 ,电极名称是 ,N的电极反应式为 ,通入乙醇的铂电极的电极反应式为 。
(2)在此过程中,乙池中某一电极析出金属银4.32g时,甲池中理论上消耗氧气为 L(标准状况下);若此时乙池溶液的体积为400mL,则乙池中溶液的pH为 。
(3)若在常温常压下,1g C2H5OH燃烧生成CO2和液态H2O时放出29.71kJ热量,表示该反应的热化学方程式为 。
A、B两种有机物均是有机合成的中间体,其中A的分子式为C4H7O2Br,B分子中含2个氧原子,其燃烧产物n(CO2) : n(H2O)=2:1, B的相对分子质量为188。A和B存在如下转化关系: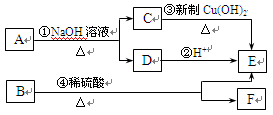
已知:①一个碳原子上连有两个羟基时,易发生下列转化: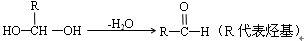
②同一个碳原子上连有两个双键的结构不稳定。
请回答:
(1)A的结构简式是。
(2)B的化学式是。
(3)写出下列反应的化学方程式
反应①;
反应③。
(4)F具有如下特点:①具有弱酸性;②可以形成五种一氯代物,其中苯环上只有两种;④除苯环外,不含有其他环状结构。写出符合上述条件且具有稳定结构的任意两种同分异构体的结构简式:、。
Ⅰ.在一定条件下,xA+yB zC,达到平衡,试填写下列空白:
zC,达到平衡,试填写下列空白:
(1)已知C是气体,且x+y=z,加压时平衡如果发生移动,则平衡必向方向移动。
(2)若B、C是气体,其他条件不变时增加A的用量,平衡不移动,则A的状态为。
Ⅱ.已知NO2和N2O4可以相互转化:2NO2(g) N2O4(g) ΔH<0。现将一定量NO2和N2O4的混合气体通入体积为2L的恒温密闭玻璃容器中,反应物浓度随时间变化关系如下图。
N2O4(g) ΔH<0。现将一定量NO2和N2O4的混合气体通入体积为2L的恒温密闭玻璃容器中,反应物浓度随时间变化关系如下图。
(1)图中共有两条曲线X和Y,其中曲线表示NO2浓度随时间的变化;
a、b、c、d四个点中,表示化学反应处于平衡状态的点是。
下列不能说明该反应已达到平衡状态的是。
A.容器内混合气体的压强不随时间变化而改变
B.容器内混合气体的密度不随时间变化而改变
C.容器内混合气体的颜色不随时间变化而改变
D.容器内混合气体的平均分子量不随时间变化而改变
(2)前10min内用NO2表示的化学反应速率v(NO2)=。
(3)反应25min时,若只改变了某一个条件,使曲线发生如上图所示的变化,该条件可能是(用文字表达);
(4)若要达到使NO2(g)的百分含量与d点相同的化学平衡状态,在25min时还可以采取的措施是。
A.加入催化剂 B.缩小容器体积 C.升高温度 D.加入一定量的N2O4
下表是元素周期表的一部分,A、B、C、D、E、X、Y是表中给出元素组成的常见单质或化合物。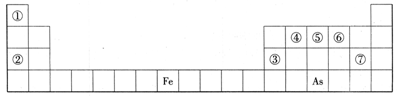
已知A、B、C、D、E、X存在如图所示转化关系(部分生成物和反应条件略去)
(1)若E为单质气体,D为白色沉淀, C与X反应的离子方程式为。
(2)若E为氧化物,则A的化学式为,A与水反应的化学方程式为。
①当X是显碱性的盐溶液,C分子中有22个电子时,则C的电子式为,表示X呈碱性的离子方程式为。
②当X为金属单质时,X与B的稀溶液反应生成C的离子方程式为。