1 L Al2(SO4)3和MgSO4的混合溶液中,含Mg2+2.4 g,SO42-的物质的量浓度为1 mol/L,则MgSO4和Al3+的物质的量浓度分别是_____________、___________。
电镀污泥中含有Cr(OH)3、Al2O3、ZnO、CuO、NiO等物质,工业上通过“中温焙烧—钠氧化法”回收Na2Cr2O7等物质。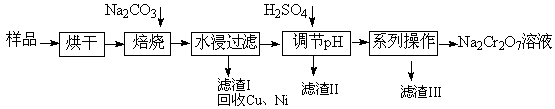
已知:水浸后溶液中存在Na2CrO4、NaAlO2[也可表示为NaAl(OH)4]、Na2ZnO2等物质。
(1)水浸后回收Cu、Ni时的操作是。水浸后的溶液呈性(“酸”、“碱”、“中”)
(2)完成氧化焙烧过程中生成Na2CrO4的化学方程式
Cr(OH)3 + Na2CO3 + O2 Na2CrO4 + CO2 +H2O
Na2CrO4 + CO2 +H2O
(3)滤渣II的主要成分有Zn(OH)2、。
(4)已知:①除去滤渣II后,溶液中存在如下反应:CrO42—+ 2H+ Cr2O72—+ H2O;②Na2Cr2O7、Na2CrO4在不同温度下的溶解度如下表
Cr2O72—+ H2O;②Na2Cr2O7、Na2CrO4在不同温度下的溶解度如下表
| 化学式 |
20℃ |
60℃ |
100℃ |
| Na2SO4 |
19.5 |
45.3 |
42.5 |
| Na2Cr2O7 |
183 |
269 |
415 |
| Na2CrO4 |
84 |
115 |
126 |
“系列操作”中为:继续加入H2SO4,冷却结晶,过滤。继续加入H2SO4目的是__________________________________________________。
(5)工业上还可以在水浸过滤后的溶液(Na2CrO4)加入适量H2SO4,用石墨做电极电解生产金属铬,写出生成铬的电极反应方程式。
某塑化剂(DEHP)的结构简式为:
其合成路线如下: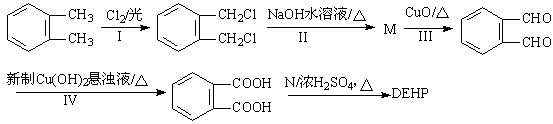
(1)DEHP的分子式;
(2)反应I的类型,反应IV的产物中含氧官能团的名称。
(3)M,N的结构简式分别为M、N。
(4)反应IV的化学方程式;
(5)一定条件下,1mol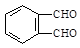 和足量的H2反应,最多可消耗H2mol。
和足量的H2反应,最多可消耗H2mol。
(6)分子式为C8H6Cl4的一种同分异构体可以通过类似: 的反应得到
的反应得到 ,请写出该同分异构体的结构简式:。
,请写出该同分异构体的结构简式:。
尿素[CO(NH2)2]是一种非常重要的高氮化肥,以天然气(含H2S)为原料合成尿素的主要步骤如下图所示(图中某些转化步骤未列出)。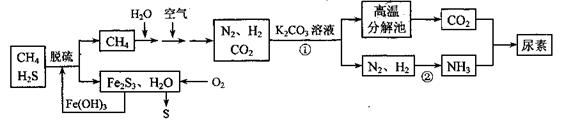
请回答下列问题:
(1)反应①的离子方程式是______________
(2)天然气脱硫后产生的Fe2S3和H2O与02反应的化学方程式是_______。
(3)反应②是放热反应,温度升高,该反应的平衡常数_______ (填 “增大”、“减小” 或“不变”)。H2NCOONH4(氨基甲酸铵)是合成尿素的中间体,其中碳原子的杂化轨道类型是_______杂化。
(4)如果整个生产过程釆用绿色化学工艺,则生产120t尿素理论上需要CH4___m3 (标准状况)。
(5)化学家正在研究尿素动力燃料电池,尿液也能发电!用这种电池直接去除城市废水中的尿素,既能产生净化的水又能发电。尿素燃料电池结构如图所示,工作时负极的电极反应式为__________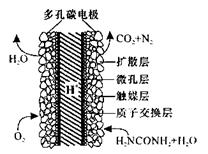
在某锂离子电池中,有一种有机聚合物作为正负极之间锂离子迁移的介质,该有机聚合物的单体之一(用M表示)的结构简式如右: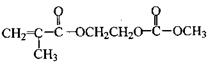
用相对分子质量为56的单烯烃A合成M的方法可设计如下: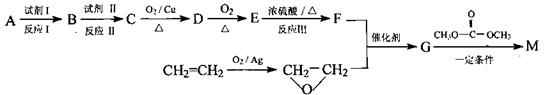
请回答下列问题:
(1)A的结构简式是_______试剂II是________,反应III的化学反应类型是_______。
(2)G在一定条件下反应生成的高聚物是制备隐形眼镜的材料,请写出生成该高聚物的化学反应方程式______________
(3)M与足量氯氧化钠溶液反应的化学方程式是______________
(4)在用E制备F的过程中,2分子的E反应会生成一种副产物,其核磁共振氢谱只有一种吸收峰,该副产物的结构简式为______________。
A、B、D、E、G、M代表六种常见元素,它们的核电荷数依次增大。其中,元素M的基态3d轨道上有2个电子,A的基态原子L层电子数是K层电子数的2倍,E的简单离子在同周期元素的简单离子中半径最小,D、G同主族;B与D形成的化合物有多种,其中一种是红棕色气体。
(1)M的基态原子价层电子排布式为_____,元素B、D、G的第一电离能由大到时小的顺序是_____ (用元素符号表示)。
(2)用价层电子对互斥理论预测,GD32-的立体构型是_____ (用文字表述)
(3)M与D形成的一种橙红色晶体晶胞结构如图所示,其化学式为_____ (用元素符号表示)。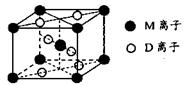
(4)已知化合物EB结构与单晶硅相似,该物质可由E 的氯化物与NaB3在高温下反应制得,且生成单质B2,该反应化学方程式为_____,若有8.4gB2生成,则转移电子数为_____。