某实验小组用0.50 mol·L-1NaOH溶液和0.50 mol·L-1硫酸溶液进行中和热的测定。
Ⅰ.配制0.50 mol·L-1NaOH溶液
(1)若实验中大约要使用245mLNaOH溶液,至少需要称量NaOH固体 g。
(2)从下图中选择称量NaOH固体所需要的仪器是(填字母): 。
| 名称 |
托盘天平 (带砝码) |
小烧杯 |
坩埚钳 |
玻璃棒 |
药匙 |
量筒 |
| 仪器 |
 |
 |
 |
 |
 |
 |
| 序号 |
a |
b |
c |
d |
e |
f |
Ⅱ.测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示。

(1)写出该反应中和热的热化学方程式:(中和热为57.3 kJ·mol-1) 。
(2)取50 mLNaOH溶液和30 mL硫酸溶液进行实验,实验数据如下表。
| 试验次数 |
起始温度t1/℃ |
终止温度 t2/℃ |
温度差平均值 (t2-t1)/℃ |
||
| H2SO4 |
NaOH |
平均值 |
|||
| 1 |
26.2 |
26.0 |
26.1 |
29.6 |
|
| 2 |
27.0 |
27.4 |
27.2 |
31.2 |
|
| 3 |
25.9 |
25.9 |
25.9 |
29.8 |
|
| 4 |
26.4 |
26.2 |
26.3 |
30.4 |
①上表中的温度差平均值为 ℃。
②近似认为0.50 mol·L-1 NaOH溶液和0.50 mol·L-1硫酸溶液的密度都是1 g·cm-3,中和后生成溶液的比热容c=”4.18” J·(g·℃)-1。则中和热ΔH= (取小数点后一位)。
③上述实验数值结果与57.3 kJ·mol-1有偏差,产生偏差的原因可能是(填字母) 。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
④实验中改用60mL0.5mol/L盐酸跟50mL0.55moi/L氢氧化钠进行反应,与上述实验相比,所放出的热量 (填相等或不相等,下同),所求的的中和热 简述理由 。
50 mL 0.050 mol/L 盐酸与50 mL 0.55 mol/L NaOH溶液在如图所示的装置中
进行中和反应,通过测定反应过程中所放出的热量可计算中和热。试回答下列问题:
⑴从实验装置上看,图中尚缺少的一种玻璃仪器是 。
⑵大小烧杯间填满碎纸条的作用是 。
⑶大烧杯上如不盖硬纸板,求得的中和热数值将 (填“偏大”、“偏小”、或“无影响”)。结合日常生活的实际该实验该在 中进行效果更好。
⑷实验中改用60 mL 0.050 mol/L 盐酸与50 mL 0.55 mol/L NaOH溶液进行反应与上述实验相比,所放出的热量 (填“相等”或“不相等”),所求中和热 (填“相等”或“不相等”),简述理由 。
⑸用相同浓度、相同体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会
(填“偏大”、“偏小”、或“无影响”);用50 mL 0.50 mol/L NaOH溶液进行上述实验,测得的中和热的数值会 (填“偏大”、“偏小”、或“无影响”)。
实验室可用硫化氢通人碘粉末的悬浊液制取一定浓度的氢碘酸。其主要装置如图所示,所用的试剂有:稀盐酸;用ott0法压成的硬方块形CaS;碘在水中的悬浊液;NaOH溶液;NaHS饱和溶液。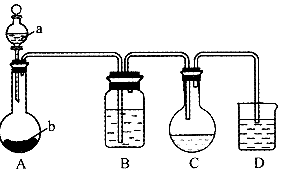
(1)在仪器中盛有的试剂:A中的a为,A中的b为,B为,D为。
(2)C中反应完全时,应呈现的现象是什么?
(3)D中的导气管末端是否应插入液面以下?请说明理由。
(4)氢碘酸在溶质的质量分数为57%时,可形成“恒沸点”溶液,在125~127℃沸腾出的蒸气中为57%的HI。试设计用C中液体制取57%的氢碘酸的主要方法。
(5)氢碘酸在空气中发雾,应保存于封得很严的暗色瓶中。为防止HI的氧化,在密封之前最好采用的措施是什么?(发挥你的创见)
有一硝酸钾溶液,其中混入少量KBr、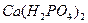 ,有人拟用
,有人拟用 、
、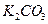 、KOH和
、KOH和 作试剂除去杂质,且最后溶液中只含
作试剂除去杂质,且最后溶液中只含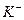 、
、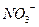 、
、 。
。
(1)加入试剂的顺序是:。
(2)用离子方程式依次表示所发生的各化学反应
我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业做出了突出贡献。他利用NaHCO3、NaCl、NH4C1等物质溶解度的差异,以食盐、氨气为原料先制得NaHCO3,进而生产出纯碱。下面是在实验室中模拟“侯氏制碱法”中制取NaHCO3的实验步骤:
第一步:连接好装置图(如下),检查气密性,在仪器内装入药品。
第二步:先让一装置发生反应,直到产生的气体不能再在C中溶解时,再通入另一装置中产生的气体,片刻后C中出现固体,继续向C中通入两种气体,直到不再有固体产生。
第三步:过滤C中所得的混合物,得到NaHCO3固体。
第四步:向滤液中加入适量的NaCl粉末,有NH4Cl晶体析出。
请回答下列问题:
(1)装置的连接顺序是:(a)接( )( )接( );(b)接( )。
(2)A中常选用的固体为;D中应选用的液体为;B中发生反应的化学方程式为。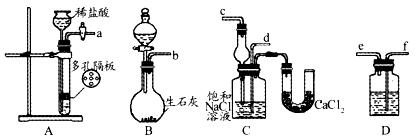
(3)第二步中必须让装置先发生反应。
(4)C中用球形干燥管而不用直导管,其作用是,C中广口瓶内发生反应的化学方程式为。
(5)第四步中分离出NH4Cl晶体的操作是;其所得的NH4Cl晶体中常含有少量的NaCl和NaHCO3 (约占5%~8%),请设计一个简单的实验证明所得固体的成分大部分是NH4Cl,简要写出操作和现象:。
某光卤石(KCl·MgCl2·6H2O)样品中含有不跟NaOH溶液和盐酸反应的杂质,某校化学课外活动研究小组现欲测定此样品中含KCl·MgCl2·6H2O的质量分数,经讨论有多种实验测定方案。
请根据提供的实验试剂和仪器(所需的仪器任选),选择精确度较高的实验测定方案,简要写出第二步以后的实验步骤和实验结果。
一、可选用的实验试剂:
(1)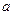 mol·L
mol·L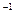 NaOH溶液 (2)
NaOH溶液 (2)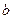 mol·L
mol·L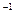 Na2CO3溶液 (3)c mol·L
Na2CO3溶液 (3)c mol·L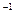 HCl溶液
HCl溶液
(4)d mol·L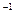 AgNO3溶液 (5)酚酞试液 (6)甲基橙试液
AgNO3溶液 (5)酚酞试液 (6)甲基橙试液
二、实验步骤:
第一步:称取m g样品,放入250mL烧杯中,加适量水溶解
第二步:
计算样品中含KCl·MgCl2·6H2O(相对分子质量为277.5)的质量分数的表达式:
。