(1)在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:CO(g)+H2O(g) CO2(g)+H2(g);△H<0。CO和H2O浓度变化如下图,则0~4min的平均反应速率v(CO)=______________mol/(L·min)
CO2(g)+H2(g);△H<0。CO和H2O浓度变化如下图,则0~4min的平均反应速率v(CO)=______________mol/(L·min)


(2)t1℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如右上表。请回答:
①表中3min~4min之间反应处于____________状态;C1数值__________0.08mol/L(填大于、小于或等于)。
②反应在4min~5min问,平衡向逆方向移动,可能的原因是____________(单选),表中5min—6min之间数值发生变化,可能的原因是____________(单选)。
a、增加了水蒸气的量 b、降低温度 c、使用催化剂 d、增加氢气浓度
经测定某苯的含氧衍生物相对分子质量为122。
(1)若该物质分子中只含一个氧原子,则其化学式为,如果其分子中没有甲基,则它遇FeCl3溶液(填“能”或“不能”)发生显色反应,如果其遇FeCl3溶液会发生显色反应,则这样的结构共有种。
(2)若该物质分子中含有两个氧原子,则其化学式为,其可能的结构共有
种,其中用水能与其他同分异构体区别出来的是(写出结构简式)。
含有C、H、O的化合物,其C、H、O的质量比为12∶1∶16,其蒸气相对于氢气的密度为58,它能使甲基橙溶液变红,也能使溴水褪色,0.58g这种物质能与50mL0.2mol/L的氢氧化钠溶液完全反应。试回答:
(1)该有机物中各原子个数比N(C)∶N(H)∶N(O)=
(2)该有机物的摩尔质量为,写出分子式
(3)该有机物的可能结构简式有
多巴胺是一种重要的中枢神经传导物质,用来帮助细胞传送脉冲的化学物质,能影响人对事物的欢愉感受。多巴胺可用香兰素与硝基甲烷等为原料按下列路线合成: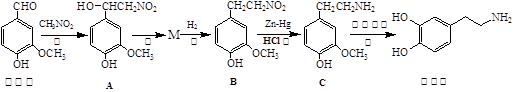
(1)香兰素保存不当往往会导致颜色、气味发生明显变化,其原因是
(2)多巴胺中的官能团的名称是、;反应②的反应条件为
;反应④的反应类型为反应。
(3)写出反应①的化学方程式
(4)写出同时满足下列条件的B的一种同分异构体的结构简式:
①具有天然α-氨基酸的共同结构②能与FeCl3溶液发生显色反应
③有6种不同化学环境的氢原子
含苯酚的工业废水处理的流程图如下所示: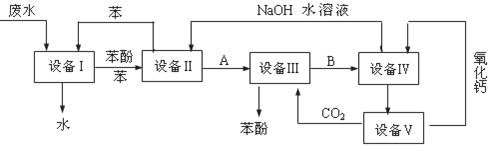
(1)上述流程里,设备Ⅰ中进行的是操作(填操作名称),实验室里这一步操作可以用进行(填仪器名称)。
(2)由设备Ⅱ进入设备Ⅲ的物质A是,由设备Ⅲ进入设备Ⅳ的物质B是
(3)在设备Ⅲ中发生反应的化学方程式为
(4)在设备Ⅳ中,物质B的水溶液和CaO反应后,产物是NaOH、H2O和,通过
操作(填操作名称)可使产物相互分离。
(5)图中,能循环使用的物质是C6H6、CaO、
某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质。以加热处理聚丙烯废塑料为例,实验装置如下左图,处理后得到的产物如下右表。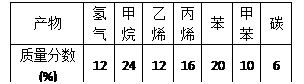
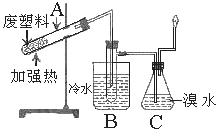
(1)试管A中残余物有多种用途,如下列转化就可制取高聚物聚乙炔。
写出反应③的化学方程式
(2)试管B收集到的产品中,能使酸性高锰酸钾溶液褪色的物质,其一氯代物有种。
(3)锥形瓶C中观察到的现象
经溴水充分吸收,剩余气体经干燥后的体积比为(请注明气体)。
(4)写出C中逸出的气体在工业上的两种用途、