二氧化硒(SeO2)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3或浓H2SO4反应生成SeO2以回收Se。完成下列填空:
(1)Se和浓HNO3反应的还原产物为NO和NO2,且NO和NO2的物质的量之比为1:1,写出Se和浓HNO3反应的化学方程式___ _____。
(2)已知:Se + 2H2SO4(浓) → 2SO2↑ + SeO2 + 2H2O
2SO2 + SeO2 + 2H2O → Se + 2SO42-+ 4H+
SeO2、H2SO4(浓)、SO2的氧化性由强到弱的顺序是_____________________。
(3)回收得到的SeO2的含量,可以通过下面的方法测定:
①SeO2 + KI + HNO3 → Se + I2 + KNO3 + H2O
②I2 + 2Na2S2O3 → Na2S4O6 + 2NaI
配平方程式①,标出电子转移的方向和数目______________________________。
(4)实验中,准确称量SeO2样品0.1500 g,消耗了0.2000 mol/L的Na2S2O3溶液25.00 mL,所测定的样品中SeO2的质量分数为_____________。
有A、B、C、D、E五种元素,其中A、B、C属于同一周期,A原子最外层p能级的电子数等于次外层的电子总数;B原子最外层中有两个不成对的电子;D、E原子核内各自的质子数与中子数相等;B元素可分别与A、C、D、E生成RB2型化合物,并知在DB2和EB2中,D与B的质量比为7:8;E与B的质量比为1:1。试回答:
(1)写出D原子的电子排布式────────────────
(2)写出AB2的结构式━━━━━━━━━━━━━━━━━━━━
(3)用电子式表示AE2的 形成过程━━━━━━━━━━━━━━━━━━━━
形成过程━━━━━━━━━━━━━━━━━━━━
(4)B、C两元素的第一电离能大小关系为:───>────(填写元素符号),原因是─────────────────────────────────────。
(5)根据VSEPR模型预测C的氢化物的立体结构为──────────,中心原子C的轨道杂化类型为────────。
(6)C的单质中π键的数目为──────,B、D两元素的气态氢化物的稳定性大小关系为:───>────(填写化学式)。
已知元素的某种性质“X”和原子半径、金属性、非金属性等一样,也是元素的一种基本性质。下面给出13种元素的X的数值:
| 元素 |
Al |
B |
Be |
C |
Cl[ |
F |
Li |
| X的数值 |
1.5 |
2.0 |
1.5 |
2.5 |
2.8 |
4.0 |
1.0 |
| 元素 |
Mg |
Na |
O |
P |
S |
Si |
|
| X的数值 |
1.2 |
0.9 |
3.5 |
2.1 |
2.5 |
1.7 |
试结合元素周期律知识完成下列问题:
(1)经验规律告诉我们:当形成化学键的两原子相应元素的X差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键。试推断AlBr3中的化学键类型是______。
(2)根据上表给出的数据,简述主族元素的X的数值大小与元素的金属性或非金属性强弱之间的关系______________________________;简述第二周期元素(除惰性气体外)的X的数值大小与原子半径之间的关系_____________________________________________。
(3)请你预测Br与I元素的X数值的大小关系________。
(4)某有机化合物分子中含有S—N键,你认为该共用电子对偏向于________原子(填元素符号)。
1994年度诺贝尔化学奖授予为研究臭氧作出特殊贡献的化学家。O3能吸收有害紫外线,保护人类赖以生存的空间。O3分子的结构如下图所示,呈V型,键角116.5℃。三个原子以一个O原子为中心,与另外两个O原子分别构成一个非极性共价键;中间O原子提供2个电 子,旁边两个O原子各提供1个电子,构成一个特殊的化学键——三个O原子均等地享有这4个电子。请回答:
子,旁边两个O原子各提供1个电子,构成一个特殊的化学键——三个O原子均等地享有这4个电子。请回答:
 |
| O3的分子结构 |
(1)臭氧与氧气的关系是___________。
(2)选出下列分子与O3分子的结构最相似的的是。
A.H2O B.CO2 C.SO2D.BeCl2
(3)分子中某原子有1对没有跟其他原子共用的价电子叫孤对电子,那么O3分子有___________对孤对电子。
(4)O3分子是否为极性分子___________(是或否)。
(5)O3与O2间的转化是否为氧化还原反应___________(若否 ,请回答A小题;若是,请回答B小题)
,请回答A小题;若是,请回答B小题)
A.O3具有强氧化性,它能氧化PbS为PbSO4而O2不能,试配平:
___________PbS+___________O3——___________PbSO4+___________O2
B.O3在催化剂作用下生成1molO2转移电子数___________mol
PtCl2(NH3)2可以形成两种固体,一种为淡黄色,在水中的溶解度小,另一种为黄绿色,在水中的溶解度较大,请回答下列问题:
⑴PtCl2(NH3)2是平面正方形结构,还是四面体结构
⑵请在以下空格内画出这两种固体分子的几何构型图,
淡黄色固体:,黄绿色固体:
⑶淡黄色固体物质是由分子组成,黄绿色固体物质是由分子组成(填“极性分子”或“非极性分子”)
⑷黄绿色固体在水中溶解度比淡黄色固体大,原因是。
已知A、J为常见金属单质,常温下B为液体化合物,E是空气的主要成分之一,L是蓝色沉淀,H为红棕色气体;它们之间的转换关系如下图所示: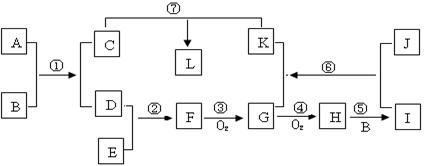
(1)H的化学式是________。
(2)③的化学方程式是__________________________________。
(3)⑥的离子方程式是_______________________________。
(4)F名称是________,检验此气体的方法是___________________________________。