(1)材料是人类赖以生存和发展的重要物质基础。
现有下列材料: A.有机玻璃 B. 普通玻璃 C.石英玻璃
①生产硅酸盐水泥和普通玻璃都需用到的共同原料是 (填化学式)。
②与光导纤维主要成分相同的是 (填字母)。
③属于塑料的是 (填字母)。
(2)保证食品安全、保持营养均衡,是保障人体健康的基础。

①维生素是人体需要的营养物质。右图为某品牌维生素C泡腾片说明书的部分内容。该泡腾片中添加的着色剂是 ,泡腾片溶于水时产生“沸腾”效果,是由于添加的酒石酸和 反应释放出了气体。
② 缺乏某种微量元素将导致甲状腺肿大,该微量元素是 (填字母)。
a. 碘 b.铁 c.钙
③在鸡蛋清溶液中加入饱和硫酸铵溶液有沉淀析出的过程称为 。
④ 使用青霉素可能会产生过敏,在用药前患者一定要进行 。
(3)我国新修订的《环境保护法》,使环境保护有了更严格的法律依据。
①生活中一次性物品的使用会大大增加生态压力,一次性纸巾使用后应投入贴有 (填字母)标志的垃圾桶内。

②漂白粉用于生活用水的杀菌消毒,漂白粉的有效成份是 (填化学式)。治理废水中的重金属污染物可用沉淀法。例如,往含铬(Cr3+)废水中加入石灰乳使Cr3+转变为 (填化学式)沉淀而除去。
③铁器件在潮湿的空气中会发生电化学腐蚀,铁锈的化学式是 发生该腐蚀时的正极反应式为 。
④向煤中加入石灰石作为脱硫剂,可以减少SO2的排放,生成CaSO4,发生的总反应化学方程式为 。
(4分)已知Ba(AlO2)2可溶于水。右图表示的是向KA1(SO4)2溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加入Ba(OH)2的物质的量x的关系。完成下列问题:
(1)a点时反应的离子方程式是
(2)a、b两点消耗Ba(OH)2的物质的量之比是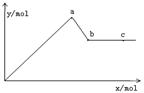
(共13分)关注饮用水,保证人民的生活质量。回答下列两个问题:
(1)饮用水中的NO3— 对人类健康会产生危害,为了降低饮用水中NO3—的浓度,可以在碱性条件下用铝粉将N O3-还原为N2,其化学方程式
O3-还原为N2,其化学方程式 为:
为:
10Al + 6NaNO3 + 4NaOH ="=" 10NaAlO2 + 3N2↑+ 2H2O。请回答下列问题:
①上述反应中,元素的化合价升高,则该元素的原子(填“得到”或“失去”)电子
②用“单线桥法”表示反应中电子转移的方向和数目:
10 Al+ 6 NaNO3 + 4 NaOH ="=" 10 NaAlO2 + 3 N2↑+ 2 H2O
(2)洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。
①工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程式为
。
②漂白粉的有效成分是(填化学式)。
③漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,离子方程式为
 。
。
A、B、C、X均为中学化学常见的物质,它们之间有如下转化关系(副产物已略去)。
试回答: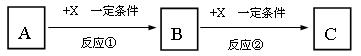
⑴若X是强氧化性单质,则A不可能是_______________。
a.S b.N2 c.Na d.Mg e.Al
⑵若A为强碱溶液,则X可能为________________。
a.AlCl3 b.CO2 c.Al d.Mg e.Al2O3
⑶若X是金属单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,则B的化学式为____________;C溶液在贮存时应加入少量X,理由是(离子方程式表示)。
⑷若A、B、C为含有同一金属元素的无机化合物,X为强电解质,A溶液与C溶液能反应生成B,写出该反应的离子方程式。
(12分)重铬酸钠(Na2Cr2O7)广泛用于合成颜料、媒染剂等。以铬铁矿(主要成分为Cr2O3还含有FeO、Al2O3、SiO2等杂质)为原料制取重铬酸钠的流程图如下: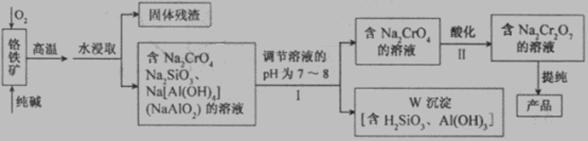 请回答下列问题。
请回答下列问题。
(1)若I中只用一种试剂调节溶液的pH,应选用___________(填标号)。
A.稀硫酸 B.氧化钠固体 C.氢氧化钾溶液
(2)I中,调节溶液pH后,如果溶液的pH过小,可能导致W沉淀部分溶解,原因是
_______________________________________________________ (用离子方程式表示)。
(3)Ⅱ中,Na2CrO4转化为Na2Cr2O7的离子反应如下: 2CrO42- (黄色)+2H+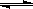 Cr2O72- (橙红色)+H2O
Cr2O72- (橙红色)+H2O
①该反应________氧化还原反应(填“是”或“不是”),反应的平衡常数表达式 K=__________。
②若往Na2Cr2O7溶液(橙红色)中加入足量NaOH固体,溶液_______ (填标号)。
A.变黄色 B.颜色不变 C.橙红色变深
③已知:25℃时,Ag2CrO4的Ksp=1.12×10-12,Ag2Cr2O7的Ksp=2×10-7。25℃时,往Na2Cr2O7溶液中加入AgNO3溶液,最终只生成一种砖红色沉淀,该沉淀的化学式是_____________________。
(12分)Ⅰ、(1)现有浓度均为0.1 mol/L的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵,则①、②、③、④四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号)。
(2)已知某温度下,纯水中的C(H+)=5×10-7mol/L,则此时溶液的C(OH-)为 mol/L;若温度不变,将pH=11的NaOH溶液a L与pH=1的H2SO4的溶液b L混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=2,则a∶b=。
Ⅱ、在一个容积固定的密闭容器中,要求通过调节体系的温度使反应A(g)+2B(g) 2C( g)达到平衡时,保持容器内气体的总物质的量为12mol。现向反应容器中加入6.5molA,xmolB,2.0molC。
2C( g)达到平衡时,保持容器内气体的总物质的量为12mol。现向反应容器中加入6.5molA,xmolB,2.0molC。
⑴若x=5.5时,需要降低体系温度使反应在平衡时达到题设条件,则正反应是热反应。
⑵欲使反应维持向逆反应方向移动,则x的取值范围为。
⑶在一定温度下的上述平衡体系中,另按1∶2的物质的量之比充入D、E两种气体(此时容器中的气体的总物质的量不要求保持12mol),按D(g)+E(g) 2F(g)发生反应。当反应达到平衡时,D在这三种物质的混合体系中的体积分数为p%。若向容器中投入m molD,n molF和一定物质的量的E,在这三种物质的新的平衡体系中,D的体积分数仍为p%,则所投入E的物质的量为(用m、n表示;设A、B、C和D、E、F之间均不发生反应)。
2F(g)发生反应。当反应达到平衡时,D在这三种物质的混合体系中的体积分数为p%。若向容器中投入m molD,n molF和一定物质的量的E,在这三种物质的新的平衡体系中,D的体积分数仍为p%,则所投入E的物质的量为(用m、n表示;设A、B、C和D、E、F之间均不发生反应)。