盐泥是氯碱工业中的废渣,主要成分是镁的硅酸盐和碳酸盐(含少量铁、铝、钙的盐)。实验室以盐泥为原料制取MgSO4•7H2O的实验过程如下:
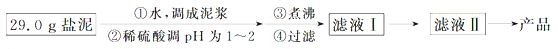
已知:①室温下Ksp[Mg(OH)2]=6.0×10﹣12.②在溶液中,Fe2+、Fe3+、Al3+从开始沉淀到沉淀完全的pH范围依次为7.1~9.6、2.0~3.7、3.1~4.7.③三种化合物的溶解度(S)随温度变化的曲线如图所示.
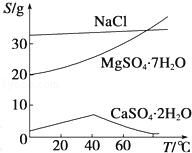
(1)在盐泥中加入稀硫酸调pH为1~2以及煮沸的目的是 ;
(2)若室温下的溶液中Mg2+的浓度为6.0mol•L﹣1,则溶液pH≥ 才可能产生Mg(OH)2沉淀;
(3)由滤液Ⅰ到滤液Ⅱ需先加入NaClO调溶液pH约为5,再趁热过滤,则趁热过滤的目的是 ,滤渣的主要成分是 ;
(4)从滤液Ⅱ中获得MgSO4•7H2O晶体的实验步骤依次为①向滤液Ⅱ中加入 ;②过滤,得沉淀;③ ;④蒸发浓缩,降温结晶;⑤过滤、洗涤得产品;
(5)若获得的MgSO4•7H2O的质量为24.6g,则该盐泥中镁[以Mg(OH)2计]的百分含量约为 (MgSO4•7H2O的相对分子质量为246);
有关物质存在如图所示的转化关系(部分产物已省略)。通常C为气体单质,G为紫黑色固体单质,且受热易升华。实验室中,常用固体E在B的催化下加热制取气体单质H,H能使带火星的木条复燃。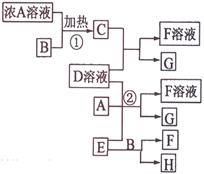
请回答下列问题:
(1)反应①的化学方程式为。
(2)反应②的离子方程式为。
(3)写出另外一种实验室制取H的化学方程式。
(4)已知D溶液与Pb(NO3)2溶液混合可形成沉淀,此沉淀的Ksp=7.0×10—9。若D的浓度为1.0×10—2 mo1/L ,将等体积的D溶液与Pb(NO3)2溶液混合,则生成沉淀所需 Pb(NO3)2溶液的最小浓度为mol/L。
实验室可以用高锰酸钾和浓盐酸反应制取氯气,反应的化学方程式如下:
2KMnO4+16HCl(浓) 2KCl + 2MnCl2 + 5Cl2↑ +8H2O
(1)用单线桥法标出电子转移的方向和数目。
(2)该反应中的氧化剂与还原剂物质的量之比是。
(3)KMnO4的氧化性比Cl2的氧化性(选填“强”或“弱”)。
(4)如反应中转移了2mol电子,则产生的Cl2在标准状况下体积为L。
(5)某同学欲用KMnO4固体配制100 mL0.5mol.L-1的溶液。回答下列问题:
①配制KMnO4溶液时需用的主要仪器有托盘天平、药匙、烧杯、玻璃棒、量筒、 、。
②应用托盘天平称取KMnO4固体g。
③不规范的实验操作会导致实验结果的误差。分析下列操作对实验结果的影响偏小的是(请填序号)。
| A.加水定容时俯视刻度线 |
| B.容量瓶内壁附有水珠而未干燥处理 |
| C.颠倒摇匀后发现凹液面低于刻度线又加水补上 |
| D.在溶解过程中有少量液体溅出烧杯外 |
(15分)有含NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂除去溶液中的NaCl和Na2SO4,从而得到纯净的NaNO3溶液.相应的实验过程可用如图表示:
请回答下列问题: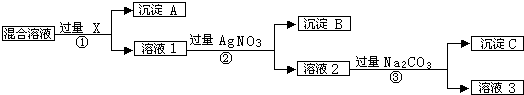
(1)写出实验流程中下列物质化学式:试剂X,沉淀A,沉淀B。
(2)①、②、③过程中均需要过滤,在进行此操作时需要用到的玻璃仪器为:、、。
(3)上述实验流程中加入过量的Na2CO3的目的是。
(4)按此实验方案得到的溶液3中肯定含有Na2CO3杂质;为了解决这个问题,可以向溶液3中加入适量的,之后若要获得固体NaNO3需进行的实验操作是(填操作名称)。
(1)①1.5molH2SO4的质量是____________;
②9.03×1023个氨分子中的质子物质的量是_________;
③标况下,1.92g某气体的体积为672mL,则该气体的摩尔质量为_______________;
④71.5g碳酸钠晶体(Na2CO3·10H2O)溶于水,配成500ml溶液,此溶液的物质的量浓度为______________。
(2)现有①铁片 ②饱和食盐水 ③液态氯化氢 ④乙醇 ⑤干冰 ⑥熔融KNO3⑦BaSO4固体⑧石墨 ⑨苛性钠,其中属于电解质的是_______________,属于非电解质的是__________,能导电的是_____________________
(3)写出下列反应的离子反应方程式:
①少量二氧化碳通入澄清石灰水中:____________________________________________
②向硫酸氢钠溶液中不断加入氢氧化钡溶液至沉淀完全:__________________________
Ⅰ.下表1是常温下几种弱酸的电离平衡常数(Ka)和弱碱的电离平衡常数(Kb),表2是常温下几种难(微)溶物的溶度积常数(Ksp)。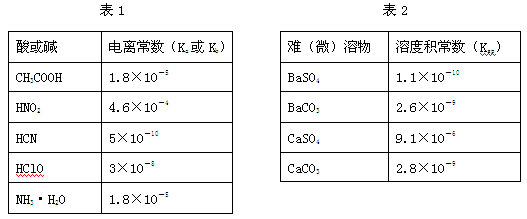
请回答下面问题:
(1)下列能使醋酸溶液中CH3COOH的电离程度增大,而电离常数不变的操作是(填序号)。
| A.升高温度 | B.加水稀释 |
| C.加少量的CH3COONa固体 | D.加少量冰醋酸 |
(2)CH3COONH4的水溶液呈(选填“酸性”、“中性”、“碱性”)。
(3)工业中常将BaSO4转化为BaCO3后,再将其制成各种可溶性的钡盐(如:BaCl2)。具体做法是用饱和的纯碱溶液浸泡BaSO4粉末,并不断补充纯碱,最后BaSO4转化为BaCO3。现有足量的BaSO4悬浊液,在该悬浊液中加纯碱粉末并不断搅拌,为使c(SO42-)达到0.0l mol/L以上,则溶液中c(CO32-)应不低于mol/L。
Ⅱ.化学在能源开发与利用中起着重要的作用,如甲醇、乙醇、二甲醚(CH3OCH3)等都是新型燃料。
(1)乙醇是重要的化工产品和液体燃料,可以利用下列反应制取乙醇。
2CO2(g)+6H2(g) 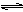 CH3CH2OH(g)+3H2O(g)△H=a kJ/mol
CH3CH2OH(g)+3H2O(g)△H=a kJ/mol
在一定压强下,测得上述反应的实验数据如下表。
根据表中数据分析:
①上述反应的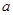 0(填“大于”或“小于”)。
0(填“大于”或“小于”)。
②在一定温度下,提高氢碳(即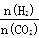 )比,平衡常数K值(填“增大”、“减小”、或“不变”)。
)比,平衡常数K值(填“增大”、“减小”、或“不变”)。
(2)催化剂存在的条件下,在固定容积的密闭容器中投入一定量的CO和H2,同样可制得乙醇(可逆反应)。该反应过程中能量变化如图所示: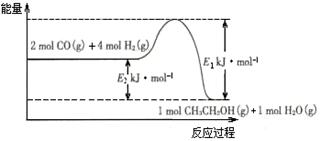
①写出CO和H2制备乙醇的热化学反应方程式。
②在一定温度下,向上述密闭容器中加入1 mol CO、3 mol H2及固体催化剂,使之反应。平衡时,反应产生的热量为Q kJ,若温度不变的条件下,向上述密闭容器中加入4 mol CO、12 mol H2及固体催化剂,平衡时,反应产生的热量为w kJ,则w的范围为。
(3)二甲醚(CH3OCH3)被称为21世纪的新型燃料,具有清洁、高效的优良性能。以二甲醚、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池,其工作原理与甲烷燃料电池原理相类似。该电池中负极上的电极反应式是。