某实验小组设计用50 mL 1.0 mol/L盐酸跟50 mL 1.1 mol/L 氢氧化钠溶液在如 图装置中进行中和反应。在大烧杯底部垫碎泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平。然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过。通过测定反应过程中所放出的热量可计算中和热。试回答下列问题:
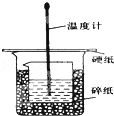
(1)本实验中还缺少一个仪器,其名称是 。
在大小烧杯中填充泡沫塑料的作用是 。
(2)该实验小组做了三次实验,每次取溶液各50 mL,并记录下原始数据(见下表)。
| 实验序号 |
起始温度t1/℃ |
终止温度(t2)/℃ |
温差 (t2-t1)/℃ |
||
| 盐酸 |
NaOH溶液 |
平均值 |
|||
| 1 |
25.1 |
24.9 |
25.0 |
31.6 |
6.6 |
| 2 |
25.1 |
25.1 |
25.1 |
31.8 |
6.7 |
| 3 |
25.1 |
25.1 |
25.1 |
31.9 |
6.8 |
已知盐酸、NaOH溶液密度近似为1.00 g/cm3,中和后混合液的比热容为:c=4.18×10-3kJ/(g·℃),则写出该反应的热化学方程式(离子方程式) (ΔH值保留到小数点后1位)。
(3)若用等浓度的醋酸与NaOH溶液反应,则测得的中和热会比(2)测出的△H____________(填“偏大”、“偏小”或“不变”)。
(4)在中和热测定实验中存在用水洗涤温度计上的盐酸后再用温度计测定NaOH溶液温度的步骤,若无此操作步骤,则测得的中和热ΔH会____________(填“偏大”、“偏小”或“不变”)。
如图所示为实验室制SO2并验证SO2的某些性质的装置图。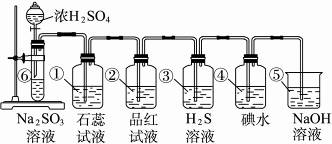
试完成下列问题:
(1)⑥中反应的化学方程式为_____________。
(2)①中的实验现象为_____________,此实验证明SO2是_____________气体。
(3)②中的品红溶液_____________,证明SO2有_____________性。
(4)③中的实验现象是_____________,证明SO2有_____________性。
(5)④中的实验现象是_____________,证明SO2有_____________性。
(6)⑤的作用是_____________,反应的化学方程式是__________________________。
已知浓硫酸与木炭粉在加热条件下会发生剧烈反应:C+2H2SO4(浓) 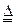 CO2↑+2SO2↑+2H2O↑。试用下图所列各装置设计一个实验,来验证上述反应所产生的各种产物。
CO2↑+2SO2↑+2H2O↑。试用下图所列各装置设计一个实验,来验证上述反应所产生的各种产物。
(1)这些装置的连接顺序(按产物气流从左至右的方向)是(填装置的编号)______→______→______→______。
(2)实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色。A瓶溶液的作用是__________________,B瓶溶液的作用是__________________,C瓶溶液的作用是____________。
(3)装置②中所加的固体药品是______,可验证的产物是______,确定装置②在整套装置中位置的理由是____________。
(4)装置③中所盛溶液是______,可验证的产物是______。
实验室制氨气通常有三种方法:①用固体氢氧化钙和氯化铵反应(装置同课本);②称取7.9 g碳酸氢铵固体放入试管内,再加入8 g氢氧化钠固体,常温下即能产生氨气(装置如下图中甲);③在锥形瓶中注入50 mL浓氨水,再加入10 g氢氧化钠固体(装置如下图中乙)。选取三个250 mL的干燥的烧瓶及瓶塞,用于收集三种制法的氨气。请完成下列问题: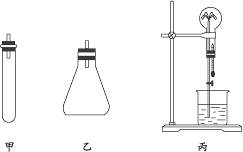
(1)写出用②法制取氨气的化学方程式:__________________________________________。
(2)说明用③法制取氨气的原理:________________________________________________。
(3)检验氨气已收集满的方法:__________________________________________________。
(4)用集满氨气的烧瓶做喷泉实验,装置如图中丙(烧杯内盛酚酞溶液),其现象是_____
_______________________________________________________________________________。
为了测定硫酸铵和氯化铵混合物中氯化铵的质量分数,甲、乙两位同学按下列实验步骤进行实验:称量样品→溶解→加过量试剂A→过滤出现沉淀B→洗涤沉淀→烘干称量→处理实验数据并得出结果。
(1)实验时,甲同学选用硝酸银溶液作试剂A,乙同学选用氯化钡溶液作试剂A,其中同学所选的试剂A不合理,理由是________________。
(2)以下都是在试剂A选择正确时进行的实验:
①为进行称量、溶解、反应、过滤、洗涤沉淀的各项操作,准备了以下仪器:托盘天平与砝码,烧杯、过滤器、铁架台及附件,胶头滴管、量筒,其中还缺少一件必备的仪器是_____________。
②若过滤所得沉淀未经洗涤烘干称量,测得结果将________(填“偏高”或“偏低”)。
③若实验测得混合物的质量为W g,沉淀物的质量为m g,实验测定的氯化铵质量分数计算式=_____________。
Ⅰ.合成氨工业对化学和国防工业具有重要意义。写出氨的两种重要用途_________________________________。
Ⅱ.实验室制备氨气,下列方法中适宜选用的是__________________。
①固态氯化铵加热分解
②固体氢氧化钠中滴加浓氨水
③氯化铵溶液与氢氧化钠溶液共热
④固态氯化铵与氧化钙混合加热
Ⅲ.为了在实验室利用工业原料制备少量氨气,有人设计了如下装置(图119中夹持装置均已略去)。
图1-9
[实验操作]
①检查实验装置的气密性后,关闭弹簧夹a、b、c、d、e。在A中加入锌粒,向长颈漏斗注入一定量稀硫酸。打开弹簧夹c、d、e,则A中有氢气产生。在F出口处收集氢气并检验其纯度。
②关闭弹簧夹c,取下截去底部的细口瓶C,打开弹簧夹a,将氢气经导管B验纯后点燃,然后立即罩上无底细口瓶C,塞紧瓶塞,如图所示。氢气继续在瓶内燃烧,几分钟后火焰熄灭。
③用酒精灯加热反应管E,继续通氢气,待无底细口瓶C内水位下降到液面保持不变时,打开弹簧夹b,无底细口瓶C内气体经D进入反应管E,片刻后F中的溶液变红。
完成下列问题:
(1)检验氢气纯度的目的是___________________________。
(2)C瓶内水位下降到液面保持不变时,A装置内发生的现象是__________________,防止了实验装置中压强过大。此时再打开弹簧夹b的原因是___________________________,C瓶内气体的成分是_________。
(3)在步骤③中,先加热铁触媒的原因是____________________________________。反应管E中发生反应的化学方程式是___________________________。