2011年12月13日,加拿大正式宣布将退出《京都议定书》,这使CO2的排放问题再次成为了热点。当空气中CO2的体积分数超过0.050%时,会引起明显的温室效应。为减小和消除CO2对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对CO2创新利用的研究。
I.最近有科学家提出“绿色自由”构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,在一定条件下与H2反应,使之变为可再生燃料甲醇。其流程如下:
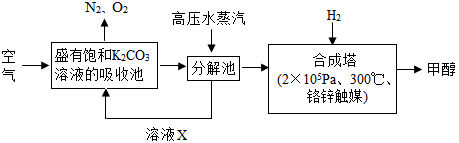
①上述流程中碳酸钾溶液所起的作用是 。
②在分解池中发生的反应为 (写出化学方程式)。
Ⅱ.碳酸钾是重要的无机化工、医药、轻工原料之一,主要用于医药、玻璃、染料等工业, 可用作气体吸附剂,干粉灭火剂,橡胶防老剂等。
已知:CO2、碳酸盐、碳酸氢盐的部分性质如下:
CO2(过量)+OH-=HCO3- HCO3-+OH-=CO32-+H2O
CO32-与H+反应生成CO2分两步:
CO32-+H+=HCO3-;HCO3-+H+=H2O+CO2↑
①小王同学在实验室用如图所示的装置和药品制取K2CO3溶液。
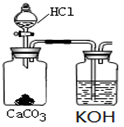
他所制得的溶液中可能含有的杂质是 。
②该同学在数字实验室中用传感器对碳酸钾和碳酸氢钾的混合物样品进行成分测定,他分别称取三份不同质量的混合物样品,配成稀溶液,然后分别逐滴加入相同浓度的50 ml硫酸,测得如下数据:
实验编号 1 2 3
混合物的质量/g 3.76 4.70 8.46
硫酸溶液的体积/mL 50.00 50.00 50.00
生成二氧化碳的物质的量/mol 0.03 0.0375 0.03
试计算:该混合固体中K2CO3与KHCO3的物质的量之比是 所用硫酸的物质的量浓度为 mol•L-1。
(15分).钛白粉(主要成分是TiO2),广泛用于油漆、塑料、造纸等行业,还可用作乙醇脱水、脱氢的催化剂。工业上常以钛矿石(主要成分为FeTiO3(钛酸亚铁),并含FeO、A12O3、 SiO2等杂质)为主要原料经过以下流程制得TiO2,并获得副产品FeSO4·7H2O.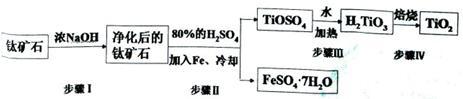
请回答下列问题:
(l)步骤I的目的是
(2)写出步骤Ⅱ中FeTiO3与H2SO4反应的化学方程式 。
(3)步骤II中经过 、 、过滤、洗涤等操作可以得到FeSO4·7H2O.晶体,还可以利用酸化的FeSO4溶液与软锰矿(主要成分为MnO2)反应生产硫酸锰(MnSO4,易溶于水).该反应的离子方程式为
(4)请结合化学用语用化学平衡理论解释步骤III中将TiOSO4转化为H2TiO3的原理:
(5)为测定步骤II后溶液中TiOSO4的含量,首先取待测钛液10 mL加水稀释至100 mL,再加过量铝粉,充分振荡,使其完全反应:3TiO2++Al+6H+=3Ti3++Al3++3H2O。过滤后,取出滤液20.00 mL,以KSCN溶液为指示剂,用0.1000 mol·L-1 NH4Fe(SO4)2溶液滴定至终点,再重复2次,测得平均值为30.00mL。
①该滴定达到终点时的现象
②待测钛液中TiOSO4的物质的量浓度是 。
已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增加。相关信息如下表所示,根据推断回答下列问题:(答题时A、B、C、D、E用所对应的元素符号表示)
| A |
A的最高价氧化物对应的水化物化学式为H2AO3 |
| B |
B元素的第一电离能比同周期相邻两个元素都大 |
| C |
C原子在同周期原子中半径最大(稀有气体除外),其单质焰色为黄色 |
| D |
Z的基态原子最外层电子排布式为3s23p2 |
| E |
E与C位于不同周期,E原子核外最外层电子数与C相同,其余各层电子均充满 |
(1)C在周期表中位于第 周期第 族,E基态原子核外电子排布式是
(2)A、B、D三种元素电负性由大到小排列顺序为 ,其中A的最高价氯化物构成晶体的微粒间作用力为
(3)A和B的最简单氢化物中较稳定的是 (填化学式)。B的最简单氢化物和E的黑色氧化物固体在加热时可反应,写出其反应方程式
(4)E的单质和过氧化氢在稀硫酸中可反应,有人将这个反应设计成原电池,请写出正极反应方程式
(5)煤燃烧产生的烟气中有B的氧化物,会引起严重的环境问题,因此,常用AH4催化还原以消除污染,已知:
① AH4(g)+2 BO2(g)= B2(g)+AO2(g)+2H2O (g) △H1=-867kJ/mol
② 2BO2(g) ⇌B2O4(g) △H2=-56.9 kJ/mol
写出AH4和B2O4反应的热化学方程式
下表中列出五种短周期元素X、Y、Z、W、T的信息。
| 元素 |
相关信息 |
| X |
基态原子最外层电子排布为nsnnpn+1 |
| Y |
其原子L层电子数是K层3倍 |
| Z |
其单质能与冷水剧烈反应,生成的阴阳离子电子数相同 |
| W |
其单质在Y2中燃烧,发出明亮的蓝紫色火焰 |
| T |
其最高正价与最低负价的代数和为6 |
回答下列问题:
(1)Y、Z、W三种元素所形成的简单离子半径由小到大的顺序是(用离子符号表示);T元素的基态原子核外电子排布式为。
(2)X、Z两元素可形成化合物ZX3,其晶体中化学键类型有,晶体类型为。
(3)T元素的最高价氧化物对应水化物的化学式是H2Y的沸点比H2W高的原因是。
(4) Z2 WY3溶液呈性,其原因是(用离子方程式表示)。
(5)已知25℃、101 kPa下:
①2Z(s)+ 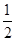 Y2(s)=Z2Y(s)△H1=-414KJ/mol
Y2(s)=Z2Y(s)△H1=-414KJ/mol
②2Z(s)+ Y2(s)=Z2Y2(s)△H1=-511KJ/mol
则1mol Z2 Y2(S)与足量Z(s)反应生成Z2 Y(s)的热化学方程式为。
镧是重要的稀土元素,应用非常广泛,如应用于压电材料、催化剂等领域。
已知:①镧是较活泼金属,在空气中易被氧化;②氢氧化镧是难溶于水的弱碱;
③
| 金属 |
熔点(℃) |
沸点(℃) |
| 钙 |
841 |
1487 |
| 镧 |
920 |
3470 |
(1)操作1、3是相同操作,其名称是。
(2)操作2中要在HCl气体的氛围内加热的原因是。
(3)电解制镧的尾气要用碱液吸收,请写出反应的离子方程式。
(4)真空、高温过程中的反应方程式为。
(5)粗镧精制过程中温度控制范围。
(6)重熔蒸馏制得的镧中仍然混有及少量的钙。某批次产品69.709g,经分析含钙0.209g,该产品的等级为(化工产品等级标准:优级纯≥99.8﹪,分析纯≥99.7﹪,化学纯≥99.5﹪).
X、Y、Z、W是常见的四种短周期元素,其原子序数依次增大。其相关信息如下表:
| 元素 |
相关信息 |
| X |
X的基态原子最外层电子排布式为nsnnpn |
| Y |
Y是空气中含量最高的元素 |
| Z |
Z是地壳中含量最高的金属元素 |
| W |
W的单质是常见的半导体材料 |
(1)Y位于元素周期表的 周期 族,Y与W的气态氢化物较稳定的是(写化学式)
(2)Z的单质与W的单质相比熔点较高的是(写化学式);Z与W原子半径较大的是 (写化学式)
(3)X的一种氧化物XO2分子中σ键与∏键数目之比为
(4)X的第一电离能比W的(填“大”或“小”)
(5)写出X的单质与Y的最高价氧化物水化物的浓溶液在加热的条件下反应的化学方程式:
(6)已知2.7gZ单质与足量Y单质反应,放出31.8kJ的热量,请写出此反应的热化学方程式:。