Al2(SO4)3的电离方程式为 ,17.1g Al2(SO4)3溶于水配成250mL溶液,SO42-的粒子数为 ,Al3+的物质的量浓度为 。
已知有机物A—F具有如下的转化关系。根据要求填空:
(1)A中的含氧官能团有___________________(写名称),A的分子式为______________。
(2)A转化生成B的反应类型是_________________。
(3)C转化生成D的试剂和条件_________________。
(4)F在酸性条件下水解的化学方程式为_________________。
(5)A的同分异构体R,具有如图所示的性质。请写出符合条件的R的同分异构体的结构简式(任写两种)。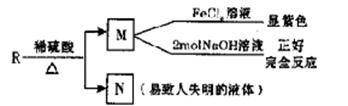
氯化硼(BN)晶体是一种新型无机合成材料。用硼砂(Na2B4O7)和尿素反应可以得到氮化硼:Na2B4O7+ 2CO(NH2)2=4BN+Na2O +4H2O+2CO2↑,根据要求回答下列问题:
(1)组成反应物的所有元素中,第一电离能最大的是___________________。
(2)尿素分子(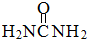 )中
)中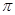 键与
键与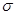 键数目之比为__________;尿素分子中处于同一平面的原子最多有_______个。
键数目之比为__________;尿素分子中处于同一平面的原子最多有_______个。
(3)尿素分子一定条件下形成六角形“超分子”(结构如图)。“超分子”中尿素分子间主要通过什么作用力结合。答:________________(填1种)。
(4)图示“超分子”的纵轴方向有一“通道”。直链烷烃分子刚好能进人通道,并形成“超分子”的包台物;支链烷烃因含有测链,空间体积较大而无法进入“通道”。利用这一性质可以实现直链烷烃和支链烷烃的分离。
①直链烷烃分子能进人通道时,通过什么作用力与“超分子”结合,从而形成 “超分子”包合物?答:___________________。
②下列物质可以通过尿素“超分子”进行分离的是____________。
A.乙烷和丁烷 B.丁烷和异丁烷 C.异戊烷和新戊烷 D氯化钠和氯化钾
(5)BN晶体有a、B两种类型,且a—BN结构与石墨相似、B—BN结构与金刚石相似。
①a一BN晶体中N原子杂化方式是____________________;
②B—BN晶体中,每个硼原予形成________个共价键。这些共价键中,有________个为配位键。
CuCl2溶液中的铜主要以Cu (H2O)42+、CuCl42-形式存在,它们间有如下转化关系:Cu(H2O)42+(蓝色)+4Cl- CuCl42-(黄色)+4H2O;电解不同浓度的CuCl2溶液,均可看做Cu2+、Cl-直接放电。下图为电解浓度较大CuCl2溶液的装置,实验开始后,观察到丙中的KI-淀粉溶液慢慢变蓝。回答下列问题:
CuCl42-(黄色)+4H2O;电解不同浓度的CuCl2溶液,均可看做Cu2+、Cl-直接放电。下图为电解浓度较大CuCl2溶液的装置,实验开始后,观察到丙中的KI-淀粉溶液慢慢变蓝。回答下列问题:
(1)甲电极的电极反应式为_________________。
(2)丙中溶液变蓝是乙电极产物与KI反应导致的,该反应的化学方程式为_________________。
(3)随电解的不断进行,U型管中溶液的颜色变化为__________;
A.由黄色变为浅蓝色 B.由蓝色变为浅黄色
溶液颜色变化的原因是_________________。
(4)当电解到一定程度,甲电极附近出现蓝色Cu(OH) 2絮状物。经测,甲电极附近溶液的pH=a,此时甲电极附近溶液中c(Cu2+)=______ mol·L-1。(已知:Cu(OH) 2的Ksp=2.2×10-20)。
(5)电解较长时间后,丙中溶液的蓝色又会褪去,这是因为乙电极产物进一步将I2氧化为IO3-。该反应的离子方程式为______________。
I.短周期元素X、Y、Z、W在元素周期表中相对位置如图所示,其中Y所处的周期序数与族序数相等。按要求回答下列问题: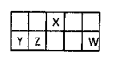
(1)写出X的原子结构示意图_______________。
(2)列举一个事实说明W非金属性强于Z: _______________(用化学方程式表示)。
(3)含Y的某种盐常用作净水剂,其净水原理是__________(用离子方程式表示)。
II.运用所学化学原理,解决下列问题:
(4)已知:Si+2NaOH+H2O=Na2SiO3+2H2。某同学利用单质硅和铁为电极材料设计原电池(NaOH为电解质溶液),该原电池负极的电极反应式为_________________。
(5)已知:①C(s)+ O2(g)=CO2(g) H=a kJ· mol-1;②CO2(g) +C(s)=2CO(g)
H=a kJ· mol-1;②CO2(g) +C(s)=2CO(g)  H=b kJ· mol-1;③Si(s)+ O2(g)=SiO2(s)
H=b kJ· mol-1;③Si(s)+ O2(g)=SiO2(s) H=c kJ· mol-1。工业上生产粗硅的热化学方程式为____________。
H=c kJ· mol-1。工业上生产粗硅的热化学方程式为____________。
(6)已知:CO(g)+H2O(g) H2(g) + CO2(g)。右表为该反应在不同温度时的平衡常数。则:该反应的
H2(g) + CO2(g)。右表为该反应在不同温度时的平衡常数。则:该反应的 H________0(填“<”或“>”);500℃时进行该反应,且CO和H2O起始浓度相等,CO平衡转化率为_________。
H________0(填“<”或“>”);500℃时进行该反应,且CO和H2O起始浓度相等,CO平衡转化率为_________。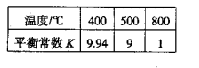
Ⅰ.如图是石油分馏塔的示意图。a、b、c三种馏分中________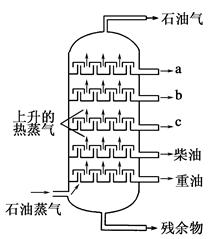
| A.a的沸点最高 |
| B.b的熔点最低 |
| C.c的平均相对分子质量最大 |
| D.每一种馏分都是纯净物 |
Ⅱ.裂化汽油中除含有C6~C11的烷烃外,还含有C5~C11的烯烃及甲苯、二甲苯等苯的同系物。已知甲苯、二甲苯能使酸性KMnO4溶液褪色。要用化学方法检验某裂化汽油样品中含有烯烃及苯的同系物,实验步骤为:
(1)先逐滴加入________,振荡,如果看到______,则证明有________存在。
(2)继续逐滴加入________至________为止,静置,用分液漏斗分出________(填“上”或“下”)层的裂化汽油样品,再加入________振荡,如果看到________,则证明裂化汽油中有________存在。