铁及其化合物在日常生活、生产中应用广泛。
(1)高铁酸钠(Na2FeO4)是水处理过程中的一种新型净水剂,工业上利用NaClO 和NaOH的混合溶液将Fe(OH)3氧化性制备高铁酸钠,反应的离子反应方程式为 ;高铁酸钠能用作新型净水剂的原理是 ;
(2)氧化铁红颜料跟某些油料混合,可以制成防锈油漆。以黄铁矿为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等,用硫酸渣制备铁红(Fe2O3)的过程如下:
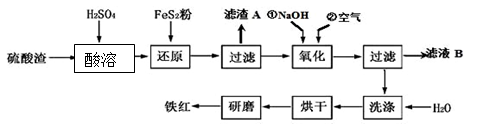
①酸溶过程中发生反应的化学方程式为 , , ;“滤渣A”主要成份的化学式为 。
②还原过程中加入FeS2的目的是将溶液中的Fe3 +还原为Fe2 +,而本身被氧化为H2SO4,请写出该反应的离子方程式 ;
③氧化过程中,O2、NaOH与Fe2+反应的离子方程式为 。
④为了确保铁红的质量和纯度,氧化过程需要调节溶液的pH的范围是 ,
| 沉淀物 |
Fe(OH)3 |
Al(OH)3 |
Fe(OH)2 |
Mg(OH)2 |
| 开始沉淀pH |
2.7 |
3.8 |
7.6 |
9.4 |
| 完全沉淀pH |
3.2 |
5.2 |
9.7 |
12.4 |
如果pH过大,可能引起的后果是 。
X、Y、Z三种元素均为前18号元素,X与Z属于同主族元素,Z元素的焰色反应为黄色。X与Y可形成X2Y和X2Y2两种无色液体,X2Y2在MnO2催化作用下可分解制得氧气和X2Y。Z与Y两单质化合可以得到Z2Y与Z2Y2两种固体化合物,其中Z2Y2为淡黄色固体粉末。Z、Z2Y和Z2Y2都能与X2Y反应生成强碱ZYX溶液。
(1)试推测X、Y所代表的元素分别为XY(填元素符号);
(2)写出Z2Y2的电子式
(3)写出下列化学方程式:X2Y2分解制氧气;
Z单质与X2Y反应;
Z2Y2与X2Y反应。
如图,取一块黄豆大小的金属钠放在石棉网上,用酒精灯预热,待钠熔成球状时,将盛氯气的集气瓶倒扣在钠的上方,钠会在氯气中剧烈燃烧,产生大量白烟,请回答下列问题: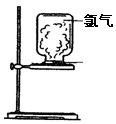
(1)对此反应及现象的描述正确的是
A.此反应为放热反应
B.白烟的生成说明产生了氯化钠分子
C.反应中钠元素被氧化,氯元素被还原。
(2)写出该反应的方程式
(3)用电子式表示氯化钠的形成过程,
(4)检验有Cl-生成,请补充实验步骤(可填满也不可填满)
①倒转集气瓶,加适量蒸馏水
②取少量溶液于试管中。
③加试管中加入。
④有生成则证明有Cl-。
X、Y、Z三种气体都是大气污染物,在工业上通常用碱液吸收。已知X是化石燃料燃烧的产物之一,是造成酸雨的主要物质;Y是一种单质,其水溶液具有漂白性;Z是硝酸工业和汽车尾气的有害物质之一,易溶于水。请写出下列有关反应的化学方程式。
(1)X在一定条件下与氧气反应;
(2)Y与消石灰反应
(3)Z溶于水
目前,汽车尾气已成为许多大城市空气的主要污染源。汽车尾气中含有CO、NO等多种污染物。
(1)汽车燃料中一般不含氮元素,为其中所含的NO是如何产生的?用化学方程式表示:
(2)治理汽车尾气中NO和CO的一种方法是:在汽车的排气管上装一个催化转化装置,使NO与CO反应,生成CO2和N2。反应的化学方程式是
(3)下列措施中,能减少或控制汽车尾气污染有效且可行的是
| A.制定严格的汽车尾气排放标准,并严格执行。 |
| B.开发清洁能源汽车,如氢能汽车、太阳能汽车等。 |
| C.市民出行戴防护面具。 |
| D.市民大量移居城市郊区。 |
(8分)石墨的片层结构如图所示,试完成下列各题: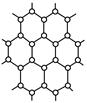
(1)平均________个碳原子构成一个正六边形。
(2)石墨晶体每一层内碳原子数与C—C化学键之比是________。
(3) 石墨层内存在强烈的共价键,层之间存在________,所以石墨兼有原子晶体和分子晶体的特征。