在不同温度下,向V L密闭容器中加入0.5 mol NO和0.5 mol活性炭,发生反应:
2NO(g)+C(s)  N2 (g)+CO2 (g) △H= —Q kJ·mol-1(Q>0),达到平衡时的数据如下:
N2 (g)+CO2 (g) △H= —Q kJ·mol-1(Q>0),达到平衡时的数据如下:
| 温度/℃ |
n (C)/mol |
n(CO2)/mol |
| T1 |
|
0.15 |
| T2 |
0.375 |
|
下列有关说法正确的是
A.由上述信息可推知:T1 > T2
B.T2℃时,若反应达平衡后再缩小容器的体积,c (N2):c (NO)增大
C.T1℃时,若开始时反应物的用量均减小一半,平衡后NO的转化率增大
D.T1℃时,该反应的平衡常数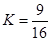
在下述条件下,一定能大量共存的离子组是
A.无色透明的水溶液中:K+、Ba2+、I-、MnO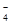 |
B.含有大量NO 的水溶液中:NH 的水溶液中:NH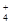 、Fe3+、SO 、Fe3+、SO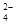 、H+ 、H+ |
C.c(HCO )=0.1 mol·L-1的溶液中:Na+、H+、NO3-、Br- )=0.1 mol·L-1的溶液中:Na+、H+、NO3-、Br- |
| D.强碱性溶液中:Cl-、Fe2+、SO42-、Na+ |
除去Na2CO3固体中少量NaHCO3的最佳方法是
| A.加入适量盐酸 | B.加入NaOH溶液 |
| C.加热 | D.配成溶液后通入CO2 |
下列说法中,错误的是
| A.向Na2SiO3溶液中通入CO2产生白色胶状沉淀 |
| B.NaOH溶液不能存放在磨口玻璃塞的试剂瓶中 |
| C.二氧化硅溶于水生成硅酸 |
| D.二氧化硅是一种熔沸点很高、硬度很大的氧化物 |
氯气是一种化学性质很活泼的非金属单质,它具有较强的氧化性,下列叙述中不正确的是
| A.通常状况下,干燥的氯气能和Fe反应 |
| B.红热的铜丝在氯气里剧烈燃烧,生成棕黄色的烟 |
| C.纯净的H2在Cl2中安静地燃烧,发出苍白色火焰,集气瓶口呈现雾状 |
| D.氯气能与水反应生成HClO和HCl,久置氯水最终变为稀盐酸 |
用NA表示阿伏加德罗常数,下列叙述不正确的是
| A.标准状况下,22.4L H2含有的分子数为 NA |
| B.常温常压下,14g N2含有分子数为0.5NA |
| C.2.3g金属钠做还原剂时失去的电子数为0.1NA |
| D.物质的量浓度为0.5mol /L的MgCl2溶液中,含有Cl-个数为NA |