氯化铁是常见的水处理剂。某氯化铁(FeCl3•6H2O)样品含有少量FeCl2杂质。现要测定其中FeCl3•6H2O的质量分数,实验按以下步骤进行:
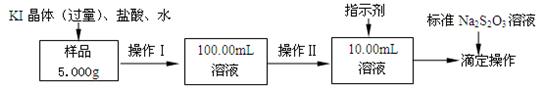
已知有关离子方程式为:2Fe3++2I-═2Fe2++I2,I2+2S2O32-═2I-+S4O62-
(1)取少量氯化铁样品滴入50mL沸水中,加热片刻,液体呈现红褐色,反应的离子方程式为:________________________。
(2)操作I所用到的玻璃仪器除烧杯、玻璃棒外,还必须有________、_________(填仪器名称)。
(3)操作II必须用到的仪器是________(选填编号);
a.50mL烧杯 b.10mL量筒 c.20mL量筒 d.25mL滴定管
指示剂是淀粉溶液,则达到滴定终点的现象是__________________________。
(4)滴定时,消耗浓度为0.1000mol/L的标准Na2S2O3溶液18.00mL。该样品中FeCl3•6H2O(式量为270.5)的质量分数为_____________。
(5)要把样品氯化铁中的少量FeCl2杂质除去,可用的试剂是________(选填编号)。
a.铁粉 b.氯水 c.溴水 d.双氧水
(6)如果采用以下步骤测定氯化铁样品元素的含量,完成下列填空。
①称量样品 ②加水溶解 ③加足量氨水,沉淀 ④过滤 ⑤灼烧 ⑥称量并进行恒重操作。
还缺少的一步操作是________;在过滤前,需要检验是否沉淀完全,其操作___________________;判断是否恒重的标准是_________________________。
(9分)某学生设计了如下实验方法分离NaCl和CaCl2两种固体混合物。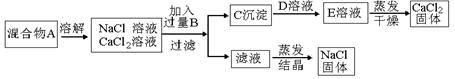
(1)B溶液是,加入过量B溶液的原因是,
反应的离 子方程式是。
子方程式是。
(2)经此实验方法分离得到的NaCl,经分析含有杂质,若要得到纯净的NaCl,还应补充的实验操作步骤是:
(3)若要测定该 混合物中NaCl和CaCl2的质量比,可称量干燥的C沉淀的质量(设为m1)和混合物A的质量(设为m2)来确定
混合物中NaCl和CaCl2的质量比,可称量干燥的C沉淀的质量(设为m1)和混合物A的质量(设为m2)来确定 ,混合物中NaCl和CaCl2的质量比为(用m1、m2表示)
,混合物中NaCl和CaCl2的质量比为(用m1、m2表示)
用98%的浓H2SO4(ρ=1.84g/cm3)配制 240mL0.5mol/L的稀H2SO4,请按要求填空:
(1)请写出该实验的实验步骤
①,②,③,④,⑤。
(2)所用浓H2SO4的物质的量浓度为 ,配制时所需浓硫酸的体积为mL。(均保留一位小数)
(3)实验中需要用到的定量仪器有(包括规格)
(4)若实验中出现下列 现象对所配溶液的浓度有什么影响?(填“偏高”、“偏低”或“无影响”)
现象对所配溶液的浓度有什么影响?(填“偏高”、“偏低”或“无影响”)
①浓硫酸溶解后未冷至室温即进行转移、定容。()
②定容时俯视刻度线。()
(5)若定容时液面高于刻度线应采取的措施是。
(6)若实验操作全部无误,最后所得的溶液应存放在试剂瓶中,并贴上标签,请你帮助把标签上的内容写一下(如右图)。
某同学应用如下所示装置研究物质的性质。其中气体C的主要成分是氯气,还含有少量空气和水蒸气。请回答下列问题: 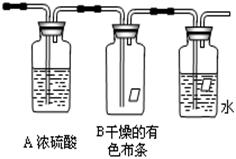
(1)该项研究的主要目的是_______。
(2)浓硫酸的作用是_______________。
(3)观察到的实验现象是___________________
(4)从物 质性质方面来看,这样的实验设计还存在事故隐患,事故表现在__。
质性质方面来看,这样的实验设计还存在事故隐患,事故表现在__。
右图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容。
现用该浓硫酸配制100 mL 1 mol·L-1的稀硫酸。可供选用的仪器有:①胶头滴管;②烧 瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平。请回答下列问题:
(1)盛放浓硫酸的试剂瓶标签上应印有下列警示标记中的▲
(2)配制稀硫酸时,还缺少的仪器 ▲(写仪器名称)
(3)经计算,配制100 mL1 mol·L-1的稀硫酸需要用量筒量取上述浓硫酸的体积为▲mL,量取硫酸时应选用▲mL规格的量筒(填字母番号)
A.10 mLB.50 mLC.100 mLD.200mL
mLD.200mL
(4)在烧杯中稀释浓硫酸的实验操作为▲; 若在稀释过程中,少量浓硫酸不慎沾在手上,处理方法为 ▲。
▲。
(5)对所配制的稀硫酸进行测定,发现其浓度大于1 mol·L-1,配制过程中下列各项操作可能引起该误差的是▲。
A.用量筒量取浓硫酸时,仰视刻度线取浓硫酸
B.容量瓶用蒸馏水洗涤后未干燥,含有少量蒸馏水
C.将稀释后的稀硫酸立即转入容量瓶后,紧接着就进行以后的实验操作
D.转移溶液时,不慎有少量溶液洒到容量瓶外面
E.定容时,俯视容量瓶刻度线进行定容
F.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴 水至刻度处
水至刻度处
我省 自贡盛产食盐,人类与食盐关系密切,食盐在老百姓生活和现代社会的工农业生产中均有重要作用,没有食盐的生活是不可以想象的。粗盐中含有Ca2+、Mg2+、SO42-以及泥沙等杂质,
自贡盛产食盐,人类与食盐关系密切,食盐在老百姓生活和现代社会的工农业生产中均有重要作用,没有食盐的生活是不可以想象的。粗盐中含有Ca2+、Mg2+、SO42-以及泥沙等杂质,
(1)为了除去粗盐中的泥沙,可采用的实验操作方法的名称是____▲____
(2)为了除去可溶性杂质,可以按以下实验步骤进行提纯:①加过量BaCl2溶液;②加过量NaOH溶液;③加过量Na2CO3溶液;④过滤;⑤加适量盐酸。
其中,在步骤③中涉及的离子反应方程式有___▲; ▲。
(3)含碘食盐往往加入KIO3,为了检验实验中是否含KIO3,可以用以下反应进行:
KIO3+5KI+3H2SO4=3I2+3K2SO4+3H2O
为了从反应后的溶液中提取得到纯净的I 2,可采用的实验操作方法的名称是___▲__。
2,可采用的实验操作方法的名称是___▲__。