四氧化三铁在生产和生活中有着广泛的应用,人们工作中常用的打印机、复印 机使用的墨粉主要成分就是 Fe3O4,下图是某企业用氧化沉淀法生产 Fe3O4的工艺流程:
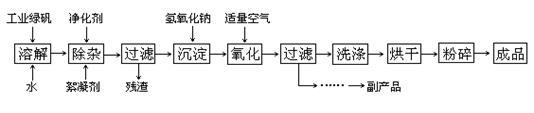
已知:① 工业绿矾中 FeSO4的含量为 52.5%,其中的杂质不参与反应;
②Fe(OH)2+2Fe(OH)3=Fe3O4·4H2O 请回答下列问题:
请回答下列问题
(1)铁的氧化物除Fe3O4·外,还有 。
(2)检验Fe3O4与稀盐酸反应后的溶液中含Fe2+的试剂是 ;
(3)在工艺流程中,通人适量空气“氧化”时的化学方程式是: ;
(4)流程图中所示的副产品的化学式是 ,从过滤所得滤液中提取该副产品需要的操作依次是 (填写序号)。
a.过滤 b.加热浓缩 c.冷却结晶 d.洗涤
( 17分)欲配制1 mol/L的氢氧化钠溶液250mL,
(1)实验室所需的仪器有:,,,,。
(2)完成下列步骤:
①称取氢氧化钠固体克。
②将称好的氢氧化钠固体放入中,加少量蒸馏水将其溶解,待冷却后将溶液沿移入中。
③用少量蒸馏水洗涤次,将洗涤液转移入中,在操作过程中不损失点滴液体,否则会使溶液的浓度偏(高或低)。
④加水定容过程中离刻度线时,改用小心地加水至溶液凹液面与刻度线相切,若加水超过刻度线,会造成溶液浓度偏,应该。
⑤最后盖好瓶盖,,将配好的溶液移入试剂瓶中并贴好标签。
过氧化钠是一种淡黄色固体,在潜水艇中用作制氧剂,供人类呼吸之用。某学生为了验证这一实验,以足量的大理石、足量的盐酸和1.95g过氧化钠样品为原料,制取O2,设计出如下实验装 置:
置:
(1)请写出过氧化钠与二氧化碳反应的化学方程式,并标明电子转移的方向和数目:;
(2)A中制取CO2的装置, 应从下列图①、②、③中选
应从下列图①、②、③中选 哪个图:;
哪个图:;
(3)B装置的作用是 ;
;
(4)为了检验E中收集到的气体,在取出集气瓶后,用的木条伸入集气瓶内,木条会出现;
(5)若E中石灰水出现轻微白色浑浊,请说明原因:;
(6)当D中的1 .95g过氧化钠样品接近反应完毕时,你预测E装置内有
.95g过氧化钠样品接近反应完毕时,你预测E装置内有 何现象?
何现象?
;
(7)反应完毕时,若测得E中的集气瓶收集到的气体为250mL,又知氧气的密度为1.43g/L,当装置的气密性良好的情况下,实际收集 到的氧气体积比理论计算值(大或小),相差约mL(取整数值,所用数据均在标准状况下测定),这是由于
到的氧气体积比理论计算值(大或小),相差约mL(取整数值,所用数据均在标准状况下测定),这是由于 ;
;
选择下列实验方法分离物质,将分离方法的序号填在横线上。
A萃取分液B升华C结晶D分液 E蒸馏 F层析 G过滤
(1)______分离饱和食盐水与沙子的混合物。
(2)______从硝酸钾和氯化钠的混合液中获得硝酸钾。
(3)______分离水和汽油的混合物。
(4)______分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物。
用98%的浓H2SO4(ρ=1.84g/cm3)配制500ml0.5mol/L的稀H2SO4,请按要求填空:
(1)所需浓H2SO4的体积为
(2)如果实验室有10mL、20mL、50mL量筒,应选用mL量筒,实验中还 需要用到的仪器有
需要用到的仪器有
(3)若实验中出现下列现象对所配溶液浓度有什么影响?(填偏高、偏低、无影响)
①浓硫酸溶解后未冷至室温即进行定容
②定容时俯视刻度线
(4)若定容时液面高 于刻度线应采取的措施是
于刻度线应采取的措施是
配制500mL 0.5mol/L的NaOH溶液,试回答下列问题。
(1)需要NaOH固体的质量为。
(2)某同学用托盘天平称量一个小烧杯的质量,称量前把游码放在标尺的零刻度处,天平静止时发现指针在分度盘的偏右位置,此时左边的托盘将(填“高于”或“低于”)右边的托盘,欲使天平平衡,所进行的操作应。假定最终称得小烧杯的质量为(填“32.6g”或“32.61g”)。
(3)配制方法:设计了如下五个操作步骤,正确的顺序是。
①向盛有NaOH的烧杯中加入200mL蒸馏水使其溶解,并冷却至室温。
②继续往容量瓶中加蒸馏水至液面距刻度线1c m~2cm。
m~2cm。
③将NaOH溶液沿玻璃棒注入500mL容量瓶中。
④在烧杯中加入少量的蒸馏水,小心洗涤2~3次后移 入容量
入容量 瓶。
瓶。
⑤改用胶头滴管加蒸馏水至刻度线,加盖摇匀。
(4)某学生实际配制NaOH溶液的浓度为0.48mol/L,原因可能是()
| A.使用滤纸称量氢氧化钠固体 | B.容量瓶中原来存有少量蒸馏水 |
| C.溶解用的烧杯未经多次洗涤 | D.用胶头滴管加水定容时仰视刻度线 |