三氯化碘(ICl3 ,I的化合价为+3价)在药物合成中用途非常广泛,其熔点:33℃,沸点73℃。实验室可用如图装置制取ICl3。
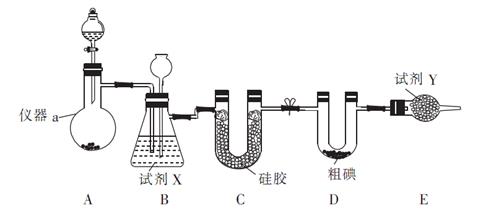
(1)试剂X、Y分别是: 、 。装置E的作用是: 。
(2)制备氯气选用的药品为漂白精固体(主要成分为Ca(ClO)2)和浓盐酸,相关反应的化学方程式为: 。
(3)装置B可用于除杂,也是安全瓶,能监测实验进行时装置C中是否发生堵塞,请写出发生堵塞时B中的现象: 。
(4)氯气与单质碘需在温度稍低于70℃下反应,则装置D适宜的加热方式为 。
(5)某同学欲测定ICl3样品中ICl3的纯度,他准确称取ICl3样品10.0g于烧杯中,加入适量水和过量KI晶体,充分反应:ICl3+3KI=2I2+3KCl(样品中杂质不反应)。将所得溶液配置成100mL待测液。取25.00mL待测液,用2.0mol/L的Na2S2O3标准液滴定(I2+2 S2O32--=2I-+S4O62-),以淀粉溶液作指示剂,达到终点时的现象为: 。重复滴定3次,测得消耗Na2S2O3溶液体积的平均值为20.00mL。该样品中ICl3的质量分数为: 。(ICl3相对分子质量为233.5)
工业上常用铁质容器盛装冷浓硫酸。为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:
[探究一]
(1)第一步:将已去除表面氧化物的铁钉(含少量碳元素)放入冷浓硫酸中,
第二步:10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面
其原因是___________ ______。
(2)另称取铁钉6.0g放入15.0mL浓硫酸中,加热充分反应后得到溶液X并收集到气体Y。取336mL(标准状况)气体Y通入足量溴水中,发生反应:________ _____,然后加入足量 BaCl2溶液,经适当操作后得到干燥固体2.33g。由此推知气体Y中SO2的体积分数为__________________。
[探究二]分析上述实验中SO2体积分数的结果,学习小组同学认为气体Y中还可能含有H2和Q气体。为此设计了下列探究实验装置(图中夹持仪器省略)。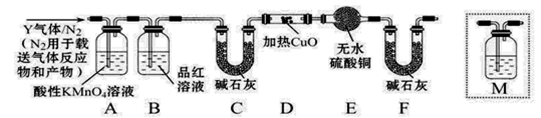
(3)装置B中试剂的作用是____________。
(4)认为气体Y中还含有Q的理由是__________(用化学方程式表示)。
(5)为确认Q的存在,需在装置中添加M于__________(填序号)。
a.A之前 b. A-B间 c.B-C间 d.C-D间
(6)如果气体Y中含有H2,预计实验现象应是_________________ __
硫代硫酸钠是一种重要的化工产品。某兴趣小组拟制备硫代硫酸钠晶体(Na2S2O3·5H2O)。
I.[查阅资料]
(1)Na2S2O3·5H2O是无色透明晶体,易溶于水。其稀溶液与BaCl2溶液混合无沉淀生成。
(2)向Na2CO3和Na2S混合液中通入SO2可制得Na2S2O3,所得产品中常含有少量Na2SO3和Na2SO4。
(3)Na2SO3易被氧化;BaSO3难溶于水,可溶于稀HCl。
Ⅱ.[制备产品]
实验装置如图所示(省略夹持装置)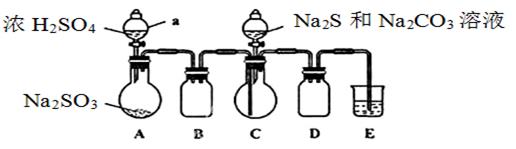
【实验步骤】
①如图示加入试剂。
②先向C中烧瓶加入Na2S和Na2CO3的混合溶液,再向A中烧瓶滴加浓H2SO4。C中发生反应:Na2CO3 + 2Na2S + 4SO2 →3Na2S2O3 + CO2
③待Na2S和Na2CO3完全消耗后,结束反应。C中溶液经一系列的操作可得到Na2S2O3 · 5H2O的粗产品。
(1)仪器a的名称是_________________; E中的试剂可以选用 __ (选填序号)。
a.稀H2SO4 b.NaOH溶液 c.饱和NaHSO3溶液 d.Na2CO3溶液
(2)为验证产品中含有Na2SO3和Na2SO4,该小组设计了以下实验方案:取适量产品配成稀溶液,滴加足量BaCl2溶液,有白色沉淀生成,过滤,用蒸馏水洗涤沉淀,取沉淀,加入足量稀盐酸, (填实验现象),则可确定产品中含有Na2SO3和Na2SO4。
(3)为减少装置C中生成Na2SO4的量,在不改变原有装置的基础上对实验步骤②进行了改进,改进后的操作是 。
Ⅱ.已知:I2+2S2O32-==2I-+S4O62-。某学生测定食用精制盐的碘含量,其步骤为:
a.准确称取w g食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉溶液为指示剂,逐滴加入物质的量浓度为2.0×10-3 mol/L的Na2S2O3溶液10.0 mL,恰好反应完全。
(4)根据以上实验和包装袋说明,所测精制盐的碘含量是 mg/kg。(以含w的代数式表示)
某研究性学习小组选用以下装置进行实验设计和探究(图中a、b、c均为止水夹)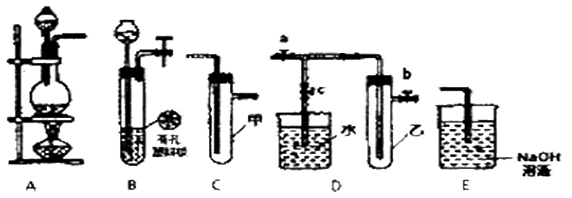
(1)在进行气体制备时,应先检验装置的气密性。将A装置末端导管密封后,在A装置的分液斗内装一定量的蒸馏水,然后 _________ ____________________ ,则证明A装置的气密性良好。
(2)用锌粒和稀硫酸制备H2时应选用装置____作为发生装置(填所选装置的序号字母),夹紧止水夹 后反应会慢慢停止下来,请描述原因 _________________ ______________________ 。
(3)某同学利用上述装置设计实验证明Cl2氧化性强于Br2
①选用的装置连接顺序为:()→()→()(填所选装置的序号字母);
②从以下试剂中选用该实验所需的试剂为 (填试剂的序号字母);
a.浓硫酸 b.浓盐酸 c.二氧化锰 d.氯化钠 e.溴化钠溶液
③实验过程中能说明Cl2氧化性强于Br2的实验现象是 ____________ ;
(4)另一同学将B、D、E装置连接后,在B装置中加入铜片和浓硝酸制取NO2,然后进行NO2气体与水反应的实验,并观察相关现象:
①B装置发生反应的离子方程式为____________________________________;
②反应一段时间后D装置中的具支试管乙中收集满NO2气体,若进行NO2气体与水反应的实验,应_______________________(填“对a、b、c三个止水夹进行的操作”),然后再适当加热 ,实验现象为___________________________________________。
我国废水三级排放标准规定:废水中苯酚的含量不得超过1.00mg/L。实验室可用一定浓度的溴水测定某废水中苯酚的含量,其原理如下: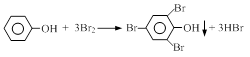
(1)请完成相应的实验步骤:
步骤1:准确量取25.00mL待测废水于250mL锥形瓶中。
步骤2:将5.0 mL 0.01mol/L溴水迅速加入到锥形瓶中,塞紧瓶塞,振荡。
步骤3:打开瓶塞,向锥形瓶中加入过量的0.1mol/L KI溶液,振荡。
步骤4: ,再用0.01 mol/L Na2S2O3标准溶液滴定至终点,消耗 Na2S2O3溶液8.50 mL。(反应原理:I2 + 2Na2S2O3 =" 2NaI" + Na2S4O6)
(2)该废水中苯酚的含量为 mg/L。
(3)步骤2塞紧瓶塞的原因是 。
(4)步骤3若振荡时间过长,则测得的废水中苯酚的含量 (填“偏高”、“偏低”或“无影响”,下同)。步骤4中若滴定至终点时滴定管尖嘴处出现气泡,而滴定前无气泡,会使测得的废水中苯酚的含量 。
某小组同学为比较酸性条件下ClO-、S、Fe3+的氧化性强弱,设计如下实验(夹持仪器已略去)。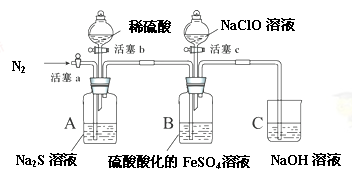
实验步骤及现象记录如下(每步操作进行前均通一段时间N2,排出装置内原有气体。):
1、打开活塞c,向装置B滴加次氯酸钠溶液,溶液立即变为黄色,一段时间后观察到装置B中液面上方出现黄绿色气体时,立即关闭活塞c。
2、用注射器取出少量装置B中的溶液,滴加几滴KSCN溶液,溶液变为血红色。
3、打开活塞b,向装置A中加入足量稀硫酸后,关闭活塞b,观察到装置B中溶液变浑浊。
4、一段时间后,用注射器取出少量装置B中的上层清液,……
请回答下列问题:
(1)在添加药品前需进行的操作是 。
(2) 步骤1中,发生反应的离子方程式是 , 。
(3)步骤3中导致浑浊的物质是 。
(4) 步骤4是为了验证该溶液中存在的金属阳离子只有Fe2+。甲同学认为后续操作应是滴加酸性KMnO4溶液,但乙同学认为该方法不妥,原因是 ;合理的操作及实验现象应该是 。
(5)分析实验现象,可得出该实验的结论是 。