向FeI2,FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示。已知:2Fe2++Br2===2Fe3++2Br-,2Fe3++2I-===2Fe2++I2。则下列有关说法中,不正确的是( )。
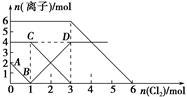
| A.线段BD表示Fe3+物质的量的变化 |
| B.原混合溶液中FeI2的物质的量为1mol |
| C.当通入2 mol Cl2时,溶液中已发生的离子反应可表示为2Fe2++2I-+2Cl2===2Fe3++I2+4Cl- |
| D.原溶液中:n(Fe2+)∶n(I-)∶n(Br-)=2∶3∶1 |
氮的某氧化物中,氮元素与氧元素的质量比为7:20,此氧化物中氮的化合价为()
| A.+1 | B.+2 | C.+3 | D.+5 |
常温下,能用铝制容器盛放的是()
| A.浓硝酸 | B.稀硫酸 | C.稀硝酸 | D.浓盐酸 |
试管中盛有少量白色固体,可能是铵盐,检验的办法是()
| A.加水,将湿润的红色石蕊试纸放在试管口 |
| B.加NaOH溶液,加热,滴入紫色石蕊试剂 |
| C.加NaOH溶液,加热,滴入酚酞试剂 |
| D.加NaOH溶液,加热,将湿润的红色石蕊试纸放在试管口 |
下列气体中,不属于污染性气体的是()
| A.NO | B.NO2 | C.NH3 | D.CO2 |
下列反应中,熵显著增加的反应是()
| A.CO(g)+2H2(g)=CH3OH(g) |
| B.CaCO3+2HCl=CaCl2+H2O+CO2↑ |
| C.C(s)+O2(g)=CO2(g) |
| D.2HgO(s)=2Hg(l)+O2(g) |