【化学—选修2:化学与技术】
金属钒素有“合金维生素”之称,普通钢中加入少量的钒(V)能极大地改善钢的弹性和强度。工业上回收废钒催化剂(含有V2O5、VOSO4、K2SO4、SiO2)中的钒的主要流程如下:
回答下列问题:
(1)滤渣l的主要成分是________________;
(2)步骤②中发生反应的离子方程式为________________;
(3)步骤③的变化过程可简化为(HA表示有机萃取剂)
VOSO4+(水层)+2HA2(有机层) VOA2(有机层)+H2SO4(水层),则步骤④中可选择硫酸作萃取剂的原因是________________;萃取和反萃取在实验室里用到的玻璃仪器有______和_____;
VOA2(有机层)+H2SO4(水层),则步骤④中可选择硫酸作萃取剂的原因是________________;萃取和反萃取在实验室里用到的玻璃仪器有______和_____;
(4)该工艺流程中,可以循环利用的物质除了氨气以外,还有____________;
(5)调节溶液pH,可将(VO2)SO4转变成NH4VO3沉淀;25℃时,当PH为1.7~1.8时,钒沉淀率为98.8%;假设其它各步反应都完全进行,已知KC1O3的还原产物是KCl,若每消耗1moiKC1O3,理论上可回收金属钒___________g(计算结果保留一位小数)。
图8-3是某气体X产生并研究其性质的装置。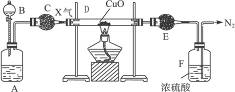
图8-3
A中盛有微溶的白色固体,B中盛有无色挥发性液体,C和E中盛有干燥剂。A和B中物质相遇时有无色气体X生成,它经图中一系列装置在末端得到N2,且E管的质量增加。
(1)写出盛放试剂的名称:
A.____________,B.____________,C.____________,E.____________。
(2)A和B中物质相遇生成X的主要原因是:________________________。
(3)D中反应的化学方程式_________________________________________。
(4)F中反应的化学方程式_________________________________________。
(5)从D中反应说明气体X具有____________(填“酸性”“碱性”“氧化性”或“还原性”)。
某研究性学习小组对氨气的制法进行了如下设计:
(1)下面是该小组同学提出的实验室制备氨气的几种方案:
A.硝酸铵固体与氢氧化钠固体共热
B.加热分解NH4Cl晶体
C.将浓氨水逐滴加到新制的生石灰中
你认为其中较为简便易行的方案有_______________(填写字母);其反应的化学方程式为__________________________________。
请从上图的仪器中选择制取氨气的发生装置(要求仪器少、合理)__________(写编号)。
(2)该小组需收集干燥后的氨气:
①如选用如右图所示的装置,则气体应由导管口_______(填“X”或“Y”)导入(集气瓶不能颠倒)。
②若用排液集气法收集氨气,可选用的试剂是_______(填字母)
A.H2O B.浓H2SO4C.CCl4 D.NaCl饱和溶液
(3)用图示装置进行喷泉实验,上部烧瓶已装满干燥氨气,引发水上喷的操作是___________
________________________。
(4)若原烧瓶中氨气是充满的,进行喷泉实验后,烧瓶内溶液中溶质的物质的量浓度为_________(假定在标准状况下)。
A是一种白色晶体,它与浓NaOH溶液共热,放出无色气体B。用圆底烧瓶收集干燥的B,按图8-2所示装置仪器,挤压滴管的胶头时,可以得到蓝色喷泉;A与浓H2SO4反应,放出无色气体C。用圆底烧瓶收集干燥的C,仍按图所示装置仪器,挤压滴管的胶头时,可以得到红色喷泉。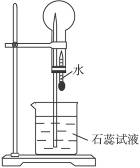
图8-2
(1)A的化学式是_____________________________。
(2)可用于除去B中水分的干燥剂是_____________。收集气体B的方法是_______________。
(3)收集气体C的方法是________________________________________________________。
资料显示:“氨气可在纯氧中安静燃烧……”某校化学小组学生设计如下装置(图中铁夹等夹持装置已略去)进行氨气与氧气在不同条件下反应的实验。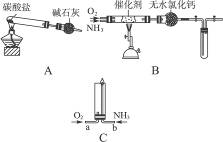
(1)用装置A制取纯净、干燥的氨气,大试管内碳酸盐的化学式是________________;碱石灰的作用是___________________________________。
(2)将产生的氨气与过量的氧气通到装置B(催化剂为铂石棉)中,用酒精喷灯加热:
①氨催化氧化的化学方程式是_________________________________,试管内气体变为红棕色,该反应的化学方程式是______________________________________。
②停止反应后,立即关闭B中两个活塞。一段时间后,将试管浸入冰水中,试管内气体颜色变浅,请结合化学方程式说明原因____________________________________________ 。
(3)将过量的氧气与A产生的氨气分别从a、b两管进气口通入到装置C中,并在b管上端点燃氨气:
①两气体通入的先后顺序是______________,其理由是________________________;
②氨气燃烧的化学方程式是______________________________________________。
大气压对许多物理实验和化学实验有着重要影响。
下图是喷泉实验的装置图(图中夹持装置均已略去)。
(1)实验室制取氨气的化学方程式是_______________。
(2)收集氨气应使用_________法,要得到干燥的氨气时用__________作干燥剂。
(3)用图甲装置进行喷泉实验,上部烧瓶已装满干燥的氨气,引发水上喷的操作是_________。该实验的原理是___________。
(4)如果只提供如图乙的装置,请说明引发喷泉的方法。