(1)硫酸的摩尔质量是 ,24.5g硫酸中所含的氧原子数目为 ,48g的氧气在标准状况下的体积是 。
(2)0.2 mol Al2(SO4)3中含有n(Al3+) _______mol,m(SO42-)_________g。某硫酸钠溶液中含有3.01×1022个Na+,则该溶液中SO42-的物质的量是n(SO42-)______ mol,该溶液中Na2SO4的质量为___________克。
(3)同温同压下的N2和H2,若体积相同时,两种气体的质量比为 ,其密度比为 ;若质量相等时,两种气体的体积比 。
合成氨是人类科学技术发展史上一项重大突破,解决了地球上因粮食不足而导致的饥饿和死亡问题。氨可用于工业上制硝酸,其中的一步反应的化学方程式为: 其中还原剂是_____________(填化学式),若有68g NH3参加反应,转移电子的物质的量为_________mol。
其中还原剂是_____________(填化学式),若有68g NH3参加反应,转移电子的物质的量为_________mol。
除杂提纯下列各物质,请写出所选化学试剂的化学式及反应的离子方程式。
| 混合物成分 |
化学试剂 |
离子方程式 |
| Na2SO4中含有少量Na2CO3杂质 |
||
| FeCl2中含有少量FeCl3杂质 |
||
| NaNO3中含有少量NaCl杂质 |
1932年美国化学家鲍林首先提出了电负性的概念。电负性(用X表示)也是元素的一种重要性质,下表给出的是原子序数小于20的16种元素的电负性数值: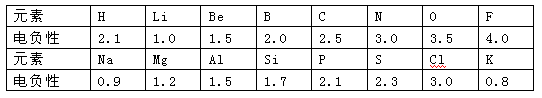
请仔细分析,回答下列有关问题:
①预测周期表中电负性最大的元素应为_____;估计钙元素的电负性的取值范围:< X <。
②根据表中的所给数据分析,同主族内的不同元素X的值变化的规律是
;简述元素电负性X的大小与元素金属性、非金属性之间的关系。
③经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键。试推断AlBr3中形成的化学键的类型为。
在A、B、C、D四种元素中,A为地壳这含量最多的元素;B的单质在气体中密度最小;C元素的原子失去两个电子后,其电子层结构和氩原子相同;D元素的原子核外有三个能层,各能层电子数之比为1:4:1。
(1)写出上述四种元素的名称:A、B、C、
(2)写出C2+离子的电子排布式
(3)指出A、B、C三种元素中所形成的化合物中所包含化学键的类型
(10分)第一电离能I1是指气态原子X(g)处于基态时,失去一个电子成为气态阳离子X+(g)所需的能量。下图是部分元素原子的第一电离能I1随原子序数变化的曲线图(其中12号至17号元素的有关数据缺失)。
请回答以下问题:
(1)认真分析上图中同周期元素第一电离能的变化规律,推断Na~Ar元素中,Al的第一电离能的大小(最小)范围为________<Al<________(填元素符号)。
(2)从上图分析可知,同一主族元素原子的第一电离能I1变化规律是________。
(3)上图中第一电离能最小的元素在周期表中的位置是________。
(4)根据对角线规则,Be、Al元素最高氧化物的水化物性质相似,它们都具有________,