某化学反应2A  B+D在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
B+D在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
| 实验 序号 |
时 间 浓度 温度 |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
| 1 |
800℃ |
1.0 |
0.80 |
0.67 |
0.57 |
0.50 |
0.50 |
0.50 |
| 2 |
800℃ |
c2 |
0.60 |
0.50 |
0.50 |
0.50 |
0.50 |
0.50 |
| 3 |
800℃ |
c3 |
0.92 |
0.75 |
0.63 |
0.60 |
0.60 |
0.60 |
| 4 |
820℃ |
1.0 |
0.40 |
0.25 |
0.20 |
0.20 |
0.20 |
0.20 |
根据上述数据,完成下列填空:
(1)在实验1,反应在10至20分钟时间内平均速率为 mol/(L·min)。
(2)在实验2,A的初始浓度c2=____________mol/L,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是___________。
(3)设实验3的反应速率为v3,实验1的反应速率为v1,则v3_______v1(填>、=、<),且c3_______1.0 mol/L(填>、=、<)。
(4)比较实验4和实验1,可推测该反应是________反应(选填吸热、放热)。理由是
金属钠保存在中。
下列金属中,遇到盐酸或强碱溶液都能放出氢气的是
| A.Al | B.Mg | C.Fe | D.Cu |
(14分)根据下图所示装置回答问题: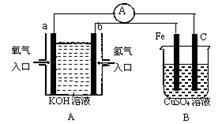
(1)装置A中a电极的电极反应式为,b电极的电极反应式为;
(2)装置B中C为极,电极反应式为。
(3)当铁电极的质量变化为19.2g时,a极上消耗O2在标准状况下的体积为L。
(4)当装置A中消耗0.05mol氢气时,装置B中溶液的pH为。(溶液体积为100mL不变)
(5)若将装置B改为电解精炼铜,则粗铜作极,另一极反应为。
(10分)碳、氮和铝的单质及其化合物在工农业生产和生活中有重要作用。
(1)真空碳热还原氯化法可实现由铝矿制备金属铝,其相关的热化学方程式如下:
①2Al2O3(s)+ 2AlCl3(g)+ 6C(s)=6AlCl(g)+ 6CO(g) △H=a kJ•mol-1
②3AlCl(g)= 2Al(l)+ AlCl3(g) △H=b kJ•mol-1
反应Al2O3(s)+ 3C(s)=2Al(l)+ 3CO(g)的△H=kJ•mol-1(用含a、b的代数式表示)。
(2)用活性炭还原法可以处理氮氧化物。某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应C(s)+ 2NO(g)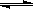 N2(g)+ CO2(g) △H="Q" kJ•mol-1。在T1℃时,反应进行到不同时间测得各物质的浓度如下:
N2(g)+ CO2(g) △H="Q" kJ•mol-1。在T1℃时,反应进行到不同时间测得各物质的浓度如下:
 时间(min) 时间(min)浓度 (mol/L) |
0 |
10 |
20 |
30 |
40 |
50 |
| NO |
1.00 |
0.68 |
0.50 |
0.50 |
0.60 |
0.60 |
| N2 |
0 |
0.16 |
0.25 |
0.25 |
0.30 |
0.30 |
| CO2 |
0 |
0.16 |
0.25 |
0.25 |
0.30 |
0.30 |
①T1℃时,该反应的平衡常数K=
②30min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是(填字母编号)
a.通入一定量的NOb.加入一定量的活性炭
c.加入合适的催化剂 d.适当缩小容器的体积
③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为3:1:1,则Q0(填“>”或“<”)。
④在恒容绝热条件下,能判断该反应一定达到化学平衡状态的依据是
a.单位时间内生成2nmolNO(g)的同时消耗nmolCO2(g)
b.反应体系的温度不再发生改变
c.混合气体的密度不再发生改变
(12分)已知二元酸H2A在水中存在以下电离:H2A===H++HA-,HA- H++A2-。试回答下列问题:
H++A2-。试回答下列问题:
(1)NaHA溶液呈__ _(填“酸”“碱”或“中”)性,理由是。
(2)某温度下,向10 mL、0.1 mol·L-1 NaHA溶液中加入0.1 mol·L-1 KOH溶液V mL至中性,此时溶液中以下关系一定正确的是(填字母)。
| A.溶液pH=7 | B.水的离子积Kw=c2(OH-) |
| C.V>10 | D.c(K+) =c(Na+) |
(3)已知难溶物CaA在水中存在溶解平衡:CaA(s) Ca2+(aq)+A2-(aq) ΔH>0。一定温度下向浊液中通入HCl气体,c(Ca2+)(填“减小”、“增大”或“不变”),原因是。
Ca2+(aq)+A2-(aq) ΔH>0。一定温度下向浊液中通入HCl气体,c(Ca2+)(填“减小”、“增大”或“不变”),原因是。
(4)测得25℃时,CaA的Ksp为2.0×10-11。常温下将10gCaA固体投入110mLCaCl2溶液中,充分搅拌后仍有固体剩余,测得溶液中c(Ca2+)=0.08 mol·L-1,则溶液中c(A2-)=。