某小组同学为比较酸性条件下NO3-、SO42-、Fe3+的氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验)。

实验记录如下:
| |
实验操作 |
实验现象 |
| I |
打开活塞c,将过量稀HNO3加入装置B中,关闭活塞c |
B中浅绿色溶液立即变为深棕色;一段时间后,溶液最终变为黄色。 |
| II |
用注射器取出少量B装置中的溶液,加入KSCN溶液 |
溶液变为红色。 |
| III |
打开活塞b,向A装置中加入足量硫酸,关闭活塞b |
A中产生气体;B中有气泡,液面上有少量红棕色气体生成。 |
| IV |
一段时间后,用注射器取出少量B装置中的溶液,…… |
…… |
| V |
打开活塞a,通入一段时间空气 |
———— |
请回答下列问题:
(1)保存Fe(NO3)2溶液时,常加入铁粉,目的是(用化学方程式表示)________。
(2)实验I中,发生反应的离子方程式是________。
(3)资料表明,Fe2+能与NO结合形成深棕色物质[Fe(NO)]2+: Fe2+ + NO [Fe(NO)]2+
[Fe(NO)]2+
用平衡移动原理解释实验I中溶液由深棕色变为黄色的原因是________________________。
(4)分析实验现象,同学们得出了结论。则:
① 实验IV的后续操作是________________,观察到的现象是________________。
② 由实验得出的结论是_______________________。
(5)实验反思
① 实验操作V的目的是_______________________________________。
② 实验操作III,开始时B中溶液的颜色并无明显变化,此时溶液中发生反应的离子方程式是________。
③ 有同学认为装置中的空气会干扰实验结论的得出,应在实验前通一段时间的氮气。你是否同意该看法,理由是________________________________________。
为测定乙炔的相对分子质量,某小组利用下图所示装置进行试验(夹持仪器已略去,气密性已检验)。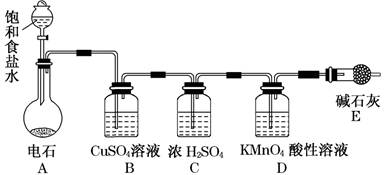
(1)小组查阅资料得出:乙炔能与硫酸酸化的KMnO4反应生成Mn2+和CO2,该反应的化学方程式是。
(2)在装置A中使用饱和食盐水而不直接滴加水的原因。
(3)B中的CuSO4溶液用于除去乙炔中混有的H2S、PH3、AsH3等气体,CuSO4溶液除H2S气体的反应类型是(基本反应)。
(4)实验前D中含有x mol KMnO4的酸性溶液,实验时向D中通入一定量的乙炔直至KMnO4酸性溶液恰好完全褪色,实验完毕后装置D及E的总质量共增重y g,通过计算求出所测乙炔的相对分子质量(用含字母x、y的代数式表示):__________(不写计算过程)。
(5)若该小组的实验原理及所有操作都正确,下列因素中,对所测乙炔相对分子质量的值不会产生影响的是________。
A.将装置A中产生的混合气体直接通入D中的KMnO4酸性溶液
B.将E装置(盛有碱石灰的干燥管)换成盛有浓硫酸的洗气瓶
C.通入过量纯净的乙炔气体于KMnO4酸性溶液时,有部分乙炔未被氧化而逸出
(6)另一活动小组的同学认为上述实验装置仍存在不足,则改进的措施是______________。
某学生应用下图所示的装置来研究物质的性质,其中气体X的主要成分是氯气,杂质是空气和水蒸气。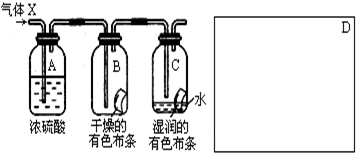
回答下列问题:
(1)该项研究(实验)的主要目的是。
(2)浓H2SO4的作用是,
与研究目的直接相关的实验现象是______________________________________。
(3)该实验装置设计上存在的缺陷为 _________________ ,
请在上图的D处画出能克服该缺陷的装置。
(14分)高锰酸钾俗称PP粉,为强氧化剂,遇到有机物就放出活性氧。这种氧有杀灭细菌的作用,且杀菌能力极强。某学生欲在实验室配制1 L 0.06 mol/L KMnO4稀溶液,用来清洗伤口。
(1)实验过程中需用托盘天平称取KMnO4晶体的质量为__________g。
(2)其操作步骤如下图所示,则右图所示操作应在下图中__________(填选项字母)之间。
A.②与③ B.①与② C.④与⑤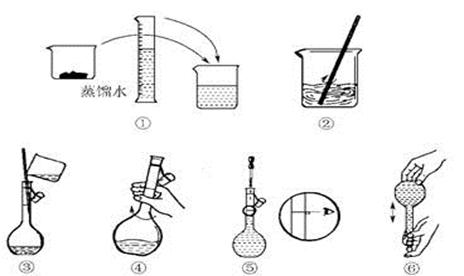
(3) 配制过程中需要用到的仪器有:托盘天平、药匙、烧杯、、、
(4)若该同学在配制溶液时,进行了如下操作,其中使所配溶液浓度偏低的操作
有_______________(填选项字母)。
A.称量KMnO4晶体时,指针偏向右边
B.将KMnO4晶体放在烧杯中溶解,冷却后,转移至含有少量蒸馏水的容量瓶中
C.定容时,仰视刻度线
D.振荡摇匀后,发现溶液液面低于刻度线,再滴加少量蒸馏水至刻度线处
盐酸、硝酸都是用途相当广泛的两种酸。
(1)瑞典科家舍勒在研究软锰矿(主要成份为MnO2)时,将浓盐酸与软锰矿混合加热,产生了一种有刺激性气味的有色气体。写出该反应的化学方程式,并标出电子转移方向和数目: 。
(2)某校合作学习探究小组学习科学家探究精神对氯气性质进行了探究,设计了以下一些实验。
| 实验内容 |
实验现象 |
|
| A |
收集一集气瓶气体,观察颜色,然后向瓶内倒入约占瓶容积1/5的蒸馏水,充分振荡。 |
蒸馏水呈浅黄绿色,瓶内气体仍呈黄绿色。 |
| B |
取出瓶内部分溶液,滴入紫色石蕊试液中直至过量。 |
紫色石蕊试液先变红色,后红色褪色。 |
| C |
取出瓶内剩下的部分溶液,滴入硝酸银溶液中。 |
产生大量白色沉淀 |
| D |
最后向瓶内倒入少量浓氢氧化钠溶液,振荡。 |
瓶内黄绿色气体立即消失。 |
①能说明氯气与水发生化学反应的实验是(填实验序号)
②写出实验D中所发生反应的离子方程式。
(3)该校另一合作学习探究小组用下列左图所示装置对铜与硝酸反应进行探究。
①甲同学观察到试管中的气体由无色变成了红棕色,由此认为试管里的硝酸是浓硝酸,你认为他的看法正确吗?。为什么?。
甲同学还能观察到的现象有。
②乙同学向反应完成后的溶液里滴加氢氧化钠溶液,产生的沉淀(m/g)和加入溶液的体积(V/mL)的关系如上右图所示。请写出O-A段反应的离子方程式 。
为研究某铁质材料与浓硫酸反应生成气体的成分,某学习小组进行了以下探究活动:
(1)称取铁钉5.6g放入20mL足量浓硫酸中,加热,理论上收集到气体SO2L(标况)。将所得气体全部通入足量溴水中,然后加入足量BaCl2溶液,经适当操作后得干燥固体23.3g。由此推知实际生成气体SO2的体积为L(标况)。
(2)分析上述实验中SO2体积的结果,有同学认为所得气体中除含有 SO2外,还可能含有H2和Q气体。为此设计了下
SO2外,还可能含有H2和Q气体。为此设计了下 列探究实验装置(图中夹持仪器省略)。
列探究实验装置(图中夹持仪器省略)。
①装置A中试剂的作用是
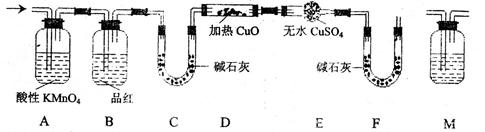
②认为气体中还含有的Q气体是
③为确认Q的存在,需在装置中添加M于,
a.A之前 b.AB之间 c.BC之间 d.CD之间
M中的试剂是
④如果气体中含有H2,预计实验现象应是