甲烷作为一种新能源在化工领域应用广泛,请回答下列问题:

(1)高炉冶铁过程中,甲烷在催化反应室中产生水煤气(CO和H2)还原氧化铁,有关反应为:CH4(g)+CO2(g)===2CO(g)+2H2(g) ;ΔH=+260 kJ·mol-1
已知:2CO(g)+O2(g)===2CO2(g) ;ΔH=﹣566 kJ·mol-1
则CH4与O2反应生成CO和H2的热化学方程式为: _____________________.
(2)如下图所示,装置Ⅰ为甲烷燃料电池(电解质溶液为KOH溶液),通过装置Ⅱ实现铁棒上镀铜。
①a处应通入_____(填“CH4”或“O2”),b处电极上发生的电极反应式是:
②电镀结束后,装置Ⅰ中溶液的pH值_____(填写“变大”“变小”或“不变”,下同),装置Ⅱ中Cu2+的物质的量浓度 .
③电镀结束后,装置Ⅰ溶液中的阴离子除了OH―以外还含有_____(忽略水解).
④在此过程中若完全反应,装置Ⅱ中阴极质量变化为12.8 g,则装置Ⅰ中理论上消耗甲烷_______L(标准状况下).
电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀。Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用。阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用。
某科研小组用电浮选凝聚法处理污水,设计装置如下图所示: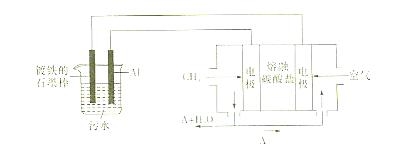
(1)实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,无法使悬浮物形成浮渣。此时,应向污水中加入适量的。
a.H2SO4b.BaSO4c.Na2SO4 d.NaoH e.CH3CH2OH
(2)电解池阳极的电极反应分别是①;②。
(3)电极反应①和②的生成物反应得到Fe(OH)3沉淀的离子方程式是:。
(4)熔融盐燃料电池是以熔融碳酸盐为电解质,以CH4为燃料,空气为氧化剂,稀土金属材料为电极。已知负极的电极反应式为:CH4+4CO32—8e-5CO2+2H2O。
①正极的电极反应是。
②为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定。为此电池工作时必须有部分A物质参加循环。则A物质的化学式是。
(5)实 验过程中,若在阴极产生了44.8L(标准状况)气体,则熔融盐燃料电池消耗CH4(标准状况)L。
验过程中,若在阴极产生了44.8L(标准状况)气体,则熔融盐燃料电池消耗CH4(标准状况)L。
X、Y、Z、W为含有相同电子数的分子或离子,均由原子序数小于10的元素组成,X有5个原子核。通常状况下,W为无色液体。
已知:X+Y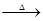 Z+W
Z+W
(1)Z的空间构型为。
(2)液态Z和W的电离相似,都可电离出电子数相同的两种离子,液态Z的电离方程式是。
(3)1mol气态Z与O2反应生成液态W和一种由两种元素组成的气体物质,放出的热量为QkJ,写出该反应的热化学方程式:。
(4)一定温度下,将1mol N2O4置于密闭容器中,保持压强不变,升高温度至T1的过程中,气体由无色逐渐变为红棕色。温度由T1继续升高到T2的过程中,气体逐渐变为无色。若保持T2,增大压强,气体逐渐变为红棕色。气体的物质的量n随温度T变化的关系如图所示。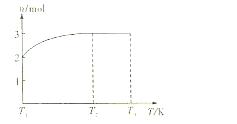
①温度在T1—T2之间,反应的化学方程式是:。
②温度在T2—T3之间,气体的平均相对分子质量是(保留1位小数)。
③若将实验所得的平衡 混和气体通入足量的水中,欲使气体被完全吸收则至少应同时通入标准状况下的空气L。(设空气组成为:N2与O2,体积比4:1)
混和气体通入足量的水中,欲使气体被完全吸收则至少应同时通入标准状况下的空气L。(设空气组成为:N2与O2,体积比4:1)
高炉炼铁中发生的基本反应如下:FeO(s)+CO(g)s Fe(s)+CO2(g)△H>0。
Fe(s)+CO2(g)△H>0。
(1)下列可以作为判断该反应已经达到化学平衡状态依据的是。
a.高炉内压强不变
b.CO2的生成速率和CO的生成速率相等
c.混合气体中CO2的浓度不变
d.c(CO2)=c(CO)
(2)此反应的平衡常数表达式为K=。
(3)温度升高平衡常数K值(填“增大”“减小”、或“不变”)。
(4)已知1100℃时,K=0.263,此时测得高炉中c(CO2)="0.025mol/L" ·c(CO)=0.1mol/L,在这种情况下,该反应是否处于化学平衡状态(填“是”或“否”),此时化学反应速率是
 (填“<”、“>”或“=”),其原因是。
(填“<”、“>”或“=”),其原因是。
A、B、C、D、E是短周期元素组成的中学常见的物质,它们的转化关系如图所示(部分产物和反应条件略去)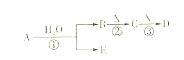
(1)若D为白色胶状难溶物,且与A摩尔质量相等,则反应③的离子方程式为:。
(2)若A为CO,则D的化学式为。
(3)若C为当今需要减排的一种常见的温室气体,E为一种弱酸,则A的化学式为。
(10分)有A、B、C、D、E五种常见化合物,都是由下表中的离子形成的:
| 阳离子 |
K+ Na+ Cu2+ Al3+ |
| 阴离子 |
SO42— HCO3— NO3— OH— |
为了鉴别上述化合物。分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,只有B、C为紫色(透过蓝色钻玻璃);
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中产生
白色沉淀;
⑤将B、D两溶液混合,未见沉淀或气体生成.
根据上述实验填空:
(1)写出B、D的化学式:B,D 。
(2)将含1molA的溶液与含1molE的溶液反应后蒸干,仅得到一种化合物,该化合物的化学式为。
(3)在A溶液中加少入量澄清石灰水,其离子方程式为。
(4)C常用作净水剂,用离子方程式表示其净水原理。