硫酸铅(PbSO4)广泛应用于制造铅蓄电池、白色颜料等。利用方铅矿精矿(PbS)直接制备硫酸铅粉末的流程如下:

已知:(ⅰ)PbCl2(s)+2Cl-(aq) PbCl42-(aq) △H>0
PbCl42-(aq) △H>0
(ⅱ)Ksp(PbSO4)=1.08×10-8, Ksp(PbCl2)=1.6×10-5
(ⅲ)Fe3+、Pb2+以氢氧化物形式完全沉淀时,溶液的PH值分别为3.2、7.04
(1)步骤Ⅰ中生成PbCl2和S的离子方程式 ,加入盐酸的另一个目的是为了控制PH值在0.5~1.0,原因是 。
(2)用化学平衡移动的原理解释步骤Ⅱ中使用冰水浴的原因 。
(3)写出PbCl2晶体转化为PbSO4沉淀的离子方程式 。
(4)请用离子方程式解释加入H2O2后滤液2可循环利用的原因 ,滤液3是 。
(5)铅蓄电池的电解液是硫酸,充电后两个电极上沉积的PbSO4分别转化为PbO2和Pb,充电时阴极的电极反应式为 。
目前上海大部分城市居民所使用的燃料主要是管道煤气,浦东新区居民开始使用东海天然气作为民用燃料,管道煤气的主要成分是CO、H2和少量烃类,天然气的主要成分是CH4,它们的燃烧反应如下: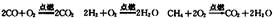
根据以上化学方程式判断,燃烧相同体积的管道煤气和天然气,消耗空气体积较大的是(1)____________,因此燃烧管道煤气的灶具如许改烧天然气,灶具的改进方法是(2)_____进风口(填“增大”或“减小”),如不改进可能产生的不良后果是(3)_____________________________________________________。
管道煤气中含有的烃类,除甲烷外还有少量乙烷、丙烷、丁烷等他们的某些性质见下表:
| 乙烷 |
丙烷 |
丁烷 |
|
| 熔点/℃ |
-183.3 |
-189.7 |
-138.4 |
| 沸点/℃ |
-88.6 |
-42.1 |
-0.5 |
试根据以上某个关键数据解释冬天严寒季节有时管道煤气火焰很小,并且呈断续状态的原因是_______________________________________________________________
(每空2分,共16分)
A、B、C、D、E、X 都是短周期元素组成的常见无机物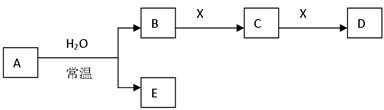
根据上框图关系,完成下列问题:
(1)A可作漂白剂,X是含有某种阳离子(此阳离子具有净水作用)的溶液,且M(A)=M(D),
则A与H2O反应的化学方程式为,C转化成D的离子方程式为
(2)A的 某种合金可作原子反应堆的导热剂,X是非极性分子的化合物,则A与H2O反应的离子方程式为,C转化成D的化学方程式为
某种合金可作原子反应堆的导热剂,X是非极性分子的化合物,则A与H2O反应的离子方程式为,C转化成D的化学方程式为
(3)A是单质,X是Na2CO3溶液,E可用消毒剂,则A与H2O反应的离子方程式为
,
(4)A是单质,X是单质(它的同素异形体是原子晶体),则E与SiO2反应的化学方程式为
(5)A是化合物,X是O2,C转化成D还需要催化剂,E具有两性,则A与H2O反应的化学方程式为
(6)A是化合物(Mr(A)=100),X是O2,B转化成C还需要催化剂,E是中强碱,则A
与H2O反应的化学方程式为
(每空3分,共15分)根据下框图关系,完成下列问题: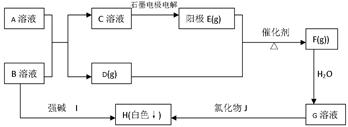
H(白色↓)不溶于盐酸,A、B都是酸式盐。
(1)工业生产D的典型设备是,工业生产F选择的条件是
(2)石墨电极电解C溶液时阳极的电极方程式是
(3)B溶液中加入I溶液反应恰好显中性时的离子方程式为
(4)B溶液与A溶液反应的离子方程式为
(每小题3分,共15分)
(1)实验室制取氯气反应的离子方程式为
(2)工业上制取漂白粉反应的化学方程式为
(3)配平:KClO3+H2C2O4+H2SO4 → K2SO4+ClO2↑+CO2↑+H2O
(4)二氧化碳气体通过一定量的过氧化钠固体,固体增重2.8g时,放出热量为Q KJ
则此反应的热化学方程式为
(5)标况下3.136 L Cl2通入0.1 L FeBr2溶液中,测得溶液Br-中消耗了三分之二,则此时总反应的离子方程式为
在密闭容器中,使2molN2和6molH2混合发生下列反应:
N2(g)+3H2(g)===2NH3(g)(正反应为放热反应)
(1)当反应达到平衡时,N2和H2的浓度比是_______;N2和H2的转化率比是_________。
(2)升高平衡体系的温度(保持体积不变),混和气体的平均相对分子质量_______,密度________。(填“变大”、“变小”或“不变” )
(3)当达到平衡时,将C(N2)、C(H2)、C(NH3)同时减小一倍,平衡将向______移动。
(4)当达到平衡时,充入氩气,并保持压强不变,平衡将向_________移动。
(5)若容器恒容,绝热、加热使容器内温度迅速升至原来的2倍,平衡将_______
(填“向左移动”“向右移动”或“不移动”)。达到新平衡后,容器内温度_______(填“大于”“小于”或“等于”)原来的2倍。