在氮的单质和化合物中,遇到HCl会产生白烟的是 (用字母填空);与氢氧化钙加热发生反应产生刺激性气味气体的是 (用字母填空)。
| A.氮气 | B.氨气 | C.硝酸钠 | D.氯化铵 |
现有属于前四周期的A、B、C、D、E、F、G七种元素,原子序数依次增大。A元素的价电子构型为nsnnpn+1;C元素为最活泼的非金属元素,D元素核外有三个电子层,最外层电子数是核外电子总数的1/6;E元素正三价离子的3d轨道为半充满状态,F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子;G元素与A元素位于同一主族,其某种氧化物有剧毒。
(1)A元素的第一电离能 B,元素的电负性由小到大的顺序为一电离能(填“<”“>”或“=”),A、B、C三种元素 (用元素符号表示)。
(2)D元素原子的价电子排布式是 。
(3)C元素的电子排布图为 ;E3+的离子符号为 。
(4)F元素位于元素周期表的 区,其基态原子的电子排布式为 。
(5)G元素可能的性质 。
A.其单质可作为半导体材料 B.其电负性大于磷 C.最高价氧化物对应的水化物是强酸
(10分)下表中实线是元素周期表的部分边界,其中上边界并未用实线画出。
根据信息回答下列问题:
(1)基态Ga原子的最外层电子排布式为_________________
(2)铁元素位于元素周期表的__________区;Fe和CO易形成配合物Fe(CO)5,在Fe(CO)5中铁的化合价为__________。
(3)已知:原子数目和价电子总数均相同的微粒互为等电子体,等电子体具有相似的结构特征。与CO互为等电子体的分子和离子分别为__________和__________(填化学式)。
(4)在CH4、CO、CH3OH中,碳原子采取sp3杂化的分子有__________。
(5)根据VSEPR模型预测ED4-的空间构型为__________。B、C、D、E原子相互化合形成的分子中,所有原子都满足最外层8电子稳定结构的分子为__________(写2种)。
(9分)钛已作为常用金属铁、铝后的第三金属,我国钛矿储量丰富,对它的应用研究是目前科学研究的前沿课题之一。
(1)请写出铝原子的基态电子排布式:________。
(2)X+、Y2-、Z-与Al3+具有相同的电子层结构,则下列说法正确的是________。
| A.元素第一电离能:X>Al |
| B.电负性:Z>Y |
| C.氢化物稳定性:H2Y>HZ |
| D.H2Y中Y的杂化类型是sp3,键角小于109.5° |
(3)某钙钛型复合氧化物晶胞结构如图①所示,以A原子为晶胞顶点,A位可以是Ca、Sr、Ba或Pb,当B位是V、Cr、Ti、Fe时,这种化合物具有磁电阻效应。该钙钛型复合氧化物的化学式为________。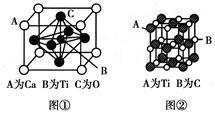
(4)最近发现钛(Ti)原子和碳原子可构成气态团簇分子,分子模型如图②所示。该气态团簇分子的分子式为________,它属于________晶体,其主要物理性质有________(写出两点即可)。
如图所示是一些晶体的结构,它们分别是NaCl、CsCl、干冰、金刚石、石墨结构中的某一种的某一部分。
(1)其中代表金刚石的是(填写编号字母,下同) ,其中每个碳原子与 个碳原子最接近且距离相等。
(2)其中代表石墨的是 ,其中每个正六边形占有的碳原子数平均为 个。
(3)其中表示NaCl的是 ,每个钠离子周围与它最接近且距离相等的氯离子有 个,每个钠离子周围与它最接近且距离相等的钠离子有 个,每个氯离子周围紧邻的钠离子相连接而成的空间几何体为 。
(4)代表CsCl的是 ,它属于 晶体,每个铯离子与 个氯离子紧邻.
下图中X是一种具有水果香味的合成香料,A是直链有机物,E与FeCl3溶液作用显紫色。请根据上述信息回答:
请回答下列问题:
(1)H中含氧官能团的名称是 。B→I的反应类型为 。
(2)只用一种试剂鉴别D、E、H,该试剂是 。
(3)D和F反应生成X的化学方程式为 。