天津港“8.12”爆炸事故中,因爆炸冲击导致氰化钠泄漏,可以通过喷洒双氧水或硫代硫酸钠溶液来处理,以减轻污染。
资料:氰化钠化学式NaCN(C元素+2价,N元素-3价),白色结晶颗粒、易潮解、有微弱的苦杏仁气味、剧毒、易溶于水、易水解生成氰化氢、水溶液呈碱性。
(1)氰化钠(NaCN)溶液呈碱性,其原因是____________(用离子方程式解释)。
(2)“8.12”爆炸事故后,当地政府组织群众用双氧水喷洒,用双氧水处理NaCN产生一种酸式盐和一种能使湿润红色石蕊试纸变蓝的气体,写出该反应的化学方程式____ 。
某化学兴趣小组在实验室制备硫代硫酸钠,并检测用硫代硫酸钠溶液处理后的氰化钠废水能否达标排放。
【实验一】实验室通过如右图所示装置制备Na2S2O3。

(3)右图a装置中盛装Na2SO3
固体的仪器名称是______________;
b装置的作用是________________。
(4)装置c中的产物有Na2S2O3和C02气体等,实验结束后,装置d中的溶质有NaOH、Na2CO3,还可能有________________________。
(5)实验结束后,在e处最好连接盛______________(选填“NaOH溶液”、“水”、“CCl4”中任一种)的注射器,再关闭K2打开K1,防止拆除装置时污染空气。
【实验二】测定用硫代硫酸钠溶液处理后的废水中氰化钠的含量。已知:
①废水中氰化钠的最高排放标准为0.50 mg/L。
② AgI呈黄色,且CN -优先与Ag+反应。
AgI呈黄色,且CN -优先与Ag+反应。
实验如下:
取25.00 mL处理后的氰化钠废水于锥形瓶中并滴加几滴KI溶液作指示剂,用1.000 ×10-4 mol/L的标准AgNO3溶液滴定,消耗AgNO3溶液的体积为2.50 mL。
(6)滴定终点的判断方法是_______________。
(7)处理后的废水中氰化钠的含量为_____________mg/L。
(一)在配制物体的量浓度溶液时,下列操作出现的后果是(填: “偏低”、“偏高”、“无影响”):
(1)配制氢氧化钠溶液时,称取已吸潮的氢氧化钠固体。
(2)配制氯化钠溶液时,容量瓶中有少量水。。
(3)发现溶液液面超过刻度线,用吸管吸出少量水,使液面降至刻度线。。
(二)实验室常用标准NaOH溶液测定未知盐酸溶液的浓度。
(1)配制0.5mol·L-1NaOH溶液250mL所需的玻璃仪器为。
(2)用滴定管准确量取20.00毫升未知浓度盐酸于锥形瓶中,加入酚酞作指示剂,用NaOH溶液滴定到终点。
某学生进行了三次实验,实验数据如下表:
| 实验编号 |
盐酸体积( mL ) |
标准NaOH溶液的体积(mL) |
| 1 |
20.00 |
18.20 |
| 2 |
17.10 |
|
| 3 |
16.90 |
滴定中误差较大的是第_____次实验,造成这种误差的可能原因是_______________。
A.滴定管在装标准NaOH溶液前未润洗
B.滴定开始前装标准NaOH溶液滴定管尖嘴部分有气泡,滴定终点读数时未发现气泡
C.滴定开始前装标准NaOH溶液的滴定管尖嘴部分没有气泡,在滴定终点读数时发现尖嘴部分有气泡
D.在装未知浓度盐酸前锥形瓶里面有少量水,未烘干
E.达到滴定终点时,俯视溶液凹液面最低点读数
F.滴定过程中,锥形瓶摇荡得太剧烈,以至有些液滴飞溅出来
G.滴定到终点时,溶液颜色由无色变到了红色
(3)该同学所测得盐酸溶液的物质的量浓度为___________(结果保留三位小数)。
实验室常用加热铵盐和碱的固体混合物的方法制取氨气。
根据下图回答问题: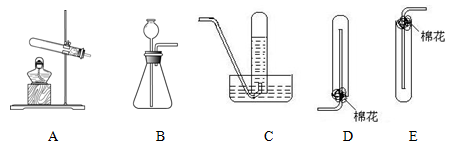
(1)实验室制取氨气的发生装置为(填序号),该反应的化学方程式为。
(2)下列气体可以用与氨气相同的收集装置收集的是(填序号)。
A. H2 B. CO2
氯气是一种化学性质活泼的气体。
⑴氯气是一种具有气味的气体,密度比空气的(填“大”或“小”),若采用图中装置收集氯气,则氯气应由管(填“A”或“B”)通入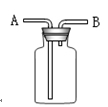
⑵氯气与NaOH溶液反应的化学方程式为,该反应可用于工业上制取漂白液,其有效成分是。
(11分)在浓CaCl2溶液中通入NH3和CO2,可以制得纳米级碳酸钙(粒子直径在1~100nm之间)。下图所示A~E为实验室常见的仪器装置(部分固定夹持装置略去),请根据要求回答问题。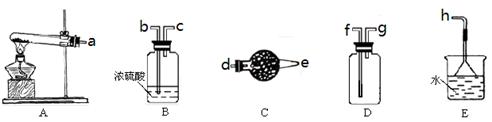
(1)实验室制取、收集干燥的NH3,需选用上述仪器装置的接口连接顺序是(选填字母):a接,接,接h;
用A装置制取NH3的化学反应方程式为
(2)用下图所示装置也可以制取NH3,则圆底烧瓶中的固体可以选用(选填字母编号);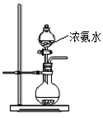
| A.碱石灰 | B.生石灰 | C.无水氯化钙 | D.无水硫酸铜 E、烧碱 |
(3)向浓CaCl2溶液中通入NH3和CO2气体制纳米级碳酸钙时,应先通入的气体是,试写出制纳米级碳酸钙的化学方程式;
(4)试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级
MnO2是一种重要的无机功能材料,粗MnO2的提纯是工业生产的重要环节。某研究性学习小组设计了将粗MnO2(含有较多的MnO和MnCO3)样品转化为纯MnO2的实验,其流程如下: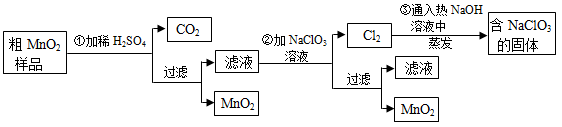
(1)第①步加稀H2SO4时,粗MnO2样品中的(写化学式)转化为可溶性物质。
(2)第②步反应的离子方程式是:
+ClO3—+=MnO2↓+Cl2↑+。
(3)第③步蒸发操作必需的仪器有铁架台(含铁圈)、、、玻璃棒。
(4)若粗MnO2样品的质量为12.69g,第①步反应后,经过滤得到8.7g MnO2,并收集到0、224LCO2(标准状况下),则在第①步反应中至少需要mol H2SO4。
(已知摩尔质量:MnO2 -87g/mol; MnO-71g/mol; MnCO3-115 g/mol)