氮元素在海洋中的循环,是整个海洋生态系统的基础和关键。海洋中无机氮的循环过程可用下图表示。

(1)海洋中的氮循环起始于氮的固定,其中属于固氮作用的一步是 (填图中数字序号)。
(2)下列关于海洋氮循环的说法正确的是 (填字母序号)。
a.海洋中存在游离态的氮
b.海洋中的氮循环起始于氮的氧化
c.海洋中的反硝化作用一定有氧气的参与
d.向海洋排放含NO3-的废水会影响海洋中NH4+的含量
(3)有氧时,在硝化细菌作用下,NH4+可实现过程④的转化,将过程④的离子方程式补充完整:
________NH4+ + 5O2== 2NO2- + ________H+ +__________+__________
(4)有人研究了温度对海洋硝化细菌去除氨氮效果的影响,下表为对10 L人工海水样本的监测数据:
| 温度/℃ |
样本氨氮含量/mg |
处理24 h |
处理48 h |
| 氨氮含量/mg |
氨氮含量/mg |
||
| 20 |
1008 |
838 |
788 |
| 25 |
1008 |
757 |
468 |
| 30 |
1008 |
798 |
600 |
| 40 |
1008 |
977 |
910 |
硝化细菌去除氨氮的最佳反应温度是 ,在最佳反应温度时,48 h内去除氨氮反应的平均速率是 mg·L-1·h-1。
(5)为了避免含氮废水对海洋氮循环系统的影响,需经处理后排放。右图是间接氧化工业废水中氨氮(NH4+)的示意图。

① 结合电极反应式简述间接氧化法去除氨氮的原理: 。
② 若生成H2和N2的物质的量之比为3:1,则处理后废水的pH将 (填“增大”、“不变”或“减小”),请简述理由: 。
有一固体混合物,可能由Na2CO3、Na2SO4、CuSO4、CaCl2、NaCl等混合而成,为检验它们,做了以下实验:
①将固体混合物溶于水中,搅拌后得无色透明溶液;②往此溶液中滴加硝酸钡溶液,有白色沉淀产生;③过滤,将沉淀物置于稀硝酸中,发现沉淀全部溶解。
根据上述实验事实,回答下列问题:
(1)原固体混合物中一定含有的物质是,一定不含有的物质是,可能含有的物质是(以上空格均填写化学式)。对可能含有的物质,可采用向滤液中滴加溶液的方法来检验。
(2)写出步骤③中的离子方程式。
随着生活水平的提高,人们越来越关注自身的健康。以下是探讨化学物质与人体健康的有关问题:
(1)微量元素与人体健康密切相关。为此,我国启动了多项工程,帮助居民补充微量元素,预防疾病。例如为了解决问题启动了“酱油加铁”工程。
(2)我国居民在平时的饮食中应多吃碱性食物。下列属于碱性食物的是(填“肉类”、“鸡蛋”或“水果”)。
(3)服用药物时要对症下药。胃舒平(主要成分Al(OH)3)可治疗胃酸过多,离子方程式为__________
(4)现有下列五种物质
| A.食盐 | B.食醋 | C.苹果汁 | D.葡萄糖 |
E.青霉素,F.阿司匹林请按下列要求填空(填序号)。
富含维生素C的是;可直接进入血液,补充能量的是;应用最广泛的抗生素之一的是;既可作为调味剂,又可作为防腐剂的是;食用过多会引起血压升高、肾脏受损的,使用最早的解热镇痛药。
(5)①明矾是一种混凝剂,净水的原理是(离子方程式);
②汽车尾气中的CO、NO在催化剂的作用下发生反应,转化为两种无毒气体。请写出该反应的化学方程式
③蛋白质遇到酸、碱、重金属盐、乙醇等化学物质时会发生凝结,失去原来的活性,这个变化称为。
(6)钢铁的生产与使用是人类文明和生活进步的一个重要标志。
①炒过菜的铁锅未及时洗净(残液中含NaCl),第二天便会因腐蚀出现红褐色锈斑。试回答:铁锅的腐蚀主要是由腐蚀造成的。铁锅锈蚀的负极反应式为。
②为防止轮船的船体在海水中腐蚀,一般在船身连接(填“锌块”或“铜块”)。
在溶液中,反应A+2B C分别在三种不同实验条件下进行,它们的起始浓度均为
C分别在三种不同实验条件下进行,它们的起始浓度均为 、
、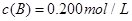 及
及 。反应物A的浓度随时间的变化如下图所示。
。反应物A的浓度随时间的变化如下图所示。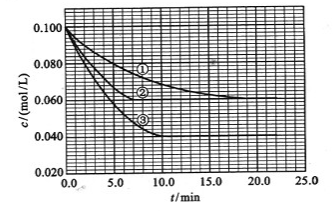
请回答下列问题:
(1)与①比较,②和③分别仅改变一种反应条件。所改变的条件和判断的理由是:
②_______________;
③_______________;
(2)实验②平衡时B的转化率为_________;实验③平衡时C的浓度为____________。
已知A、B、C、D、E五种物质中均为含有A元素,它们之间有如图所示转化关系,若A为气态非金属单质,按下列要求写出化学方程式
① Cu与E的浓溶液反应 : ______________________________
② A→C:______________________________
③ B→C: ______________________________
④ B和E反应: ____________________________
在高温下,下列反应达到平衡:
C(s)+ H2O(g) CO(g)+H2(g)(正反应为吸热反应)
CO(g)+H2(g)(正反应为吸热反应)
(1)如果升高温度,平衡向_______反应方向移动(填正或逆);
(2)如果增大压强,H2的体积分数将_______(填增大、减小或不变);
(3)如果通入水蒸汽,平衡向_______反应方向移动(填正或逆);
(4)如果加入焦炭,H2O的转化率将______(填增大、减小或不变)。