硫铁矿烧渣(主要成分Fe2O3、Fe3O4、FeO、SiO2等)是工业生产硫酸的废渣,利用硫铁矿烧渣制备铁红等产品的流程如下图所示:
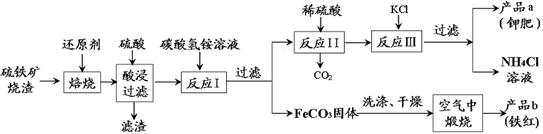
(1)硫铁矿烧渣焙烧时所添加的还原剂最有可能的是 。(填字母)
A.铝 B.锌 C.碳
(2)酸浸、过滤后滤液中的主要成分是 。
(3)反应Ⅰ的反应温度一般需控制在35℃以下,其目的是 。
(4)空气中煅烧FeCO3生成产品b的化学反应方程式为 。
(5)检验产品a中是否含有氯化物杂质的实验操作是:取少量产品a于试管中配成溶液, 。
[化学——选修2化学与技术]
(1)我国某地区已探明蕴藏有丰富的赤铁矿(主要成分为Fe2O3,还含有SiO2等杂质)、煤矿、石灰石和黏土。拟在该地区建设大型炼铁厂。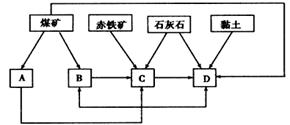
①随着铁矿的开发和炼铁厂的建立,需要在该地区相应建立焦化厂、发电厂、水泥厂等,形成规模的工业体系。据此确定图中相应工厂的名称:
| A.________, | B.________, | C.________, | D.________; |
②以赤铁矿为原料,写出高炉炼铁中得到生铁和产生炉渣的化学方程式:______________。
(2)玻璃钢可由酚醛树脂和玻璃纤维制成。
①酚醛树脂由酚醛和甲醛缩聚而成,反应有大量热放出,为防止温度过高,应向有苯酚的反应釜________地加入甲醛,且反应釜应装有________装置。
②玻璃钢中玻璃纤维的作用是______。玻璃钢具有 等优异性能(写出两点即可)。
③下列处理废旧热固性酚醛塑料的做法合理的是________。
a.深埋b.粉碎后用作树脂填料
c.用作燃料 d.用有机溶剂将其溶解,回收树脂
(3)工业上主要采用氨氧化法生产硝酸,如图是氨氧化率与氨-空气混合气中氧氨比的关系。其中直线表示反应的理论值;曲线表示生产实际情况。当氨氧化率达到100%,理论上r[n(O2)/n(NH3)]=_____,实际生产要将r值维持在1.7~2.2之间,原因是__________________________。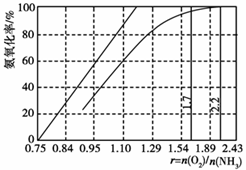
运用化学反应原理研究碳、氮的单质及其化合物的反应对缓解环境污染、能源危机具有重要意义。
(1)液氨作为一种潜在的清洁汽车燃料已越来越被研究人员重视。它在安全性、价格等方面较化石燃料和氢燃料有着较大的优势。氨的燃烧实验涉及下列两个相关的反应:
①4NH3(g)+5O2(g)=4NO(g)+6H2O(l) △H1
②4NH3(g)+6NO(g)=5N2(g)+6H2O(l) △H2
则反应4NH3(g)+3O2(g)=2N2(g)+6H2O(l) △H= 。(请用含有△H1、△H2的式子表示)
(2)NO和CO气体均为汽车尾气的成分,这两种气体在催化转换器中发生如下反应:2NO(g)+ 2CO(g) 2CO2(g)+ N2(g) △H=—a kJ•mol-1(a>0)。在一定温度下,将2.0mol NO、2.4mol CO气体通入到固定容积为2L的密闭容器中,反应过程中部分物质的浓度变化如图所示:
2CO2(g)+ N2(g) △H=—a kJ•mol-1(a>0)。在一定温度下,将2.0mol NO、2.4mol CO气体通入到固定容积为2L的密闭容器中,反应过程中部分物质的浓度变化如图所示: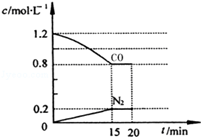
①0~15min N2的平均速率v(N2)= 。
②20min时,若改变反应条件,导致CO浓度减小,则改变的条件可能是 (选填序号)。
a.缩小容器体积b.增加CO的量
c.降低温度d.扩大容器体积
③若保持反应体系的温度不变,20min时再向容器中充入NO、N2各0.4mol,化学平衡将 移动(选填“向左”、“向右”或“不”)。
(3)某研究小组在实验室用某新型催化剂对CO、NO催化转化进行研究,测得NO转化为N2的转化率随温度、CO混存量的变化情况如下图所示,利用以下反应:
NO+CO N2+CO2(有CO) 2NO
N2+CO2(有CO) 2NO N2+O2(无CO)
N2+O2(无CO)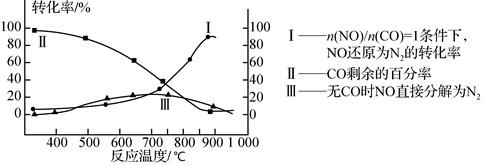
①若不使用CO,温度超过775 ℃,发现NO的分解率降低,其可能的原因为 ;在n(NO)/n(CO)=1的条件下,应控制最佳温度在 左右。
②用CxHy(烃)催化还原NOx也可消除氮氧化物的污染。写出C2H6与NO2发生反应的化学方程式 。
本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容。请选定其中一题,并在相应的答题区域内作答。若两题都做,则按A题评分。
A.[物质结构与性质]原子序数依次增大的A、B、C、D、E、F六种元素。其中A的基态原子有3个不同的能级,各能级中的电子数相等;C的基态原子2p能级上的未成对电子数与未成对电子数相等;D为它所在周期中原子半径最大的主族元素;E和C位于同一主族,F的原子序数为24。
(1)F+基态的核外电子排布式为 。
(2)BA3-的空间构型为 ;1molAD2中含有π键的数目为 。
(3)由A、B、C形成的离子CAB-与AC2互为等电子体,则CAB-的结构式为 。
(4)在元素A与E所形成的常见化合物中,A原子轨道的杂化类型为 。
(5)由B、C、D三种元素形成的化合物晶体的晶胞如图所示,则该化合物的化学式为 。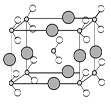
氮可以形成多种化合物,如NH3、N2H4、HCN、NH4NO3等。
(1)已知:N2(g)+2H2(g)=N2H4(l)△H=" +" 50.6kJ·mol-1
2H2(g)+O2(g)=2H2O(l)△H="-571.6" kJ·mol-1
则①N2H4(l)+O2(g)=N2(g)+2H2O(l)△H= kJ·mol-1
②用次氯酸钠氧化氨,可以得到N2H4的稀溶液,该反应的化学方程式是 。
(2)污水中的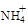 可以用氧化镁处理,发生如下反应:
可以用氧化镁处理,发生如下反应:
MgO+H2O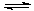 Mg(OH)2Mg(OH)2+2NH4+
Mg(OH)2Mg(OH)2+2NH4+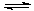 Mg2+ +2NH3·H2O。
Mg2+ +2NH3·H2O。
①温度对氮处理率的影响如图所示。在25℃前,升高温度氮去除率增大的原因是 。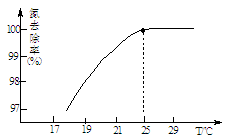
②剩余的氧化镁,不会对废水形成二次污染,理由是 。
(3)污水中的含氮化合物,通常先用生物膜脱氮工艺进行处理,在硝化细菌的作用下将NH4+氧化为
NO3-(2NH4++3O2=2HNO2+2H2O +2H+;2HNO2 +O2=2HNO3)。然后加入甲醇,甲醇和NO3-反应转化为两种无毒气体。
①上述方法中,14g铵态氮元素转化为硝态氮元素时需氧的质量为 g。
②写出加入甲醇后反应的离子方程式: 。
(4)甲醇燃料电池的工作原理如图所示,则该电池负极的电极反应式为 。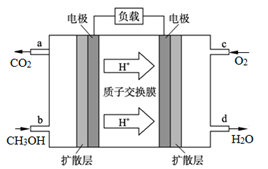
硼镁矿属于硼酸盐,可用来制备硼酸(H3BO3)和MgO,方法如下:硼镁矿粉与(NH4)2SO4溶液混合后加热,反应生成H3BO3晶体和MgSO4溶液,同时放出NH3;再向MgSO4溶液中通入NH3与CO2,得到MgCO3沉淀和滤液,沉淀经洗涤、煅烧后得MgO,滤液则循环使用。回答下列问题:
(1)与硅酸盐类似,硼酸盐结构也比较复杂,如硬硼钙石化学式为Ca2B6O11·5H2O,将其改写为氧化物的形式 。
(2)上述制备过程中,检验沉淀洗涤是否完全的方法是 。
(3)写出MgSO4溶液中通入NH3与CO2反应的化学方程式 。
(4)若准确称取1.68 g硼镁矿,完全反应后得H3BO3晶体1.24 g,MgO 0.8 g,计算该硼酸盐的组成。(写出计算过程)