电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。某工程师为了从使用过的腐蚀废液中回收铜,并重新获得氯化铁溶液,准备采用下列步骤:

(1)请写出上述实验中加入或生成的有关物质的化学式:
③ ④ ⑤ ⑥
(2)合并溶液通入⑥的离子反应方程式________________ 。
(3)若向废液中加入任意质量的①物质,下面对充分反应后的溶液分析合理的是
| A.若无固体剩余,则溶液中一定有Fe3+ |
| B.若有固体存在,则溶液中一定没有Cu2+ |
| C.若溶液中有Cu2+,则一定没有固体析出 |
| D.若溶液中有Fe3+,则一定还有Cu2+ |
(4)若向②中加入氢氧化钠溶液,其实验现象为 。
某课题小组合成一种复合材料的基体M的结构简式为: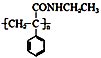
合成路线如下: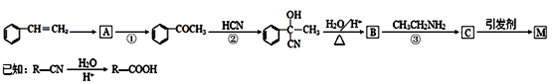
请回答下列问题:
(1)写出A的结构简式____。②的反应类型为____。
(2)B中含有的官能团有。D的名称(系统命名)是。
(3)写出反应⑤的化学方程式____。
(4)写出符合下列条件:①能使FeCl3溶液显紫色;②苯环只有二个取代基;③与新制的Cu(OH)2悬浊液混合加热,有砖红色沉淀生成;④苯环上一氯代物有2种同分异构体。写出有机物B的一种同分异构体的结构简式。
(5)下列说法正确的是。
a.E与分子式相同的醛互为同分异构体
b.F的分子式为C9Hl0NO
c.CH3CH2NH2能与盐酸反应
d.C分子中苯环上取代基含2个 健
健
(12分)己知X、Y、Z、W、N、U、V是短周期的主族元素,原子序数依次增大。X与N同主族,且与W都能形成A2B、A2B2型化合物;Z、W的单质常温下均为无色气体;Y原子的L层电子数是K层电子数的2倍;U原子的最外层电子数是其电子层数的2倍,试回答下列问题:
(1)YW2的电子式;Z的氢化物结构式为;
写出U元素在周期表中的位置。
(2)离子半径:N+W2-(填>、<或=);
(3)写出Y2X4与V元素的单质在水溶液中反应的化学方程式是。
(4)由N、W组成A2B2型的一种化合物,该物质属于(填“离子”或“共价”)化合物。
(6分)现有CH4、C2H4、C6H6三种有机物:
(1)等质量的三种气体完全燃烧时生成水最多的是________;
(2)同状况、同体积的三种气体完全燃烧时耗去O2的量最多的是________。
(3)在150℃、1.01×105 Pa下时,有两种气态烃和足量的氧气混合点燃,相同条件下测得反应前后气体体积没有发生变化,这两种气体是________。
(6分)完成下列化学反应方程式并注明反应类型。
1、乙烯与水一定条件下反应
2、甲烷与氯气光照条件下反应(只写第一步)
3、苯与浓硝酸,浓硫酸一定条件下反应
下列各组物质①O2和O3②12C和14C ③CO(NH2)2和NH4CNO④CH3CH2CH2CH3和(CH3)2CHCH3
⑤CH2=CH2和CH3CH=CH2⑥CH3CH2CH2CH(C2H5)CH3和CH3CH2CH2CH(CH3)C2H5
互为同系物的是__________,互为同分异构体的是_____________
互为同位素的是______,互为同素异形体的是_________,
是同一物质的是__________。