(1)分别用等体积的蒸馏水和0.01mol/L硫酸洗涤BaSO4沉淀,用水洗涤造成BaSO4的损失量大于用稀硫酸洗涤的损失量。原因是
(请结合平衡移动原理,用相关的化学用语及文字表述回答。)
(2)Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s) Cr3+(aq)+3OH-(aq),常温下,Cr(OH)3的溶度积Ksp=10-32,要使c(Cr3+)降至10-5 mol/L时,溶液的pH应调至
Cr3+(aq)+3OH-(aq),常温下,Cr(OH)3的溶度积Ksp=10-32,要使c(Cr3+)降至10-5 mol/L时,溶液的pH应调至
(3)实验证明,多元弱酸的分步电离一步比一步困难。原因是
(提示:可以从粒子的电荷情况和电离平衡的移动两方面加以考虑)
(4)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl-),则溶液是 (填“酸”、“碱”或“中”)性;用含a的代数式表示NH3·H2O的电离常数Kb=
某无色溶液,由Na+、Ag+、Ba2+、Al3+、AlO2-、MnO4-、CO32-、SO42-、SiO32-中的
若干种组成(不考虑水的电离)。取该溶液进行如下实验:
Ⅰ.取适量溶液,加入过量的盐酸,有气体生成,并得到无色溶液;
Ⅱ.在Ⅰ所得溶液中加入过量的NH4HCO3溶液,有气体生成,同时析出白色沉淀甲;
Ⅲ. 在Ⅱ所得溶液中加入过量的Ba(OH)2溶液,加热,也有气体生成,同时析出白色沉淀乙。
请回答下列问题:
(1)由实验Ⅰ可知原溶液中一定不含有的离子是;
一定含有的离子是。
(2)由实验Ⅱ可知原溶液溶液中还一定含有的离子是;生成甲的离子方程式为。
(3)实验Ⅲ中生成白色沉淀乙的离子方程式为
。
原溶液中还可能存在的离子是;检验该离子的方法是。
已知A、B、C、D、E、F、G为七种短周期的主族元素,原子序数依次增大。已知:A、F的最外层电子数分别等于各自的电子层数,其中A的单质在常温下为气体。C与B、G在元素周期表中处于相邻位置,这三种元素最外层电子数之和为17,质子数之和为31。D与F同周期,且在该周期中D元素的原子半径最大。根据以上信息回答下列问题:
(1)B、C、G的氢化物中稳定性最强的是(填化学式),G的某种氧化物能使溴水褪色,写出该反应的化学方程式。
(2)B、C、D、E、F形成的简单离子半径由大到小的顺序为(用离子符号表示)。
(3)A与B能形成离子化合物A5B,A5B中既含离子键又含共价键,其电子式为,该物质能与水剧烈反应生成两种气体,这两种气体的化学式是。
(4)碳酸盐DACO3溶液与稀硫酸混合,当生成11.2L(标准状况)气体(不考虑气体溶解)时放热6.32kJ,写出该反应的热化学离子方程式。
(5)美国国家科学院(NationalAcademyofSciences)正式发表了题为《行星系统中有机生命的限制》的研究报告。报告称,在温度、压力、物质基础以及能源供给方式都与地球迥异的地外行星上,如果存在生命,它们完全没有必要以地球生命的形式存在。有学者提出,在大气中充满B元素单质并含有丰富的A的化合物的星球上可能存在“B基生命”而不是“碳基生命”。科学家猜想这样的星球上可能会存在着一种组成结构与BA3、B2A4类似的系列化合物如B3A5、B4A6等。该系列化合物的通式为(用元素符号表示)。有B2A 4与另外两种等物质的量的该系列中的化合物组成的混合蒸气,在足量氧气中充分燃烧,只生成B元素的单质和水,且B元素的单质和水的物质的量之比为1:2,则另外两种化合物是(写化学式)。
恒温下,将a mol N2与b mol H2的混合气体通入一定容积的密闭容器中,发生如下反应:N2(g)+3H2(g) 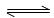 2NH3(g)
2NH3(g)
(1)若反应进行到某时刻t时,n(N2)=13mol,n(NH3)=6mol,
计算a=。
(2)反应达到平衡时,混合气体的体积为716.8L(标准状况下),其中NH3的百分含量(体积分数)为25%。计算:平衡时NH3的物质的量为。
(3)原混合气体与平衡混合气体的总物质的量之比
n(始): n(平)=。
(4)原混合气体中a : b=。
(5)达到平衡时,N2和H2的转化率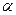 (N2):
(N2): 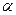 (H2)=。
(H2)=。
(6)平衡混合气体中n(N2): n(H2): n(NH3)=。
A、B、C、D、E为中学常见的五种物质,均含元素Y,有的还可能含有元素X、Z,元素X、Y、Z的原子序数依次递增。
①元素Y在A、B、C、D、E中所呈现的化合价依次递增,其中只有B为单质;
②常温下将气体D通入水中发生反应,生成E和C;
③工业上可以用A与空气为原料,通过催化氧化法得到C。
请回答以下问题:
(1)B的电子式为,A的结构式为,A分子的空间构型是。
(2)写出②中反应的化学方程式
(3)写出③中反应的化学方程式
将等物质的量的A、B、C、D四种物质混合,发生下列反应:
aA+bB cC(固)+dD。当反应进行一定时间后,测得A减少了n mol,
cC(固)+dD。当反应进行一定时间后,测得A减少了n mol,
B减少了n/2 mol,C增加了3n/2 mol,D增加了n mol,此时达到化学平衡。
(1)该化学方程式中各物质的系数为:a=_____,b=_____,c=_____,d=_____
(2)若只改变压强,反应速率发生变化,但平衡不发生移动,该反应中各物质的状态为:A_______, B________, C_______
(3)若只升高温度,反应一段时间后测知四种物质的量又相等,则该反应的正反应为________反应(填“放热”或“吸热”)。