某学生欲完成2HCl+2Ag=2AgCl↓+H2↑反应,设计了下列四个实验,你认为可行的实验是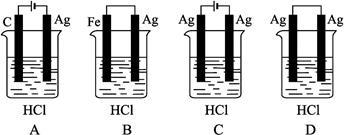
根据下图所示的装置,判断下列说法正确的是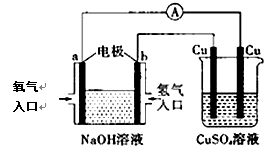
| A.该装置中a极为负极 |
| B.该装置中b极的电极反应式是:2H++2e-= H2↑ |
| C.一段时间后,左边装置中溶液pH增大 |
| D.CuSO4溶液浓度保持不变 |
等质量的两份锌粉a、b分别加到两份质量相同的过量的稀硫酸中,同时向a中加入少量的CuSO4溶液,下列各图为产生H2的体积V(L)与时间t(min)的关系,其中正确的是
将V1 mL 1.0 mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50 mL)。下列叙述正确的是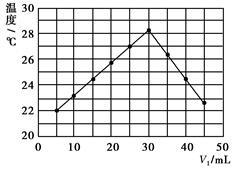
| A.做该实验时环境温度为22 ℃ |
| B.该实验表明化学能可以转化为热能 |
| C.NaOH溶液的浓度约是1.00 mol/L |
| D.该实验表明有水生成的反应都是放热反应 |
下列有关热化学方程式的叙述正确的是
| A.已知2H2(g)+O2(g)=2H2O(g) △H =-483.6kJ·mol-1,则氢气的标准燃烧热为-483.6kJ/mol |
| B.ΔH的数值与化学反应方程式的化学计量系数无关 |
| C.含20.0g NaOH的稀溶液与稀硫酸完全中和,放出28.7kJ的热量,则该反应的热化学方程式为:NaOH(aq)+1/2H2SO4(aq)=1/2Na2SO4(aq)+H2O(l) △H =-57.4 kJ·mol-1 |
| D.己知C(s)+O2(g)=CO2(g) △H1;C(g)+O2(g)=CO2(g) △H2,则△H1﹤△H2 |