某小组同学采用以下装置验证SO2的性质:(夹持及加热装置略)

(1)写出圆底烧瓶中发生反应的化学方程式: 。
(2)从实验目的分析,试管1、4的目的都是为了证明SO2具有 (性质),试管2是为了证明SO2具有 (性质)。
(3)除上述两种性质外,你认为SO2还具有的性质是 ,可以通过加入 (填试剂化学式或者名称)加以证明。
(4)经过实验,观察到如下实验现象:
① 试管1中 。
② 试管2中有浅黄色浑浊出现,写出反应的化学方程式 。
(5)试管4中无明显现象,将其分成两份,分别加入下列物质均产生沉淀。将产生的沉淀的化学式填入下表相应位置。
| 加入的物质 |
O2 |
氨水 |
| 沉淀的化学式 |
|
|
(6)试管4和试管5均加入NaOH溶液,在实验目的上的不同点是 。
[化学——选修2:化学与技术](15分)草酸(乙二酸)可作还原剂和沉淀剂,用于金属除锈、织物漂白和稀土生产。一种制备草酸(含2个结晶水)的工艺流程如下:
回答下列问题:
(1)CO和NaOH在一定条件下合成甲酸钠、甲酸钠加热脱氢的化学反应方程式分别为、。
(2)该制备工艺中有两次过滤操作,过滤操作②的滤液是和,滤渣是。
(3)工艺过程中③和④的目的是。
(4)有人建议甲酸钠脱氢后直接用硫酸酸化制备草酸。该方案的缺点是产品不纯,其中含有的杂质主要是____________________。
(5)结晶水合草酸成品的纯度用高锰酸钾法测定。称量草酸成品0.250 g溶于水,用0.050 0 mol·L-1的酸性KMnO4溶液滴定,至浅粉红色不消褪,消耗KMnO4溶液15.00 mL,反应的离子方程式为;列式计算该成品的纯度。
某研究性学习小组对Zn跟一定量的浓硫酸反应生成的气体产物进行探究。
【提出假设】:小组同学经过分析讨论认为生成气体可能含H2和SO2。
【设计实验方案,验证假设】主要包括两个环节:
Ⅰ.验证SO2,实验装置如图所示;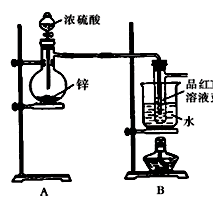
Ⅱ.检验产物中含有H2,实验内容将由B部分导出的气体依次通过装置
C、D、E、F、G。Ⅱ中装置C、D、E、F、G的信息如下表所示:
| 仪器标号 |
C |
D |
E |
F |
G |
| 仪器 |
洗气瓶 |
洗气瓶 |
硬质玻璃管,加热 |
干燥管 |
干燥管 |
| 仪器中所加物质 |
NaOH溶液 |
浓硫酸 |
CuO粉末 |
试剂X |
无水CaCl2固体 |
试回答下列问题:
(1)小组同学认为生成气体中含H2的理由是;
(2)盛放锌粒的仪器名称是;
(3)B部分装置的目的是验证SO2并探究SO2与品红作用的可逆性,实验的操作及主要现象是;
(4)①装置D、G的作用依次是、;
②E中发生反应的化学方程式是;
③试剂X是。
工业上以粗食盐(含有少量Ca2+、Mg2+杂质)、氨、石灰石等为原料,可以制备Na2CO3 。其过程如下图所示。
请回答:(1)在处理粗盐水的过程中,可加入石灰乳和纯碱作为沉淀剂,则所得滤渣的成分除过量的沉淀剂外还有___________________________________。
(2)将CaO投入含有大量的NH4C1的母液中,能生成可循环使用的NH3,该反应的化学方程式是__________________________________。
(3)向饱和食盐水中首先通入的气体是_______________________,过程III中生成NaHCO3晶体的反应的化学方程式是_________________________________________________________。
(4)碳酸钠晶体失水的能量变化示意图如下:
Na2CO3·H2O(s)脱水反应的热化学方程式是。
(5)产品纯碱中常含有NaCl。取ag混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得bg固体。则该产品中Na2CO3的质量分数是。
(6)熔融Na2CO3可作甲烷-空气燃料电池的电解质,该电池负极的反应式是_________________。
实验室可用MnO2和KClO3混合加热的方法制取氧气。现有下列仪器或装置:
Ⅰ.(1)A~D装置中,用作KClO3为原料制氧气的反应装置是(填序号);
(2)排水法收集氧气,接口顺序是:氧气出口→→→g→h→烧杯(填序号)。
Ⅱ. KClO3分解时尚有副反应,导致收集到的气体有异味.据推测,副产物可能是O3、Cl2、ClO2中的一种或几种.资料表明:O3、Cl2、ClO2的沸点依次为-111℃、-34℃和11℃,且O3、ClO2也能将KI氧化为I2.为探究副反应气体产物的成分,将KClO3分解产生的气体经干燥后通入下图装置进行实验:
(3)若要确认副产物中含Cl2,F中应盛放溶液。
(4)确定副产物中含有ClO2的现象是。
(5)实验时若D中无现象,E中试纸变蓝,能否得出副产物含有O3的结论?理由是。
Ⅲ.ClO2是饮用水消毒剂.用ClO2处理过的饮用水(pH为5.5~6.5)除含有ClO2外,常含有一定量对人体不利的ClO2-.为测定此饮用水中两者成分,进行如下实验:准确量取VmL水样加入到锥形瓶中,调节水样pH=8,加人足量KI晶体,发生如下反应:2ClO2+2I-═I2+2ClO2-,反应结束后产生amol I2;继续调节溶液pH=1,又发生如下反应:ClO2-+4H++4I-═2I2+Cl-+2H2O,反应结束后叉产生b mol I2。
(6)饮用水中c(ClO2-)=mol•L-1(用含字母的代数式表示)。
为研究铁质材料与热浓硫酸的反应,某学习小组用碳素钢(即铁和碳的合金)进行了以下探究活动:
【探究一】
(1)常温下,工业上用铁质容器盛放冷的浓硫酸,其原因是。
(2)称取碳素钢6.0g放入15.0mL浓硫酸中,加热,充分反应后得到溶液X并收集到混合气体Y。
①甲同学认为X中除Fe3+之外还可能含有Fe2+。若要确认其中的Fe2+,应选用(选填序号)。a.KSCN溶液和氯水 b.铁粉和KSCN溶液 c.浓氨水 d.酸性KMnO4溶液
②乙同学取560mL(标准状况)气体Y通入足量溴水中,然后加入足量BaCl2溶液,经适当操作后得干燥固体4.66g,由此可求算气体Y中SO2的体积分数。
写出探究②中出现的所有离子反应方程式。
【探究二】
根据上述实验中SO2体积分数的分析,丙同学认为气体Y中还可能含有Q1和Q2两种气体,其中Q1气体,在标准状况下,密度为0.0893g·L-1。为此设计了下列探究实验装置(图中夹持仪器省略,假设有关气体完全反应)。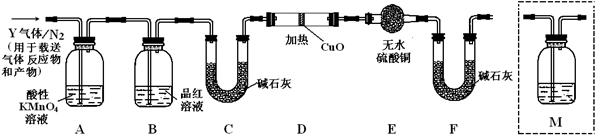
(3)装置B中试剂的作用是。
(4)分析Y气体中的Q2气体是如何生成的。(用化学方程式表示)。
(5)为确认Q2的存在,需在装置中添加洗气瓶M于(选填序号)。
a.A之前 b.A-B间 c.B-C间 d.C-D间
(6)如果气体Y中含有Q1,预计实验现象应是。