某探究小组同学用金属铝分别与稀盐酸或稀硫酸反应的方法研究金属与不同酸反应的差异及影响反应速率的因素.
实验药品:2.0moL/L盐酸、4.0mol/L盐酸、2.0mol/L硫酸、4.0mol/L硫酸,质量和相同的铝片和铝粉(金属表面氧化膜都已除去);每次实验各种酸的用量均为50.0mL,金属用量均为9.0g.
(Ⅰ)甲同学用铝片分别和稀盐酸、稀硫酸反应,实验及其现象如下:
| 反应进程(分钟) |
1 |
2 |
5 |
15 |
20 |
| 4.0mol/L盐酸 |
少量气泡 |
较多气泡 |
大量气泡 |
反应剧烈 |
反应结束 |
| 2.0mol/L硫酸 |
无明显现象 |
极少量气泡 |
少量气泡 |
||
| 4.0mol/L硫酸 |
无明显现象 |
少量气泡 |
有比较连续的气泡 |
请回答:
(1)写出铝与盐酸反应的离子方程式 .
(2)反应1~15min内,铝与盐酸的反应速率逐渐加快,其原因是 .
(3)以上探究铝与稀盐酸、稀硫酸反应速率有差异,你认为其原因有哪些可能?请提出你的假设(写出2种可能):
(Ⅱ)(1)乙同学设计了如下影响反应速率因素的实验(温度控制为25℃和35℃).请你根据实验目的帮助该同学完成以下实验设计表(用量:酸均为50.0mL、铝为9.0g过量):
| 实验目的 |
实验 编号 |
温度 |
金属铝 形态 |
盐酸浓度 /mol·L﹣1 |
| 1 实验①和②探究盐酸浓度对该反应速率的影响; 2实验①和③探究温度对该反应速率的影响; 3实验①和④探究金属规格(铝片、铝粉)对该反应速率的影响. |
① |
25˚C |
铝片 |
4.0 |
| ② |
|
|
|
|
| ③ |
|
|
|
|
| ④ |
|
|
|
过氧化镁MgO2易溶于稀酸,溶于酸后会产生过氧化氢,在医学上可作为“解酸剂”等。过氧化镁产品中常会混有一定量的MgO,实验室可通过多种方案测定样品中过氧化镁的含量。某研究小组拟用下图装置测定一定质量的样品中过氧化镁的含量。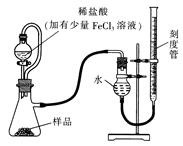
(1)实验前需进行的操作是:,稀盐酸中加入少量FeCl3溶液的作用是:。
(2)用恒压分液漏斗的优点有:①;②。
实验结束时,待恢复至室温,先,再平视刻度线读数。实验室还可通过下列两种方案来测定样品中过氧化镁的含量:
方案I:取a g样品,加入足量稀盐酸,充分反应后再加入 NaOH溶液至Mg2+沉淀完全,过滤、洗涤后,将滤渣充分灼烧,最终得到b g固体。
(3)推算该样品中过氧化镁的质量分数(用含a、b的表达式表示)。
方案Ⅱ:称取0.1 g样品置于某定量用锥形瓶中,加入15 mL0.6 mol/LKI溶液和足量盐酸,摇匀后在暗处静置5 min,然后用0.1000 mol/L Na2S2O3溶液滴定,滴定到终点时共消耗28.50 mL Na2S2O3溶液。(已知:I2+2Na2S2O3→Na2S4O6+2NaI)
(4)该实验在滴定前需加入少量作指示剂;判断到达滴定终点的现象是;
(5)推算该样品中过氧化镁的质量分数为。
水中因含有机物而具有较高的化学耗氧量。常用酸性KMnO4氧化有机物测其含量。主要操作步骤如下:
(1)仪器A为(填酸式或碱式)滴定管;要顺利完成实验,步骤Ⅲ中溶液颜色应为。
(2)完善步骤Ⅳ涉及的离子方程式:
C2O42—+MnO4—+=Mn2++CO2↑+
该步骤中KMnO4溶液紫色会逐渐褪去.某探究小组测得某次实验(恒温)时溶液中Mn2+物质的量与时间关系如图.
请解释n(Mn2+)在反应起始时变化不大、一段时间后快速增大的原因:
(3)若步骤Ⅳ中所用Na2C2O4溶液为20.00ml,已知滴定后的液面如图所示,请写出滴定前的液面读数。
(4)若实验测量结果比实际有机物含量偏高,分别从以下两个方面猜想:
猜想1:水样中Cl—影响
猜想2:配制Na2C2O4标液定容时。
(5)若猜想1成立,请根据资料卡片补充完善上述实验以消除Cl—影响。(限选试剂:AgNO3溶液、Ag2SO4溶液、KMnO4溶液、Na2C2O4溶液)。
资料卡片:
1、有机物可被HNO3氧化。
2、AgCl不与酸性KMnO4溶液反应。
3、Ag2C2O4可被酸性KMnO4溶液氧化。
为保护环境,节约资源,某研究性学习小组探究用易拽罐制取明矾[KAl(SO4)2·12H2O]。
查阅资料得知:明矾溶于水,不溶于乙醇:易拉罐主要成分为铝,另含有镁、铁等。
实验步骤如下:
步骤1、将易拉罐剪开,裁成铝片。用砂纸磨去表面的油漆,颜料及透明塑胶内衬:
步骤2、制备NaAlO2
称量1 g上述处理过的铝片,切碎,分数次放入盛有40mL5% NaOH溶液的烧杯中:将烧杯置于热水浴中加热。反应完毕后,溶液呈灰黑色浑浊,趁热过滤。
步骤3、氢氧化铝的生成和洗涤
在所得滤液中滴加3mol·L-1H2SO4溶液,用pH试纸检验,调节pH至8~9为止:此时溶液中生成大量的白色氢氧化铝沉淀,过滤,并用热蒸馏水多次洗涤沉淀
步骤4、明矾的制备
将过滤后所得氢氧化铝沉淀转入蒸发皿中,加10 mL 9mol/L H2SO4,再加15 mL水,小火加热使其溶解,加入4g硫酸钾继续加热至溶解,将所得溶液在空气中自然冷却,待结晶完全后,过滤,用无水酒精洗涤晶体两次;将晶体用滤纸吸干,制得明矾。
回答以下问题:
(1)步骤2中铝片溶于烧碱的反应建议在通风橱中进行,用热水浴加热,避免明火,原因是;过滤后,滤渣的主要成分是。
(2)步骤3中,若调节pH过低,导致的结果是;洗涤氢氧化铝沉淀的方法是。
(3)步骤4中用到的主要仪器是:铁架台(带铁圈),蒸发皿、量筒、漏斗、烧杯、酒精灯和;加入硫酸钾后制取明矾的化学反应方程式是。
(4)不用水而用无水酒精洗涤明矾晶体的原因是。
(5)实验验证明矾晶体中含有SO42—离子的方法是。
(6)该实验制得明矾15.8 g,则称取的1 g铝片中铝元素含量不低于%。
实验室欲配制80mL,1.5 mol/L的NaHCO3溶液,试回答:
(1)该实验必须使用的玻璃仪有;
(2)配置该溶液时应称取NaHCO3的质量为_____________________;(3)下列操作对上述所配溶液物质的量浓度的影响(填写无影响、偏高或偏低)
A.配制过程中未洗涤烧杯和玻璃棒;
B.容量瓶使用之前未烘干,有少量蒸馏水;
C.定容时俯视容量瓶的刻度线;
D.将所配溶液从容量瓶转移到试剂瓶时,有少量液体溅出;__________
写出下列反应的离子方程式:
A.向NaHCO3溶液中滴加盐酸
B.向Ba(OH)2溶液中滴加少量NaHCO3溶液
C.向氨水中滴加MgCl2溶液
(9分)某学生用已知物质的量浓度的盐酸来测定未知浓度的氢氧化钠溶液时,选择甲基橙作指示剂。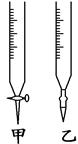
请填写下列空白:
(1)酸式滴定管用蒸馏水洗净后,接下来应该进行的操作是_________。
(2)用标准盐酸溶液滴定时,应将标准盐酸溶液注入________(填“甲”或“乙”)中。
(3)用标准的盐酸滴定待测的氢氧化钠溶液时,左手握酸式滴定管的活塞,右手轻轻摇动锥形瓶,眼睛注视_______________________________________________________。
(4)直到因加入一滴盐酸后,溶液颜色由________色变为________色,并在30 s内不变,即为终点。
(5)下列操作中可能使所测氢氧化钠溶液浓度偏大的是________。
| A.酸式滴定管未用标准盐酸润洗,直接装入标准盐酸。 |
| B.酸式滴定管滴定前有气泡,滴定后气泡消失。 |
| C.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后未干燥。 |
| D.读取盐酸体积开始时仰视读数,滴定结束后俯视读数。 |